HRD und BRCA1/2 beim Ovarialkarzinom
Bedeutung und Prävalenz von HRD und BRCA1/2-Mutationen beim Ovarialkarzinom
Etwa 90 % der Ovarialkarzinome sind epithelialen Ursprungs.1 Etwa die Hälfte der epithelialen Ovarialkarzinome weist genomische Veränderungen auf, die durch eine homologe Rekombinationsdefizienz (HRD) verursacht werden. Bei 27–29 % liegt eine Mutation im Breast Cancer Associated Gene 1 (BRCA1) oder Breast Cancer Associated Gene 2 (BRCA2) vor, bei weiteren 19 % ist die HRD durch Mutationen in anderen Genen der homologen Rekombinationsreparatur (HRR) oder durch chromosomale Strukturveränderungen verursacht.2-4
Störungen der HRR – etwa durch BRCA1/2-Mutationen – erhöhen nicht nur das Risiko für eine Tumorentstehung, sondern sind zugleich therapeutisch relevant.
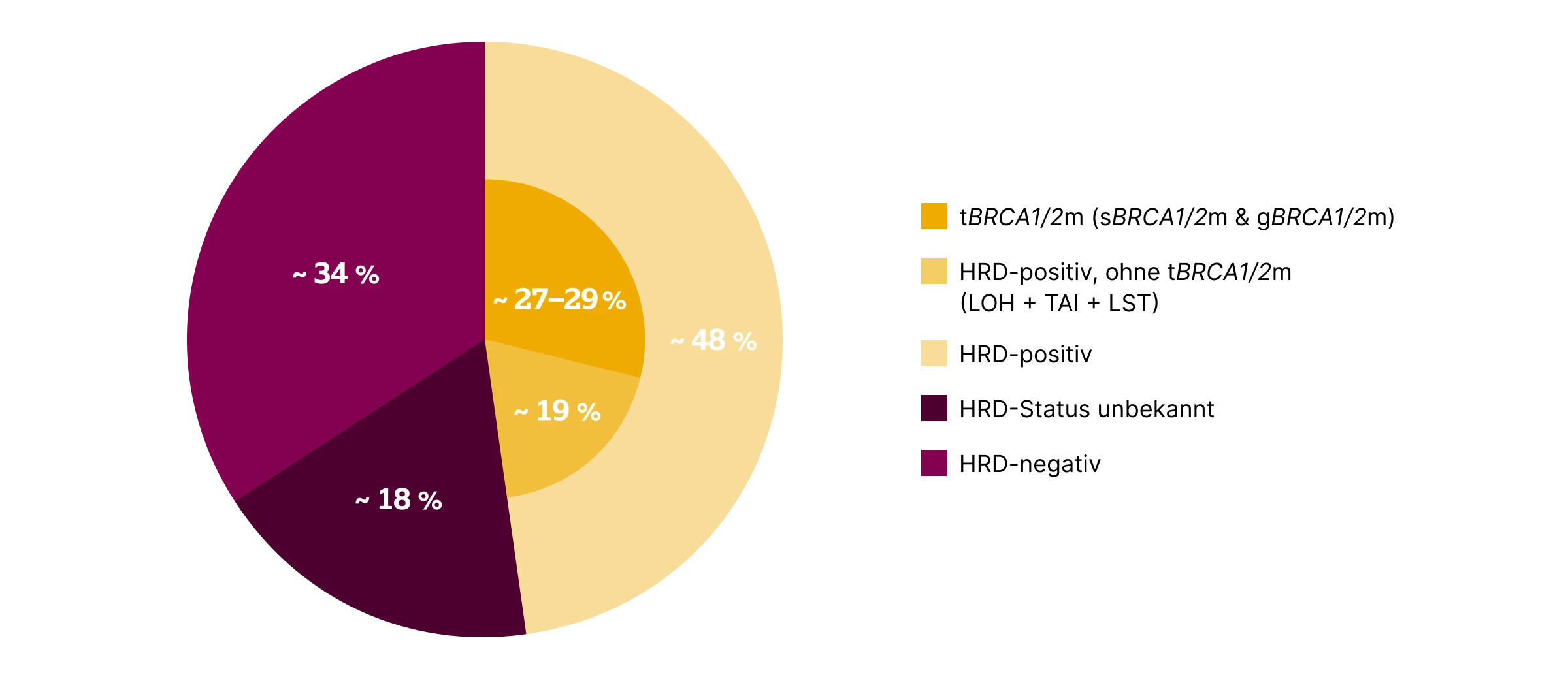
Relevanz der HRD- und BRCA1/2-Testung beim Ovarialkarzinom
Ursprünglich wurden BRCA1/2-Mutationen hauptsächlich als Risikofaktoren für familiäre Mamma- und Ovarialkarzinome betrachtet. Heute gilt der Nachweis von BRCA1/2-Mutationen zudem als wichtiger Biomarker für die Therapieplanung, unter anderem beim Mamma-, Ovarial-, Pankreas- und Prostatakarzinom.5-8
Patientinnen mit einem Ovarialkarzinom können bei Nachweis einer HRD und unter bestimmten Voraussetzungen von einer zielgerichteten Erhaltungstherapie mit Poly(ADP-ribose)-Polymerase (PARP)-Inhibitoren profitieren. Diese Therapieoptionen stehen sowohl Patientinnen mit somatischen und/oder Keimbahnmutationen in BRCA1/2 als auch jenen zur Verfügung, die keine BRCA1/2-Mutation, jedoch HRD-bedingte Genomschäden (genomische Instabilität) aufweisen.9,10
Studien- & Leitlinienempfehlungen zur HRD- und BRCA1/2-Testung beim Ovarialkarzinom
S3-Leitlinie: Empfehlung zur genetischen Testung für alle Patient:innen mit Ovarialkarzinom
In der aktuellen S3-Leitlinie wird empfohlen, dass alle Patientinnen mit Diagnose eines Ovarialkarzinoms über das Risiko einer erblichen Erkrankung aufgeklärt werden sollen. Den Betroffenen soll ein genetischer Test angeboten werden.5
Darüber hinaus unterstreicht die S3-Leitlinie die Bedeutung der Testung auf BRCA1/2-Mutationen und HRD für die individualisierte therapeutische Entscheidungsfindung bei Patientinnen mit fortgeschrittenem Ovarialkarzinom.5
ESMO: Molekulare Testung für alle Patientinnen mit high-grade Ovarialkarzinom
Die ESMO-Empfehlungen sprechen sich dafür aus, bei allen Patientinnen mit neu diagnostiziertem high-grade Ovarialkarzinom eine routinemäßige molekulargenetische Testung auf BRCA1/2-Mutationen (somatisch und/oder in der Keimbahn) durchzuführen. Bei fortgeschrittenen high-grade Karzinomen wird außerdem ein Test auf genomische Instabilität (HRD) empfohlen. Entscheidungen zur systemischen Therapie – insbesondere zur Erhaltungstherapie – sollten bei Patientinnen mit epithelialem Ovarialkarzinom (FIGOStadium III‑-I‑V) auf dem BRCA1/2- und HRD-Status basieren. Daher ist die molekulare Testung bereits bei Primärdiagnose sinnvoll.1
ESGO-ESMO-ESP-Konsensus: Aktualisierung der europäischen Empfehlungen
Der im Jahr 2024 veröffentlichte multidisziplinäre Konsensus der ESGO, ESMO und ESP aktualisiert und erweitert die bisherigen europäischen Empfehlungen zur molekularen Diagnostik beim Ovarialkarzinom.10 Empfohlen wird eine molekulargenetische Testung auf BRCA1/2-Mutationen (Keimbahn und/oder somatisch) bei allen Patientinnen mit high-grade nicht-muzinösem epithelialem Tuben-/ Ovarialkarzinom, unabhängig vom Erkrankungsstadium und bereits bei Erstdiagnose. Zusätzlich sollte bei Patientinnen mit BRCA1/2-Wildtyp-Tumoren im FIGO-Stadium III-IV eine Testung auf genomische Instabilität (HRD) erfolgen, da diese wichtige prädiktive Informationen für die Therapieplanung liefert.10
Betont wird zudem die Verwendung klinisch validierter HRD-Tests. Für die molekulare Diagnostik wird eine geeignete chirurgisch entnommene oder bildgesteuert gewonnene Probe des therapienaiven Primärtumors empfohlen. Diese sollte vorzugsweise einen Tumorzellgehalt von mindestens 30 % aufweisen. Alternativ können auch Zellblockpräparate aus peritonealen oder pleuralen Ergüssen verwendet werden.10

a High-grade seröses Karzinom oder endometrioides Karzinom
b Nachgewiesen durch einen validierten Test
NCCN und SGO: Internationale Empfehlungen zur Testung bei epithelialem Ovarialkarzinom
Laut aktueller NCCN-Leitlinie wird bei Patientinnen mit epithelialem Ovarial-, Tuben- oder primärem Peritonealkarzinom eine BRCA1/2-Testung (Keimbahn und somatisch) zur Therapieplanung empfohlen. Besteht keine Keimbahnmutation, sollte eine HRD-Testung zur weiteren Einschätzung des Therapieansprechens erfolgen.11
Auch die SGO rät zu einer universellen Keimbahntestung auf BRCA1/2-Mutationen bei allen Patientinnen mit epithelialem Ovarialkarzinom und ergänzt, dass eine alleinige somatische Analyse bis zu 10 % der klinisch relevanten Keimbahnveränderungen übersehen kann. Daher sollte auch bei negativem Tumortest eine Keimbahnanalyse erfolgen.12
Im Primärsetting sind laut NCCN und SGO mindestens die Bestimmung von BRCA1/2-Status (somatisch), Verlust der Heterozygotie (LOH) und HRD (im Falle eines negativen Keimbahnbefunds) empfohlen. Im Rezidivsetting sollte eine erweiterte Diagnostik erfolgen, einschließlich Marker mit tumorspezifischer oder tumoragnostischer Relevanz.11,12

Keine Evidenz für den prädiktiven Nutzen von HRR- Genpanel- Analysen
Die Ergebnisse der Erstlinienstudie PAOLA-1/ENGOT-ov25 zeigten, dass HRR-Genpanel-Analysen über den BRCA1/2-Mutationsnachweis hinaus (z. B. ATM, ATR, BARD1, BLM, BRIP1, CDK12, CHEK2, EMSY, FANCA, FANCI, FANCL, FANCM, MSH2, MSH6, NBN, PALB2, PMS2, RAD51B, RAD51C, RAD51D, RAD54L) keinen prädiktiven Wert für einen progressionsfreien Überlebensvorteil unter der Erhaltungstherapie mit PARP-Inhibitoren zeigten – unabhängig davon, welches Genpanel verwendet wurde.13 Aktuell verfügbare Genpanels zur Analyse von nicht-BRCA-HRR-Mutationen sollten daher bei neu diagnostiziertem fortgeschrittenen Ovarialkarzinom nicht als Ersatz für die Bestimmung des BRCA-Mutationsstatus und der genomischen Instabilität (HRD) betrachtet werden.13
Diese Erkenntnisse stimmen mit aktuellen europäischen Empfehlungen überein: Sowohl ESMO als auch der ESGO-ESMO-ESP-Konsensus sprechen sich gegen eine routinemäßige Tumortestung auf nicht-BRCA-Gene für die prädiktive Einschätzung des Therapieansprechens aus.10,14 Solche Analysen können jedoch im Rahmen klinischer Studien sinnvoll sein.10
Abkürzungen:
ATM: Ataxia Telangiectasis Mutated (Gen); ATR: ATR Checkpoint Kinase (Gen); BARD1: BRCA1 Associated Ring Domain 1 (Gen); BLM: BLM RecQ Like Helicase (Gen);BRCA1: Breast Cancer Associated Gene 1; BRCA2: Breast Cancer Associated Gene 2; BRIP1: BRCA1-Interacting Protein 1; CDK12: Cyclin-abhängige Kinase 12 (Gen); CHEK2: Checkpoint Kinase 2 (Gen); DNA: Desoxyribonukleinsäure; EMSY: EMSY Transcriptional Repressor, BRCA2 Interacting (Gen); ESGO: European Society of Gynaecologic Oncology; ESMO: European Society for Medical Oncology; ESP: European Society of Pathology; FANCA: Fanconi Anemia Complementation Group A (Gen); FANCI: Fanconi Anemia Complementation Group I (Gen); FANCM: Fanconi Anemia Complementation Group M (Gen); FANCL: Fanconi Anemia Complementation Group L (Gen); FIGO: International Federation of Gynecology and Obstetrics; gBRCA1/2m: BRCA1/2‑Keimbahnmutation; GIS: genomischer Instabilitätsscore; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HRD: Homologe Rekombinationsdefizienz; HRR: Homologe Rekombinationsreparatur; IHC: Immunohistochemie; LOH: Verlust der Heterozygotie; LST: large‑scale state transitions; MMR: DNA‑Mismatch‑Reparatur; MSH2: Mutator S Homolog 2 (Gen); MSH6: Mutator S Homolog 6 (Gen); MSI: Mikrosatelliteninstabilität; NBN: Nibrin (Gen); NCCN: National Comprehensive Cancer Network; PALB2: Partner and Localizer of BRCA2 (Gen); PARP: Poly(ADP-ribose)-Polymerase; RAD51B: RAD51 Paralog B (Gen); RAD51C: RAD51 Paralog C (Gen); RAD51D: RAD51 Paralog D (Gen); RAD54L: RAD54 Like (Gen); sBRCA1/2m: somatische BRCA1/2‑Mutation; SGO: Society of Gynecologic Oncology; TAI: telomerisches allelisches Ungleichgewicht; tBRCA1/2m: BRCA1/2‑Mutation im Tumor
- González-Martín A, et al. Ann Oncol 2023;34(10):833–48.
- Ray-Coquard I, et al. N Engl J Med 2019;381(25):2416–28.
- Hauke J, et al. J Med Genet 2019;56(9):574–80.
- Harter P, et al. PLoS One 2017;12(10):e0186043.
- S3-Leitlinie Diagnostik, Therapie und Nachsorge maligner Ovarialtumoren. Version 6.0, Januar 2024. Verfügbar unter https://register.awmf.org/assets/guidelines/032-035OLl_S3_Ovarialkarzinom_2024-10.pdf. Letzter Zugriff: Januar 2026.
- S3-Leitlinie Prostatakarzinom. Version 8.0, Juli 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/leitlinien/prostatakarzinom/. Letzter Zugriff: Januar 2026.
- S3-Leitlinie Exokrines Pankreaskarzinom. Version 3.1, September 2024. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Pankreaskarzinom/Version_3/LL_Pankreaskarzinom_Langversion_3.1.pdf. Letzter Zugriff: Januar 2026.
- S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Konsultationsfassung Version 5.02, Mai 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/LL_Mammakarzinom_Langversion_5.02_Konsultationsfassung.pdf. Letzter Zugriff: Januar 2026.
- Vergote I, et al. Ann Oncol 2022;33(3):276–87.
- Ledermann JA, et al. Ann Oncol 2024;35(3):248–66.
- NCCN Clinical Practice Guidelines in Oncology. Ovarian Cancer Including Fallopian Tube Cancer and Primary Peritoneal Cancer. Version 2.2025. Verfügbar unter https://www.nccn.org/professionals/physician_gls/pdf/ovarian.pdf. Letzter Zugriff: Januar 2026.
- Gressel GM, et al. Gynecol Oncol 2024;181:170–78.
- Pujade-Lauraine E, et al. JCO Precis Oncol 2023;7:e2200258.
- Miller RE, et al. Ann Oncol 2020;31(12):1606–22.