HER2-Alterationen bei Tumoren
HER2-Alterationen treten bei etwa 5,5 % aller soliden Tumoren auf – mit erhöhter Prävalenz bei folgenden Tumorentitäten:1
- Mammakarzinom
- Nicht-kleinzelliges Lungenkarzinom (NSCLC)
- Kolorektales Karzinom
- Harnblasenkarzinom
- Magenkarzinom
- Karzinom des gastroösophagealen Übergangs
- Ösophaguskarzinom
- Zervixkarzinom
Die Veränderungen im HER2-Protein und/oder im HER2 (ERBB2) Gen führen zu einer Hyperaktivierung des Rezeptors. Diese aktivieren onkogene Signalwege, was Tumorprogression und Metastasierung durch gesteigerte Zellproliferation und verlängerte Überlebenssignale fördert.2 Beispielsweise können Mammakarzinome bis zu 50 Kopien des HER2 (ERBB2) Gens aufweisen und eine 40- bis 100-fach erhöhte HER2-Proteinexpression zeigen.3
HER2-Alterationstypen
Drei Hauptmechanismen der HER2-Aktivierung sind beschrieben:4,5

Überexpression
des HER2-Proteins

Amplifikation
des HER2 (ERBB2) Gens

Aktivierende Mutationen
im HER2 (ERBB2) Gen
Diese Alterationen sind molekular voneinander unabhängig und zeigen unterschiedliche biologische Eigenschaften sowie prädiktive und prognostische Relevanz.2
Je nach Alterationstyp kommen unterschiedliche diagnostische Verfahren zum Einsatz, darunter:
Immunhistochemie (IHC)
In-situ-Hybridisierung (ISH)
Next-Generation-Sequencing (NGS)

DIAGNOSTIKInformationen zur HER2- Diagnostik allgemein.
HER2-Überexpression
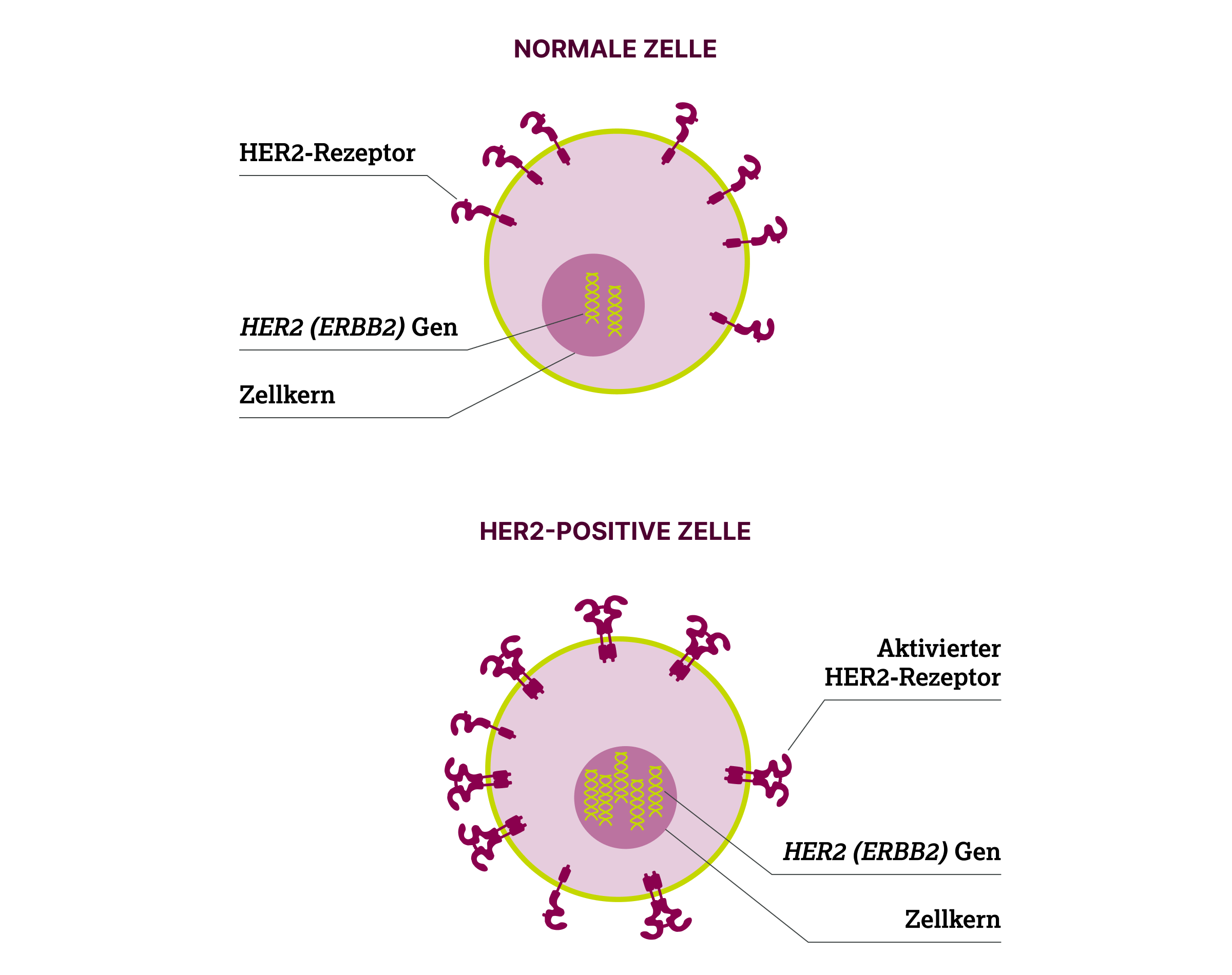
HER2 wird unter physiologischen Bedingungen in geringer Menge auf der Zellmembran von Epithelzellen in verschiedenen Organen exprimiert – darunter Brust, Haut, Magen-Darm-Trakt, Atemwege, Urogenitaltrakt und Harnwege.6–8 Normale Zellen tragen entsprechend nur eine begrenzte Anzahl an HER2-Rezeptoren auf ihrer Oberfläche.9
Beim Mammakarzinom beruht eine HER2-Überexpression in 90–95 % der Fälle auf einer Amplifikation des HER2-Gens;5,6 folgender Vergleich verdeutlicht das Ausmaß: In normalen Brustepithelzellen exprimieren zwei HER2 (ERBB2) Genkopien ca. 20.000 HER2-Rezeptoren pro Zelle.6,9
In HER2-positiven Tumorzellen können 25–50 Genkopien vorliegen, was zu einer 40- bis 100-fachen Steigerung der Genexpression und einer Rezeptordichte von bis zu zwei Millionen HER2-Rezeptoren pro Zelle führen kann.6,9
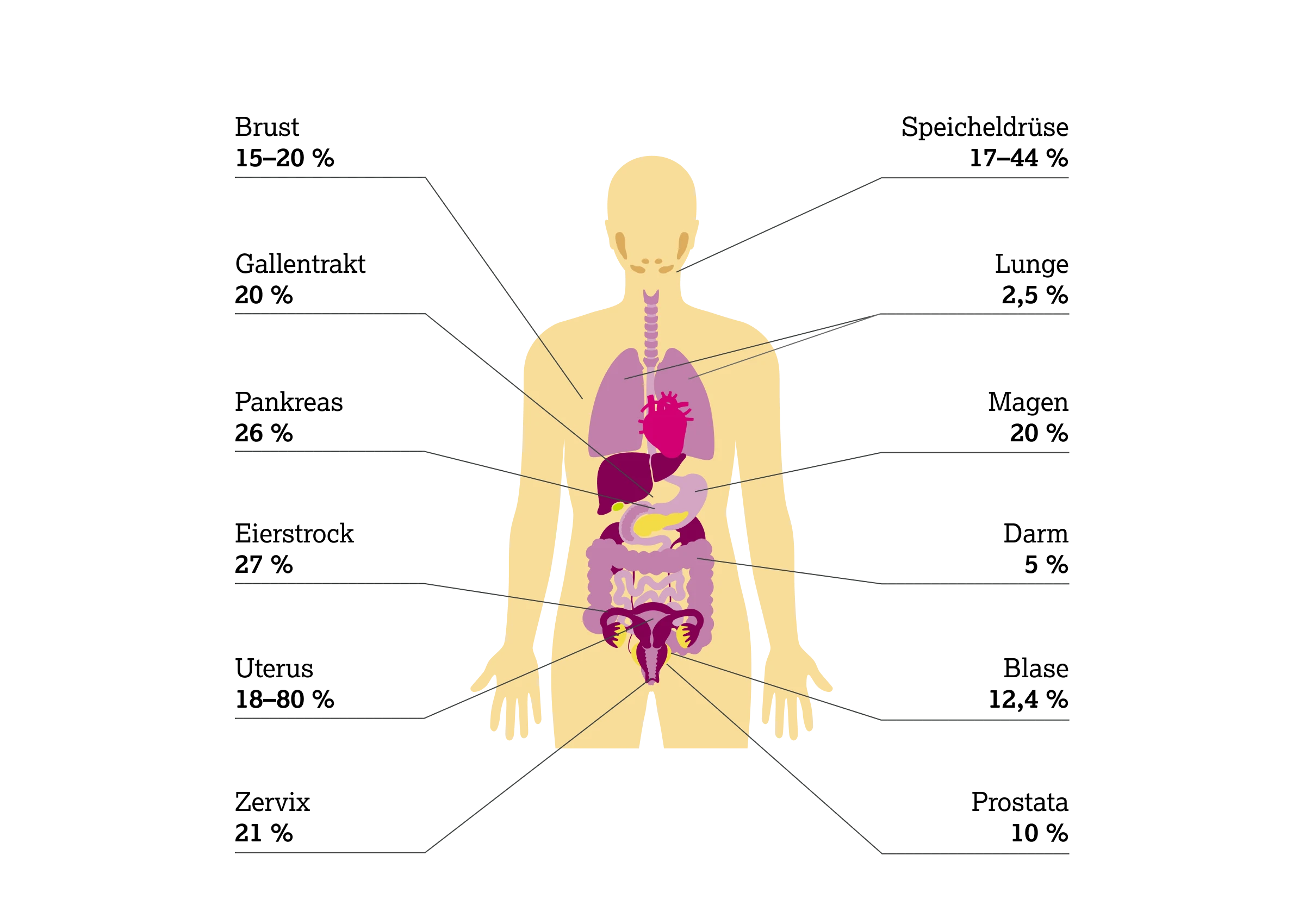
* Die Angaben zur Prävalenz von HER2-Alterationen basieren auf einzelnen Studien und können in der Literatur stark variieren. Die hier genannten Prozentwerte entstammen einer spezifischen Quelle; andere Untersuchungen berichten teilweise abweichende Häufigkeiten.
Die hohe Rezeptordichte führt zur konstitutiven Aktivierung HER2-abhängiger Signalwege, was unkontrolliertes Zellwachstum, Tumorprogression und Metastasierung begünstigt.6,11,12
Neben der Gen-Amplifikation können auch andere Mechanismen zur HER2-Überexpression beitragen, darunter:5,6,13
DNA-Hypomethylierung in der Promotorregion
Mutationen im Tumorsuppressor-Gen TP53
posttranskriptionelle und epigenetische Veränderungen
HER2-Amplifikation
Die HER2 (ERBB2) Amplifikation beschreibt die genomische Vervielfältigung des Gens, was typischerweise zu einer HER2-Proteinüberexpression führt, damit die Bildung von HER2-Homo- oder -Heterodimeren induziert, nachgeschaltete Signalwege aktiviert und so die Tumorproliferation und Metastasierung fördert.6
Beim Mammakarzinom stellt die HER2 (ERBB2) Amplifikation ein frühes und häufiges Ereignis in der Tumorentstehung dar. Sie tritt in etwa 50 % der duktalen Carcinoma in situ (DCIS) auf. Im Vergleich dazu zeigen nur rund 20 % der invasiven Mammakarzinome eine HER2 (ERBB2) Amplifikation – ein Hinweis darauf, dass viele DCIS mit HER2 (ERBB2) Amplifikation nicht ins invasive Stadium übergehen.6
HER2 (ERBB2) amplifizierte Mammakarzinome weisen distinkte biologische Eigenschaften auf:14
- Erhöhte Ansprechrate auf bestimmte zytotoxische Chemotherapeutika
- Resistenz gegenüber hormonbasierten Therapien
- Erhöhte Inzidenz von Hirnmetastasen
Eine HER2 (ERBB2) Amplifikation wird u. a. auch in Subgruppen von Magen-, Ösophagus- und Endometriumkarzinomen beobachtet, die ebenfalls mit einem schlechteren Krankheitsverlauf assoziiert sind.14
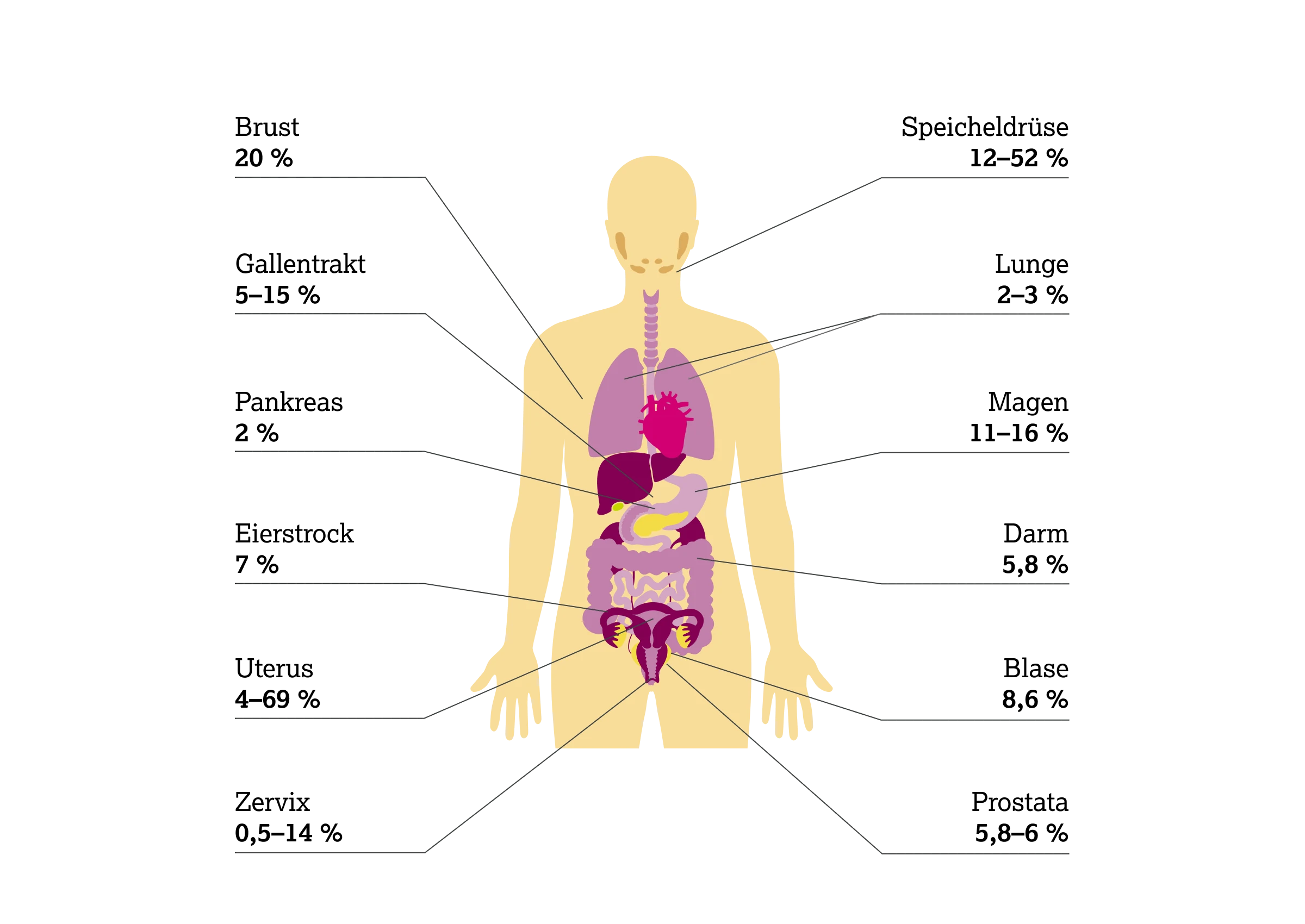
* Die Angaben zur Prävalenz von HER2-(ERBB2) Amplifikationen basieren auf einzelnen Studien und können in der Literatur stark variieren. Die hier genannten Prozentwerte entstammen einer spezifischen Quelle; andere Untersuchungen berichten teilweise abweichende Häufigkeiten.

DIAGNOSTIKInformationen zur HER2-Diagnostik.
HER2 (ERBB2) Mutationen
Im Gegensatz zur HER2 (ERBB2) Amplifikation führen aktivierende Mutationen im HER2 (ERBB2) Gen zu strukturellen Veränderungen des HER2-Proteins. Diese Veränderungen bewirken eine konstitutive, ligandenunabhängige Aktivierung der nachgeschalteten Signalwege – ohne dass eine Homo- oder Heterodimerisierung des Rezeptors erforderlich ist.5
Verteilung und Lokalisation von HER2 (ERBB2) Mutationen
Mutationen können in allen Exons des HER2 (ERBB2) Gens auftreten, mit deutlicher Heterogenität sowohl zwischen verschiedenen Tumorentitäten als auch innerhalb derselben Tumorart.15 Betroffen sind v. a. funktionell relevante Bereiche des Proteins:15
- Extrazelluläre Domäne
- Transmembranregion
- Intrazelluäre oder Tyrosinkinase-Domäne

Eine umfassende Analyse von 25 Krebsarten zeigte:16
- 46 % der HER2 (ERBB2) Mutationen lagen in der Tyrosinkinase-Domäne, insbesondere in
Exon 20: 20 %
Exon 19: 11 %
Exon 21: 9 %
- 37 % der Mutationen betrafen die extrazelluläre Domäne.16
Klinische Relevanz bei soliden Tumoren
Aktivierende HER2 (ERBB2) Mutationen wurden erstmals beim nicht-kleinzelligen Lungenkarzinom (NSCLC) beschrieben15 – häufig als In-Frame-Insertionen in Exon 20 (Tyrosinkinase-Domäne).5,16,17 Typischerweise schließen sich diese Mutationen mit anderen onkogenen Treibermutationen gegenseitig aus und treten selten gemeinsam mit HER2 (ERBB2) Amplifikationen auf.5,17
Inzwischen wurden HER2 (ERBB2) Mutationen bei einer Vielzahl solider Tumorarten identifiziert, am häufigsten beim Urothelkarzinom.4
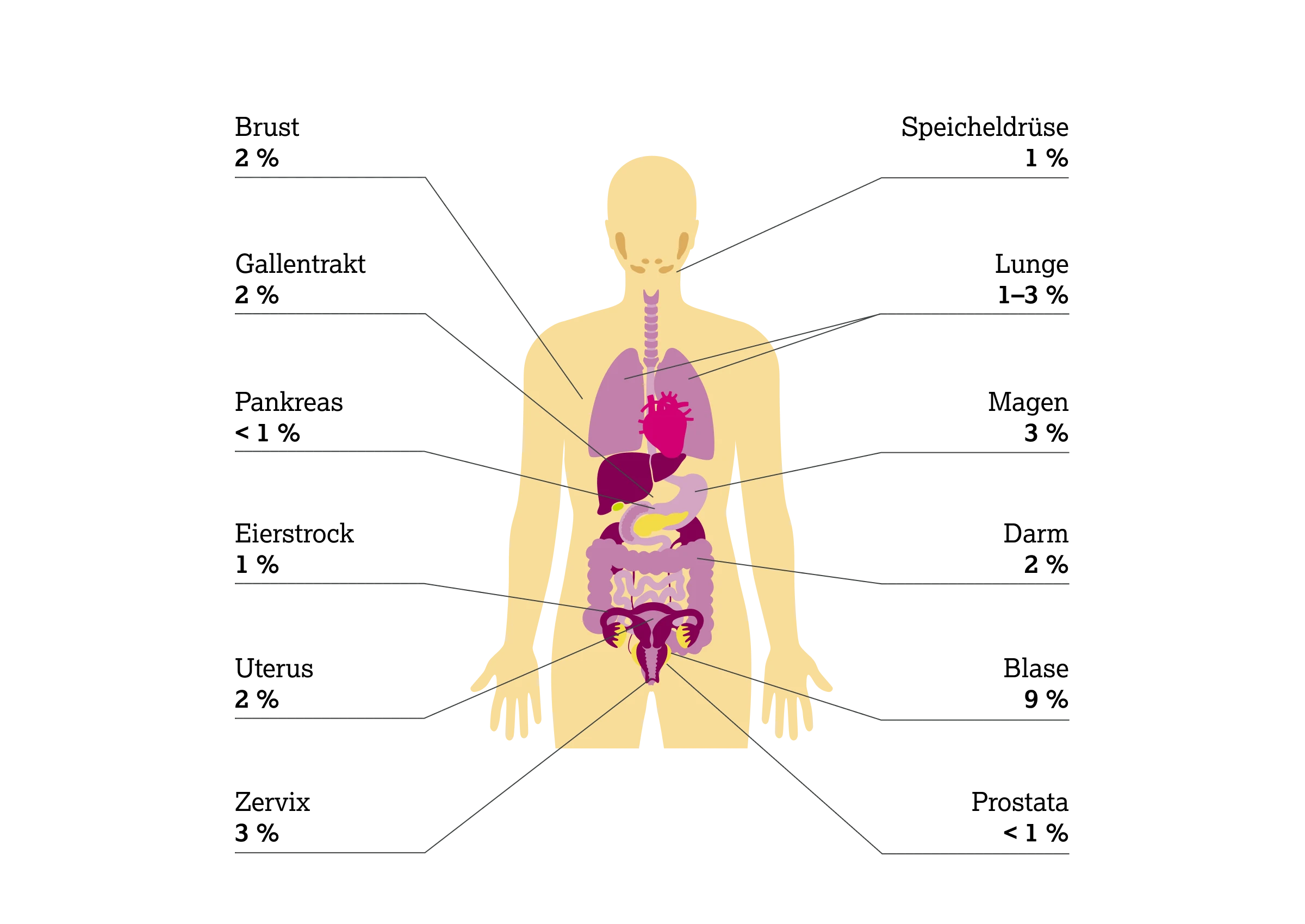
* Die Angaben zur Prävalenz von HER2 (ERBB2) Mutationen basieren auf einzelnen Studien und können in der Literatur stark variieren. Die hier genannten Prozentwerte entstammen einer spezifischen Quelle; andere Untersuchungen berichten teilweise abweichende Häufigkeiten.
Diagnostik und therapeutische Bedeutung
Im Unterschied zur HER2-Überexpression und HER2 (ERBB2) Amplifikation, die insbesondere beim Mammakarzinom eine etablierte, therapeutisch relevante Zielstruktur darstellt, war die Testung auf HER2 (ERBB2) Mutationen bislang nicht Teil der routinemäßigen molekularpathologischen Diagnostik. Sie erfolgt derzeit überwiegend im Rahmen erweiterter molekularer Analysen, vor allem bei fortgeschrittenen oder therapierefraktären Tumoren.18–20
TUMORERKRANKUNGENInformationen zu HER2 beim Mammakarzinom.
Die klinische Relevanz von HER2 (ERBB2) Mutationen nimmt jedoch stetig zu – insbesondere beim nicht-kleinzelligen Lungenkarzinom (NSCLC): Hier ist die Testung mittlerweile Bestandteil der molekularen Diagnostik gemäß der aktuellen S3-Leitlinie, da für Patient:innen mit aktivierenden HER2 (ERBB2) Mutationen zielgerichtete Therapieoptionen zur Verfügung stehen.21
TUMORERKRANKUNGENInformationen zu HER2 beim Lungenkarzinom.
Auch bei anderen Tumorentitäten, etwa dem kolorektalen Karzinom, dem Gallengangskarzinom oder bestimmten gynäkologischen Tumoren, werden HER2 (ERBB2) Mutationen zunehmend im Rahmen erweiterter Paneldiagnostik detektiert und in klinischen Studien therapeutisch adressiert.22–24 Eine generelle Integration in die Standarddiagnostik steht hier jedoch noch aus.
Angesichts der sich weiterentwickelnden Studienlage und zunehmenden Zulassungen HER2-gerichteter Substanzen bei mutierten Tumoren ist mittelfristig mit einer weiteren Etablierung der HER2 (ERBB2) Mutationsanalyse in der molekularen Diagnostik verschiedener Tumorentitäten zu rechnen.
Abkürzungen
DCIS: duktales Carcinoma in situ; ERBB: v-erb-b2 erythroblastic leukemia viral oncogene homolog 2 (Synonym für HER2); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; GFR: Wachstumsfaktor-Rezeptor; IHC: Immunohistochemie; ISH: In-situ-Hybridisierung; NGS: Next-Generation-Sequencing; NSCLC: nicht-kleinzelliges Lungenkarzinom; TP53: Tumorsuppressor-Gen p53
- Danesi R, et al. ESMO Open 2021;6(2):100040.
- Riudavets M, et al. ESMO Open 2021;6(5):100260.
- Budi HS, et al. Stem Cell Res Ther 2022;13(1):40.
- Oh D-Y, et al. Nat Rev Clin Oncol 2020;17(1):33–48.
- Jebbink M, et al. Cancer Treat Rev 2020;86:101996.
- Albagoush SA, et al. (2025). Tissue Evaluation for HER2 Tumor Marker. Verfügbar unter ncbi.nlm.nih.gov/books/NBK537134/. Letzter Zugriff: Juli 2025.
- Rinnerthaler G, et al. Int J Mol Sci 2019;20(5):1115.
- Plum PS, et al. BMC Cancer 2019;19(1):38.
- Furrer D, et al., 1st Aufl. In: Lemamy, G-J (Hrsg.) 2018 – Cancer Prognosis, Herausgeber. London (UK): IntechOpen; 2018, p. 11–32.
- McNamara B, et al. Molecules 2023;28(21):7389.
- Pillai RN, et al. Cancer 2017;123(21):4099–105.
- Gutierrez C, et al. Arch Pathol Lab Med 2011;135(1):55–62.
- Román-Rosales AA, et al. BMC Cancer 2018;18(1):709.
- Moasser MM. Oncogene 2007;26(45):6469–87.
- Connell CM, et al. ESMO Open 2017;2(5):e000279.
- Robichaux JP, et al. Cancer Cell 2019;36(4):444-457.e7.
- Baraibar I, et al. Crit Rev Oncol Hematol 2020;148:102906.
- Varga Z, et al. Kompass Onkol 2024;11(2):63–75.
- Rieke D, et al; 2024. Verfügbar unter onkopedia.com/de/onkopedia/guidelines/praezisionsonkologie/@@guideline/html/index.html. Letzter Zugriff: Juli 2025.
- Wild PJ, et al. Pathologie (Heidelb) 2022;43(5):388–98.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: Juli 2025.
- Zhu K, et al. Biomark Res 2024;12(1):16.
- Ivanova M, et al. Life (Basel) 2022;12(9):1403.
- Manrai PA, et al. Int J Gynecol Pathol 2025;44(2):144–54.


