MMR- & MSI-Diagnostik beim Endometriumkarzinom
Mutationen in den DNA‑Mismatch‑Reparatur (MMR)‑Genen führen zum Expressionsverlust der entsprechenden Proteine, wodurch eine defiziente Mismatch‑Reparatur (dMMR) immunhistochemisch am Tumorgewebe nachgewiesen werden kann. Wird kein Expressionsverlust nachgewiesen, spricht man von einer Mismatch-Reparatur-Profizienz (pMMR). Im Gegensatz dazu beruht der Nachweis einer Mikrosatelliteninstabilität (MSI) auf der Detektion von Längenveränderungen repetitiver DNA‑Sequenzen, weshalb technisch keine direkte Aussage über zugrunde liegende Gendefekte möglich ist.1 Die MSI‑Analyse erfolgt mittels Polymerase‑Kettenreaktion (PCR) oder alternativ Next‑Generation‑Sequencing (NGS) am Tumorgewebe im Vergleich zu Nicht‑Tumorgewebe.1 Beim Endometriumkarzinom sollte die MSI‑Analyse ausschließlich bei unklaren Befunden einer immunhistochemischen dMMR/pMMR‑Analyse nachgeschaltet und nicht routinemäßig erfolgen.2

Informationen zur MMR und MSI.
Technischer Nachweis von dMMR und pMMR mittels Immunohistochemie
Die Immunohistochemie (IHC) ist eine etablierte, kosteneffiziente Methode zum Nachweis einer intakten (pMMR) oder defizienten (dMMR) Mismatch‑Reparatur mit Genmutationen in MSH2, MLH1, MSH6 und/oder PMS2. Da Zellen mit dMMR oft auch eine MSI aufweisen, gilt der Nachweis einer dMMR gleichzeitig als indirekter Hinweis auf eine MSI.3
Trotz hoher diagnostischer Konkordanz4 sind dMMR und MSI biologisch nicht identisch und werden durch unterschiedliche Methoden nachgewiesen.
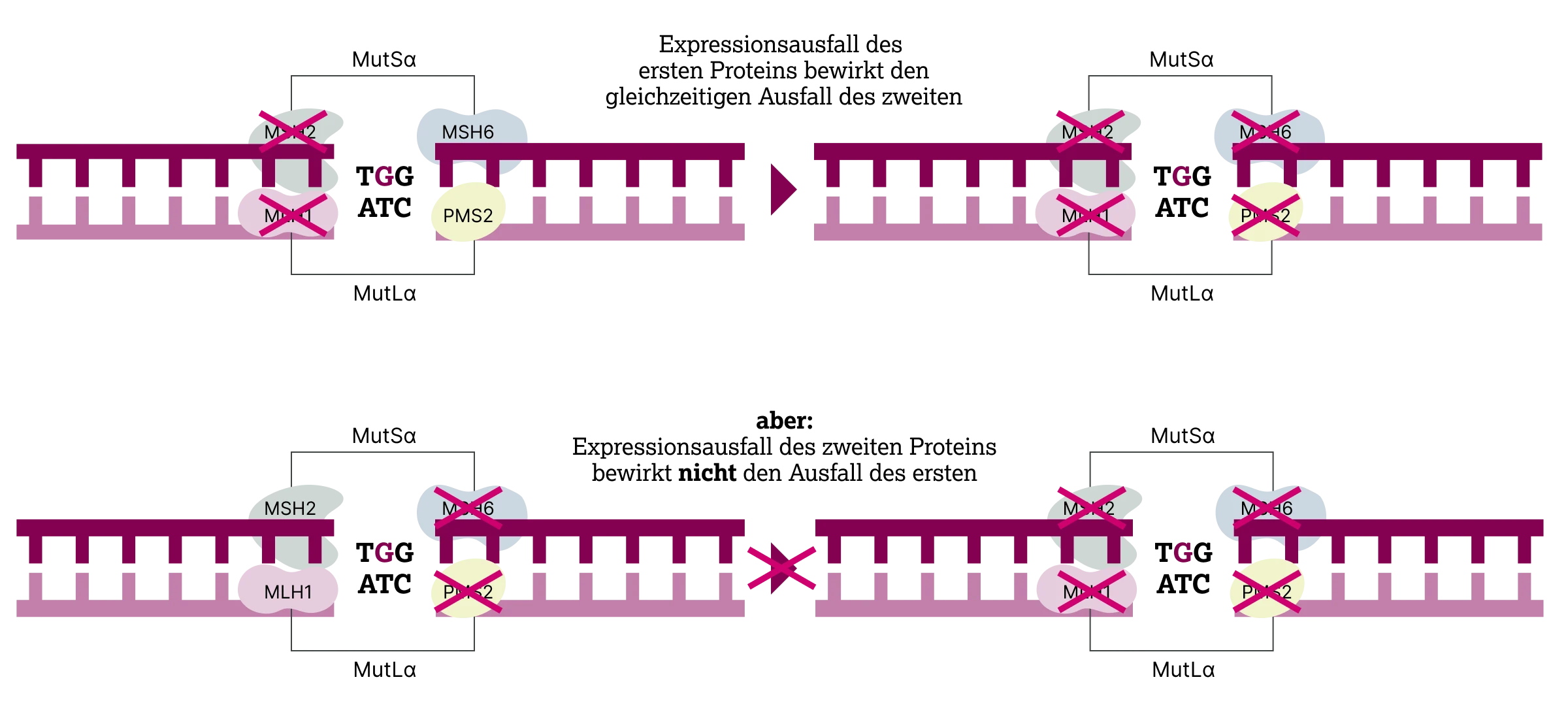
Die beiden Proteine MLH1 und MSH2 sind obligatorische Partner für die Bildung der MMR‑Heterodimere MutLα bzw. MutSα. Der Expressionsverlust von MLH1 oder MSH2 bewirkt automatisch auch den Ausfall des jeweiligen Partners im Heterodimer (PMS2 bzw. MSH6) und damit eine Defizienz des gesamten DNA‑Mismatch‑Reparatursystems.
Mutationen in MLH1 bzw. MSH2 resultieren daher in einem Doppelausfall (MLH1 und PMS2 bzw. MSH2 und MSH6) auf Proteinebene in der IHC. Mutationen in PMS2 oder MSH6 resultieren hingegen nicht zwingend in einem Expressionsverlust von MLH1 bzw. MSH2, da die Funktion sekundärer Proteine durch andere Proteine kompensiert werden kann.3
Aus diesem Grund sollte die initiale MMR‑Analyse bei einem 2‑Marker‑IHC‑Panel mit PMS2‑ bzw. MSH6‑Antikörpern erfolgen – nur so können alle Fälle mit entweder PMS2‑ oder MLH1‑Alterationen bzw. MSH6‑ oder MSH2‑Alterationen nachgewiesen werden.3
- Bei Expressionsausfall von PMS2 bzw. MSH6 sollte zusätzlich auf MLH1 bzw. MSH2 getestet werden.3
- Bei unklaren Befunden mit nicht eindeutigem Expressionsausfall in < 90 % der Tumorzellen oder bei fehlender Färbung im Normalgewebe (interne Kontrolle) sollte zusätzlich eine MSI‑Analyse durchgeführt werden.3
- Bei alleinigem Ausfall von MLH1 sollte ein molekularpathologischer Ausschluss einer MLH1‑Promotormethylierung im Kontext des Lynch‑Syndroms erfolgen.3
Für die IHC wird eine Tissue‑Microarray Tumorprobe (0,6 mm Durchmesser) benötigt. Nach hitzeinduzierter Antigendemaskierung erfolgt die Färbung gemäß Herstellerprotokollen unter Verwendung geeigneter Positiv- und Negativkontrollen. Für MSH2, MLH1, MSH6 und PMS2 sollte jeweils die Zellkernfärbung als Positivkontrolle verwendet werden. Bei abweichenden, mehrdeutigen oder nicht interpretierbaren Ergebnissen sollte die Färbung wiederholt werden.5-7
Die IHC‑Diagnostik birgt methodische Herausforderungen wie Variabilitäten in der Gewebefixierung oder heterogene Färbemuster. Auch genetische und molekulare Faktoren können die Interpretation erschweren. Dazu gehören beispielsweise Mutationen, die zu funktionellen, aber immunhistochemisch nicht nachweisbaren Proteinveränderungen führen oder die Proteinstabilität bzw. zelluläre Lokalisierung beeinflussen (z. B. Trunkierungen).2
Technischer Nachweis von MSI mittels Polymerase-Kettenreaktion
Für die MSI‑Analyse sind mehrere NGS-Verfahren verfügbar und weitere befinden sich in der Entwicklungsphase. Der derzeitige diagnostische Standard für MSI bleibt jedoch die PCR.2
Beim Nachweis mittels PCR wird die MSI als Längenabweichung in einfach repetitiven DNA‑Sequenzen gegenüber dem Normalgewebe mit oder ohne Bestimmung der Fragmentlängen untersucht. Wenn die PCR-Produkte aus Tumor- und Normalgewebe exakt gleich groß sind, liegt keine MSI vor.
Für den Nachweis einer MSI bietet NGS im Vergleich zur PCR eine Sensitivität von > 95 % und eine Spezifität von 99 %. Allerdings sind die Auswahl und die Anzahl der untersuchten Mikrosatellitenloci sehr unterschiedlich, denn es stehen wenige einzelne Marker bis zu mehreren Tausend Loci zur Verfügung. Außerdem können die Schwellenwerte der jeweiligen MSI‑Scores tumorentitätenspezifisch sein und müssen entsprechend angepasst und validiert werden.3
Bei der MSI‑Analyse mittels NGS sind zusätzliche Herausforderungen zu bedenken: Beim Funktionsverlust der vier zentralen MMR‑Gene können unterschiedliche Sequenztypen betroffen sein. Bei MSH6 sind das vor allem Mononukleotid- und bei MSH1 oder PMS2 meist Dinukleotid-Sequenzen.3
Mono- und Dinukleotidmarker sollten außerdem immer in Kombination verwendet werden. Bei Tumoren mit dMMR‑/MSI kann es sekundär (ganz selten auch primär als Keimbahnmutation) zum Ausfall von MSH3 kommen und damit zur Instabilität an Tri- und
Tetranukleotid-, seltener Dinukleotid-Sequenzen („elevated microsatellite alterations at selected tetranucleotide repeats“, EMAST). Dieser Fall kann nicht über Mononukleotid-NGS-Panels erfasst werden.3
Qualitätssicherung in der MMR- und MSI-Diagnostik
In der S3‑Leitlinie wird die Bedeutung einer genauen molekularen Klassifikation zur Optimierung der Therapie hervorgehoben: Für die MMR‑Analyse eignet sich primär Tumorgewebe aus dem Abradat oder einer Endometriumbiopsie, wobei die Verwendung des Abradats bevorzugt wird.2 Die Untersuchung sollte in spezialisierten Laboren erfolgen, um eine präzise und zuverlässige Diagnostik zu gewährleisten.
Für belastbare und vergleichbare Testergebnisse ist das Einhalten unterschiedlicher Qualitätsstandards von zentraler Bedeutung.
Ein wichtiges Instrument für die interne und externe Qualitätssicherung diagnostischer Verfahren sind Ringversuche. Sie haben das Ziel, die technischen Abläufe empirisch zu validieren und zu zertifizieren. Bei einem Ringversuch werden den teilnehmenden Laboren validierte Gewebeproben zur Verfügung gestellt und die Ergebnisse der Analyse anschließend statistisch ausgewertet. Beim erfolgreichen Abschluss eines Ringversuchs erhält das teilnehmende Labor ein Zertifikat, das sein Testergebnis dokumentiert und die Analysequalität bestätigt.8
In Deutschland werden Ringversuche zur MMR- bzw. MSI‑Analyse durch die Qualitätssicherungs-Initiative Pathologie GmbH (QuIP) angeboten. Entsprechend aktuellen Zulassungen stehen dafür sowohl Proben von Endometriumkarzinomen als auch Kolonkarzinomen zur Verfügung. Mit den Ringversuchen konnte gezeigt werden, dass die Antikörper verschiedener Hersteller für eine IHC-basierte Detektion der vier Reparaturproteine MLH1, MSH2, MSH6 und PMS2 vergleichbare Ergebnisse liefern können.
Bei der QuIP finden Sie weitere Informationen zur Diagnostik und eine Liste der Institute, die erfolgreich an den Ringversuchen teilgenommen haben.8

Weitere Informationen zu den Ringversuchen der QuIP.
Abkürzungen
dMMR: defiziente Mismatch‑Reparatur; DNA: Desoxyribonukleinsäure; EMAST: elevated microsatellite alterations at selected tetranucleotide repeats; IHC: Immunhistochemie; MLH1: MutL Homolog 1; MMR: DNA‑Mismatch‑Reparatur; MSH1: Mutator S Homolog 1; MSH2: Mutator S Homolog 2; MSH3: Mutator S Homolog 3; MSH6: Mutator S Homolog 6; MSI: Mikrosatelliteninstabilität; MutLα: Mutator L alpha; MutSα: Mutator S alpha; NGS: Next-Generation-Sequencing; PCR: Polymerase‑Kettenreaktion; pMMR: profiziente Mismatch‑Reparatur; PMS2: Postmeiotic Segregation Increased 2; QulP: Qualitätssicherungs‑Initiative Pathologie GmbH
- Engel C, et al. Int J Cancer 2006;118(1):115–22.
- S3-Leitlinie Endometriumkarzinom; Version 3.0; Juni 2024. Verfügbar unter: https://www.leitlinienprogramm-onkologie.de/leitlinien/endometriumkarzinom. Letzter Zugriff: September 2025.
- Dietmaier W, et al. Pathologe 2019;40(3):313–27.
- Stelloo E, et al. Ann Oncol 2017;28(1):96–102.
- McConechy MK, et al. Gynecol Oncol 2015;137(2):306–10.
- Kommoss S, et al. Ann Oncol 2018;29(5):1180–88 (inkl. Supplement).
- Doghri R, et al. Appl Immunohistochem Mol Morphol 2019;27(9):678–82.
- Qualitätssicherungs-Initiative Pathologie QuIP GmbH; Ringversuche. Verfügbar unter: https://www.quip.eu/de_DE/ringversuche. Letzter Zugriff: September 2025.