PD-L1 Diagnostik allgemein
Der Immuncheckpoint-Rezeptor PD-1 (Programmed Cell Death Protein 1) und sein Ligand PD-L1 (Programmed Death Ligand 1) spielen eine zentrale Rolle in der Tumorimmunologie und sind etablierte Zielstrukturen in der Immuntherapie maligner Erkrankungen.1 Eine hohe PD-L1 Expression wird bei zahlreichen Tumorentitäten beobachtet und ist häufig mit einer ungünstigen Prognose assoziiert.1
Beispielsweise zeigen ca. 50 % der Lungenkarzinome eine PD-L1 Expression von ≥ 1 % der Tumorzellen.2 Beim Magenkarzinom wird dieser Anteil mit über 70 % angegeben3, beim malignen Melanom mit bis zu 77 %.4 Die Prozentangaben zur PD-L1 Expression variieren abhängig vom verwendeten immunhistochemischen Assay, dem gewählten Antikörper und dem Bewertungsalgorithmus (z. B. TPS, CPS, TC- oder IC-Score). Methodische Unterschiede und unterschiedliche Cut-Offs können zu abweichenden Prävalenzdaten führen.5
Seit der ersten Zulassung eines Checkpoint-Inhibitors vor über 10 Jahren wurden in Europa mehrere PD-1 / PD-L1 Antikörper zugelassen – darunter bronchiale, gastrointestinale, urogenitale und kutane Malignome.,6–9 Die Indikation zur Therapie mit diesen Inhibitoren ist häufig an definierte PD-L1 Expressionsniveaus gebunden.
Die immunhistochemische Bestimmung dieses prädiktiven Biomarkers ist daher ein zentraler Bestandteil der pathologischen Diagnostik und essenziell für die therapeutische Entscheidungsfindung.10
Immunhistochemie zur PD-L1 Bestimmung
Der Nachweis des Biomarkers PD-L1 erfolgt in der Regel mittels Immunhistochemie (IHC) an formalinfixiertem, paraffineingebettetem Gewebe (FFPE). Es kommen verschiedene kommerziell verfügbare Antikörperklone und Testkits zum Einsatz, die sich bezüglich Sensitivität, Spezifität und Auswertungsmodalitäten unterscheiden.11
Die meisten der verfügbaren PD-L1 Assays wurden als prädiktive Biomarker für bestimmte ICIs entwickelt, wobei jeweils unterschiedliche IHC-Plattformen, PD-L1 Färbungsmuster und Bewertungssysteme (Algorithmen) untersucht wurden.11
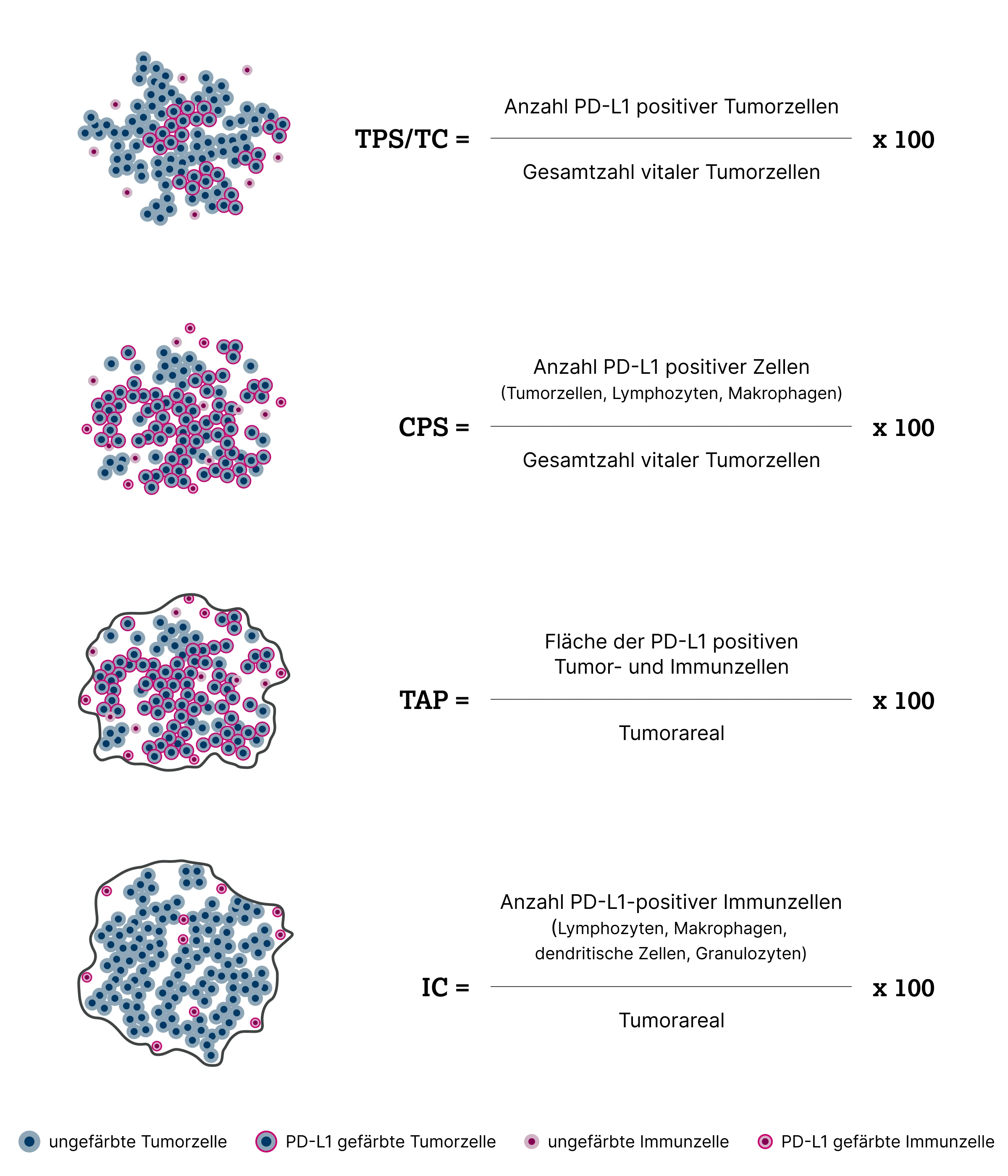
Zur Quantifizierung der PD-L1 Expression werden unterschiedliche Scoring-basierte Bewertungssysteme eingesetzt:11–13
|
Scoring Algorithmus |
Interpretation |
Tumorarten |
|
Tumor Proportion Score oder Tumor Cell Score |
Anteil der PD-L1 positiven Tumorzellen, bezogen auf alle in der Probe vorhandenen vitalen Tumorzellen |
NSCLC |
|
Combined Positive Score |
Anteil der PD-L1 positiven Tumor- und Immunzellen an allen vitalen Tumorzellen |
GEJ, Zervixkarzinom, Urothelkarzinom, Mammakarzinom |
|
Immune Cell Score |
Anteil der Tumorfläche, die von PD-L1 positiven Immunzellen eingenommen wird, bezogen auf die Gesamttumorfläche |
NSCLC, TNBC, Urothelkarzinom |
|
Tumor Area Positivity |
Anteil der Tumorfläche, die von PD-L1 positiven Zellen und tumorassoziierten Immunzellen eingenommen wird, bezogen auf die Gesamttumorfläche |
GEJ, Magenkarzinom, Ösophaguskarzinom |
Derzeit verwendete Scorings für die immunhistochemische Bewertung der PD-L1 Expression in verschiedenen Tumorarten (mod. nach Vranic S et al. 202311, Liu C et al. 202313 und Pai T et al. 202412)
Therapeutische Grenzwerte (Cut-offs) der PD-L1 Expression sind assay- und indikationsspezifisch und liegen in den Zulassungsstudien häufig im Bereich ≥ 1 % bis ≥ 50 % Tumorzell bzw. kombinierten Scores.4,15 Dies unterstreicht die Notwendigkeit standardisierter, sensitiver und reproduzierbarer Testmethoden.
Weitere Verfahren
Zusätzlich zur IHC kommen in der Forschung und in seltenen Spezialfällen weitere Verfahren zum Einsatz, u. a.:
Quantitativer Nachweis von löslichem PD-L1 in Serum oder Plasma. Der Einsatz erfolgt überwiegend im Rahmen wissenschaftlicher Studien und ist derzeit nicht Bestandteil der routinemäßigen Diagnostik.16,17
Bestimmung der PD-L1 Genexpression mittels RT-PCR. Diese Methode hat aktuell nur eine untergeordnete Bedeutung für klinische Therapieentscheidungen.16,17
Für eine valide Anwendung dieser Assays ist ein detailliertes Verständnis ihrer methodischen Grundlagen, Vor- und Nachteile sowie möglicher Fehlerquellen essenziell. Insbesondere sollten Angaben zu verwendeten Antikörperklonen, Testplattformen, Bewertungsalgorithmen und relevanten Begleitmedikationen dokumentiert werden, um die Ergebnisse zur PD-L1 Expression korrekt interpretieren zu können.17

Informationen zu den Studien- und Leitlinienempfehlungen zur PD-L1 Testung.
Abkürzungen
CPS: Combined Positive Score; ECL: Elektrochemilumineszenz Immunoassay; ELISA: Enzyme-linked Immunosorbent Assay; FFPE: formalinfixiert, paraffineingebettet; GEJ: Gastroösophagealer Übergang; IC: Immune Cell; ICI: Immuncheckpoint-Inhibitor; IHC: Immunhistochemie; mRNA: messenger-RNA; NSCLC: nicht-kleinzelliges Lungenkarzinom; PD-1: Programmed cell death-1; PD-L1: Programmed cell death ligand-1; RT-PCR: Reverse-Transkriptase-PCR; TAP: Tumor Area Positivity; TC: Tumor Cell; TNBC: triple-negatives Mammakarzinom; TPS: Tumor Proportion Score
- Hossain A. Int Immunopharmacol 2024;143(Pt 2):113365.
- Dietel M, et al. Lung Cancer 2019;134:174–9.
- Cho Y, et al. J Gastric Cancer 2025;25(1):177–91.
- Patel SP, et al. Mol Cancer Ther 2015;14(4):847–56.
- Udall M, et al. Diagn Pathol 2018;13(1):12.
- Mc Neil V, et al. Cancers (Basel) 2025;17(9):1408.
- Shiravand Y, et al. Curr Oncol 2022;29(5):3044–60.
- Falcone R, et al. Cancers (Basel) 2022;14(4).889.
- Zietse M, et al. Lancet Oncol 2024;25(11):e611-e616.
- Baretton GB, et al. J Cancer Res Clin Oncol 2023;149(17):16231–8.
- Vranic S, et al. Biomol Biomed 2023;23(1):15–25.
- Pai T, et al. J Cancer Immunol 2024;6(2):77–91.
- Liu C, et al. Diagn Pathol 2023;18(1):48.
- Epistola R, et al. Cancer Manag Res 2023;15:265–75.
- Davis AA, et al. J Immunother Cancer 2019;7(1):278.
- Qi C, et al. Clin Exp Med 2024;24(1):162.
- Jeong S, et al. Cancers (Basel) 2021;13(20):5225.