IVDR
Die IVDR im Überblick
Seit dem 26. Mai 2022 ist die EU-Verordnung 2017/746 über In-vitro-Diagnostika (IVDR) in Kraft und ersetzt die bisher geltende EU-Richtlinie 98/79/EG (IVDD). Anders als die IVDD, die in nationales Recht umgesetzt werden musste, in Deutschland über das Medizinproduktegesetz (MPG), gilt die IVDR als Verordnung unmittelbar und einheitlich in allen EU-Mitgliedsstaaten.1,2
Ziel der IVDR ist es, den wissenschaftlichen und technologischen Fortschritt in der Medizin zu berücksichtigen, die klinische Sicherheit von In-vitro-Diagnostika (IVDs) zu erhöhen und gleichzeitig das reibungslose Funktionieren des europäischen Binnenmarkts zu gewährleisten. Für Patholog:innen bedeutet dies insbesondere eine strengere Regulierung sowohl für kommerzielle In-vitro-Diagnostika als auch für (von Laboren) selbst entwickelte Tests (LDTs), die nun systematisch dokumentiert, validiert und überwacht werden müssen.2
Was wird unter IVDR reguliert?
Die IVDR reguliert die Herstellung, das Inverkehrbringen und die Anwendung von IVD innerhalb der Europäischen Union. Sie richtet sich in erster Linie an Hersteller, Händler und Importeure von IVD-Produkten.
Was unter einem In-vitro-Diagnostikum zu verstehen ist, wird im Artikel 2 (2) der IVDR festgelegt:
„In-vitro-Diagnostikum bezeichnet ein Medizinprodukt, das als Reagenz, Reagenzprodukt, Kalibrator, Kontrollmaterial, Kit, Instrument, Apparat, Gerät, Software oder System – einzeln oder in Verbindung miteinander – vom Hersteller zur In-vitro-Untersuchung von Proben aus dem menschlichen Körper, einschließlich Blut- und Gewebespenden, bestimmt ist und ausschließlich oder hauptsächlich dazu dient, Informationen zu einem oder mehreren der folgenden Punkte zu liefern:
a) über physiologische oder pathologische Prozesse oder Zustände,
b) über kongenitale körperliche oder geistige Beeinträchtigungen,
c) über die Prädisposition für einen bestimmten gesundheitlichen Zustand oder eine bestimmte Krankheit,
d) zur Feststellung der Unbedenklichkeit und Verträglichkeit bei den potenziellen Empfängern,
e) über die voraussichtliche Wirkung einer Behandlung oder die voraussichtlichen Reaktionen darauf oder
f) zur Festlegung oder Überwachung therapeutischer Maßnahmen.“1
Mit dem Übergang von der IVDD auf die IVDR wurde der Begriff der In-vitro-Diagnostika präzisiert: Neu ist unter anderem, dass auch Software als IVD gilt, wenn sie für medizinische Zwecke genutzt wird, wie bspw. KI-Software zur Bildanalyse.3 Der erweiterte Anwendungsbereich der IVDR schließt zudem folgende Produkte mit ein:
- prädikative Gentests
- Produkte zur Eigenanwendung (z. B. Schwangerschaftstests)
- patientennahe Tests (z.B. Urinteststreifen)
- therapiebegleitende Diagnostika (Companion Diagnostics)1
Therapiebegleitende Diagnostika werden in der EU-Verordnung für IVD erwähnt und somit regulatorisch erfasst (IVDR Artikel 2 (7)).1 Sie spielen mittlerweile eine große Rolle in der personalisierten Medizin: Das Testergebnis bestimmt maßgeblich, ob ein spezifisches Medikament für die Patientin oder den Patienten geeignet ist oder nicht. In der Onkologie etwa basiert die Auswahl der geeignetsten Therapieoptionen auf dem Ergebnis der Biomarkertestung mit solchen begleitenden Diagnostika, welche z. B. die Proteinexpression oder genetische Alterationen untersuchen.
Mit der IVDR werden europaweit erstmals auch einheitliche Anforderungen zur Herstellung und Verwendung selbst entwickelter IVDs geregelt.3 IVDs, die in Gesundheitseinrichtungen entwickelt und angewendet werden, werden als LDTs (Laboratory Developed Tests) oder Inhouse-IVDs bezeichnet.

Sobald ein Labor beispielsweise ein kommerzielles Testkit für eine Fragestellung außerhalb des vom Hersteller angegebenen Verwendungszweckes einsetzt, wird das modifizierte Verfahren zum LDT und das Labor einem Hersteller gleichgesetzt hinsichtlich der regulatorischen Anforderungen. Grundsätzlich dürfen LDTs nicht im industriellen Maßstab produziert werden.3
Gemäß Artikel 1 gilt die IVDR jedoch nicht für folgende Dinge:
„Produkte für den allgemeinen Laborbedarf oder allein für Forschungszwecke bestimmte Produkte, es sei denn, sie sind aufgrund ihrer Merkmale vom Hersteller speziell für In-vitro Untersuchungen bestimmt“
„Invasive zur Entnahme von Proben bestimmte Produkte oder Produkte, die zum Zweck der Probenahme direkt am menschlichen Körper angewendet werden“
„Invasive zur Entnahme von Proben bestimmte Produkte oder Produkte, die zum Zweck der Probenahme direkt am menschlichen Körper angewendet werden“
„Materialien, die für externe Qualitätsbewertungsprogramme verwendet werden“1
Neue Klassifizierung: 4 risikobasierte IVD-Klassen
Die IVDR teilt die In-vitro-Diagnostika anhand von 7 Klassifizierungsregeln in 4 Risikoklassen ein. Die Einstufung erfolgt gemäß Anhang VIII (Klassifizierungsregeln) auf Basis der Zweckbestimmung und des Risikoprofils des jeweiligen Produkts. Im Sinne der Patientensicherheit gelten folgende Risikoklassen:1
- Individuelles Risiko: gering
- Risiko für die öffentliche Gesundheit: gering
- Folgende Produkte fallen in diese Klasse:
- „Erzeugnisse für den allgemeinen Laborbedarf, Zubehör ohne kritische Merkmale, Pufferlösungen, Waschlösungen sowie allgemeine Nährmedien und histologische Färbungen, die vom Hersteller dafür vorgesehen sind, die Produkte für In-vitro-Diagnoseverfahren im Zusammenhang mit einer spezifischen Untersuchung einsetzbar zu machen“
- „Instrumente, die vom Hersteller speziell für die Verwendung bei In-vitro-Diagnoseverfahren vorgesehen sind“
- „Probenbehältnisse“
- Individuelles Risiko: mittel
- Risiko für die individuelle Gesundheit: gering
- Folgende Produkte fallen in diese Klasse:
- „Produkte zur Feststellung einer Schwangerschaft, zur Fertilitätsuntersuchung und zur Bestimmung des Cholesterinspiegels und Produkte zum Nachweis von Glukose, Erythrozyten, Leukozyten und Bakterien im Urin“
- „Kontrollgeräte ohne einen zugewiesenen quantitativen oder qualitativen Wert“
- Individuelles Risiko: hoch
- Risiko für die individuelle Gesundheit: mittel
- Folgende Produkte fallen in diese Klasse:
- „Produkte, die zur Blutgruppenbestimmung oder Gewebetypisierung verwendet werden, um die Immunkompatibilität von für die Transfusion, Transplantation oder Zellgabe bestimmtem Blut, Blutbestandteilen, Zellen, Geweben oder Organen festzustellen, werden der Klasse C zugeordnet, es sei denn, sie werden zur Bestimmung eines der folgenden Marker eingesetzt:
AB Null-System [A (ABO1), B (ABO2), AB (ABO3)];
Rhesus-System [RH1 (D), RHW1, RH2 (C), RH3 (E), RH4 (c), RH5 (e)];
Kell-System [Kel1 (K)];\
Kidd-System [JK1 (Jka), JK2 (Jkb)];
Duffy-System [FY1 (Fya), FY2 (Fyb)];
In diesem Fall werden sie der Klasse D zugeordnet.“
- „Produkte, die zur Blutgruppenbestimmung oder Gewebetypisierung verwendet werden, um die Immunkompatibilität von für die Transfusion, Transplantation oder Zellgabe bestimmtem Blut, Blutbestandteilen, Zellen, Geweben oder Organen festzustellen, werden der Klasse C zugeordnet, es sei denn, sie werden zur Bestimmung eines der folgenden Marker eingesetzt:
-
- „Produkte zur Eigenanwendung“
- Individuelles Risiko: hoch
- Risiko für die individuelle Gesundheit: hoch
- Folgende Produkte fallen in diese Klasse:
- Nachweis des Vorhandenseins von oder der Exposition gegenüber übertragbaren Erregern im Blut, Blutbestandteilen, Zellen, Geweben oder Organen oder in einem ihrer Derivate, um ihre Eignung für die Transfusion, Transplantation oder Zellgabe zu bewerten;
- Nachweis des Vorhandenseins von oder der Exposition gegenüber übertragbaren Erregern, die eine lebensbedrohende Krankheit mit einem hohen oder mutmaßlich hohen Verbreitungsrisiko verursachen;
- Bestimmung des Infektionsgrads einer lebensbedrohlichen Krankheit, dessen Überwachung im Rahmen des Patientenmanagements von entscheidender Bedeutung ist.“
Die Risikoklasse entscheidet das Konformitätsverfahren: Mit steigender Risikoklasse steigen die Anforderungen an die Konformitätsbewertung für die Hersteller von CE-IVD.4,5
Die Konformitätsbewertung ist essenziell für die Markteinführung
Im Sinne der Patientensicherheit müssen die IVD-Hersteller in einem Konformitätsbewertungsverfahren nachweisen, dass ihre Produkte aller Risikoklassen den Sicherheits- und Leistungsanforderungen der IVDR (Anhang I) entsprechen. Mit der IVDR erfordern Produkte ab Risikoklasse B in diesem Prozess die Einbeziehung einer unabhängigen Zertifizierungsstelle, der Benannten Stelle.1 Diese erstellt für konforme Produkte ein CE-Zertifikat und am Ende des Prozesses steht die Konformitätserklärung des Herstellers als Voraussetzung für das Inverkehrbringen des Produktes auf den EU-Markt. Für LDTs, die ausschließlich innerhalb von in der Europäischen Union ansässigen Gesundheitseinrichtungen hergestellt und verwendet werden, entfällt die Einbeziehung einer Benannten Stelle, insofern die Voraussetzungen nach Artikel 5 (Inverkehrbringen und Inbetriebnahme) der Verordnung erfüllt sind.1
Tipps für eine erfolgreiche IVDR-Umsetzung
Die IVDR verpflichtet diagnostische Labore in der EU, einschließlich pathologischer Einrichtungen, ihre LDTs vollständig an die Anforderungen der Verordnung anzupassen – von der Entwicklung über die Herstellung bis hin zur laufenden Überwachung. Ein wesentlicher Punkt: Es besteht kein Bestandsschutz. Auch langjährig etablierte und bewährte Tests müssen die IVDR-Vorgaben erfüllen. Der Einsatz eigener LDTs ist künftig nur zulässig, wenn kein vergleichbares IVD mit ausreichender Leistungsfähigkeit auf dem Markt verfügbar ist. Diese regulatorischen Vorgaben stellen insbesondere für pathologische Labore eine erhebliche organisatorische und dokumentarische Herausforderung dar.1
Die dargestellte Roadmap kann als Orientierungshilfe dienen, um die Umsetzung der IVDR besser zu bewältigen. Welcher Schritt zu welchem Zeitpunkt der richtige ist, hängt dabei von der individuellen Situation des Labors ab.

Ein Labor, das ein LDT verwenden möchte, sollte die Anforderungen der IVDR gründlich prüfen und sich mit folgenden Schritten vorbereiten, die erforderlichen Bestimmungen zu erfüllen.
Überprüfen und aktualisieren Sie Ihr IVD-Portfolio: Definieren Sie Ihre Inhouse-Methoden und entscheiden Sie, welche weiterhin verwendet werden sollen.
Die definierte Zweckbestimmung gibt an, wofür das Produkt im medizinischen Sinne gedacht ist, in welchem medizinischen Kontext es verwendet und wie es angewendet wird. Sie beschreibt die Verwendung, für die ein Produkt nach Angaben des Herstellers bestimmt ist. Ist Ihr Produkt ein IVD? Welcher Risikoklasse gehört Ihr Produkt an und welche gesetzlichen Anforderungen leiten sich daraus ab?6
Zur Einhaltung der IVDR muss das QM-System ergänzt werden: Welche Komponenten fehlen? Für medizinische Labore sind die Vorgaben der RiLi-BÄK 2024 ohnehin verpflichtend.7 Die Akkreditierung nach DIN EN ISO 15189 für medizinische Labore und nach DIN EN ISO/IEC 17020 für Pathologien ist der effektivste Weg, um diese Forderung der IVDR zu erfüllen.8,9
Eine Pressemitteilung im April 2025 weist darauf hin, dass eine RiLi-BÄK speziell für die Pathologie veröffentlicht werden soll. Was genau dahinter steckt, können Sie hier nachlesen.
Die IVDR fordert ein Risikomanagementsystem im Zusammenhang mit der Entwicklung und Anwendung diagnostischer Produkte. Ziel eines solchen Systems ist es, potenzielle Gefährdungen und Risiken, die bei der Nutzung der Produkte im pathologischen Arbeitsumfeld auftreten können, zu identifizieren, zu bewerten und zu minimieren. Gemäß IVDR sind dabei Informationen aus der Marktüberwachung hinsichtlich Art und Häufigkeit von Risiken sowie in Bezug auf das Gesamtrisiko, das Nutzen-Risiko-Verhältnis und die Risikoakzeptanz systematisch zu analysieren.1
Gemäß Artikel 5 (5) muss die technische Dokumentation Informationen über den Herstellungsort, das Herstellungsverfahren, die Konstruktion und die Leistungsdaten der Produkte einschließlich ihres Verwendungszwecks enthalten. Die Daten müssen ausreichend detailliert sein und darlegen, dass Ihr Produkt die grundlegenden Sicherheits- und Leistungsanforderungen gemäß Anhang I der IVDR erfüllt. Diese Bestimmung gilt mindestens für Produkte der Risikoklasse D. Die Mitgliedstaaten können sie jedoch auch auf Produkte anwenden, die in Risikoklasse A, B, oder C eingestuft sind.1
Roadmap IVDR: So behalten Sie den Überblick
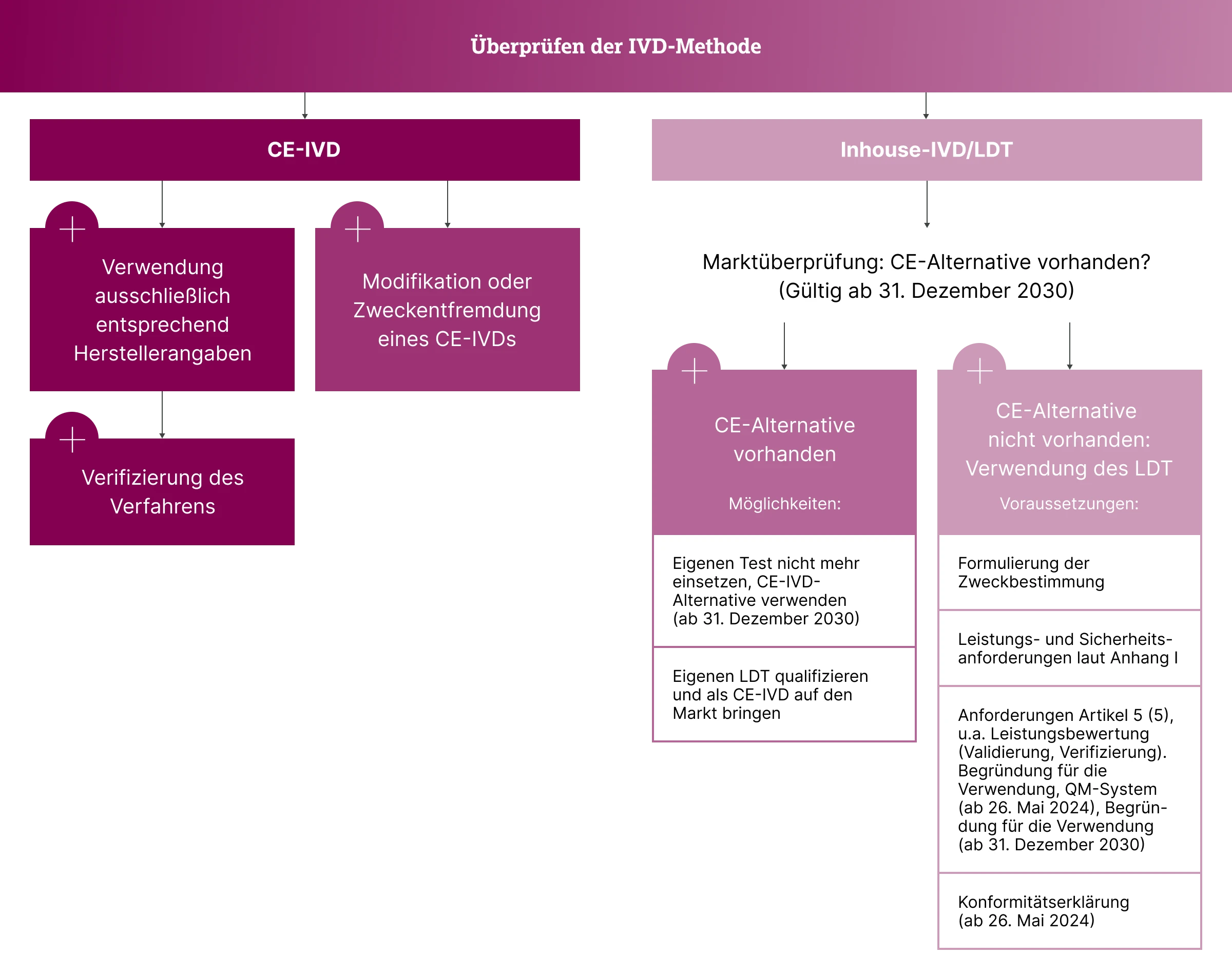
Roadmap IVDR: Mögliche Wege für diagnostische Labore durch die IVDR (mod. nach Hafen U. Johner Institut, 2024)5
Auch nach mehreren Jahren der Umsetzung der IVDR stehen Pathologien als diagnostische Laboratorien weiterhin vor wichtigen regulatorischen Herausforderungen. Ein umfassendes Inventar der verwendeten IVDs bleibt unerlässlich für die Praxis.
Labore sind von der IVDR grundsätzlich angehalten, IVDs mit einer CE-Zertifizierung zu verwenden. Die IVDR gibt den Laboren jedoch die Möglichkeit, weiterhin LDTs herzustellen und anzuwenden, um den spezifischen Bedürfnissen von Patientengruppen gerecht zu werden, die sonst nicht erfüllt werden können (Art. 29).1
Die IVDR gibt vor, dass ab 2031 bezüglich der Verwendung von LDTs Sonderregelungen gelten: Existieren vergleichbare kommerzielle CE-IVDs auf dem Markt, die die gewünschte Leistung für Ihre spezifische Patientenzielgruppe erbringen können? Falls ja, wird die Umstellung auf diese kommerziellen Alternativen obligatorisch. Gibt es kein äquivalentes kommerzielles CE-IVD, kann das diagnostische Labor die eigenentwickelte Testmethode im Rahmen der IVDR verwenden. Dabei gelten die Anforderungen aus Anhang I – vorausgesetzt, Artikel 5 (5) wird eingehalten. Diese Marktüberwachung erfordert eine systematische und dokumentierte Bewertung verfügbarer Produkte.1
Abkürzungen
CE: Conformité Européenne; EU: Europäische Union; IVD: In-vitro-Diagnostikum; IVDD: In-vitro-Diagnostik-Richtlinie; IVDR: In-vitro-Diagnostik-Verordnung; LDT: Laboratory Developed Test; MPG: Medizinproduktegesetz; QM: Qualitätsmanagement; QMS: Qualitätsmanagement-System; RiliBÄK: Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
- Amtsblatt der Europäischen Union. Verordnung über In-Vitro-Diagnostik und zur Aufhebung der Richtilinie 98/79/EG und des Beschlusses 2010/227/EU der Kommission, 2025. Verfügbar unter: https://eur-lex.europa.eu/legal-content/DE/TXT/HTML/?uri=CELEX:32017R0746&qid=1643555738061&from=DE). Letzter Zugriff: Dezember 2025.
- Stenzinger A et al. Pathologe 2020. (https://www.pathologie-dgp.de/media/Dgp/aktuelles/DGP-VHB2020_W._Weichert_IVDR__Der_Pathologe_Suppl.3_Dez.2020_.pdf). Letzter Zugriff: Dezember 2025.
- GMS Zeitschrift zur Förderung der Qualitätssicherung in medizinischen Laboratorien. Stellungnahme der Ad-hoc-Kommission In-vitro-Diagnostika der AWMF zur Umsetzung der Verordnung (EU) 2017/746 (IVDR) im Hinblick auf In-vitro-Diagnostika aus Eigenherstellung, 2025. (https://www.egms.de/static/en/journals/lab/2021-12/lab000043.shtml). Letzter Zugriff: Dezember 2025.
- European Commission. Verordnung über In-vitro-Diagnostika, 2021.
- Hafen U. Die EU reguliert medizinische Labore. Sind Inhouse-IVD (LDT) noch erlaubt? Johner Institut GmbH. 2024 Apr 6.
- Havlicek J. Zweckbestimmung und bestimmungsgemäßer Gebrauch: Folgenreicher als Sie denken! Johner Institut GmbH. 2025 Oct 4.
- Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen (Rili-BÄK-2019). Verfügbar unter https://www.bundesaerztekammer.de/fileadmin/user_upload/BAEK/Themen/Qualitaetssicherung/_Bek_BAEK_RiLi_BAEK_ONLINE_FINAL_VERS_26_05_2023.pdf. Letzter Zugriff: Dezember 2025.
- Deutsche Akkreditierungsstelle. Regel zur Akkreditierung von medizinischen Laboratorien nach DIN EN ISO 15189:2024, 2024. (https://www.dakks.de/files/Dokumentensuche/Dateien/R-15189_Akkreditierung%20von%20medizinischen%20Laboratorien.pdf). Letzter Zugriff: Dezember 2025.
- Deutsche Akkreditierungsstelle, 2025. (https://www.dakks.de/de/fb-3.5.html). Letzter Zugriff: Dezember 2025.



