Molekulare Treiber beim NSCLC – Grundlage der personalisierten Therapie
Die zielgerichtete Therapie beim nicht-kleinzelligen Lungenkarzinom (NSCLC) beruht heute in weiten Teilen auf der Identifikation sogenannter onkogener Treibermutationen. Für Patient:innen mit nicht-plattenepithelialem NSCLC – insbesondere im metastasierten Stadium – ist die molekulare Testung auf relevante Biomarker zu einem integralen Bestandteil der Diagnostik und Therapieplanung geworden.1
Genetische Veränderungen in EGFR, ALK, ROS1, BRAF, MET, RET, NTRK, KRAS oder HER2 (ERBB2) definieren Subgruppen, für die heute zugelassene oder in Entwicklung befindliche zielgerichtete Therapien zur Verfügung stehen – mit teils deutlicher Verlängerung des progressionsfreien Überlebens und Gesamtüberlebens.1
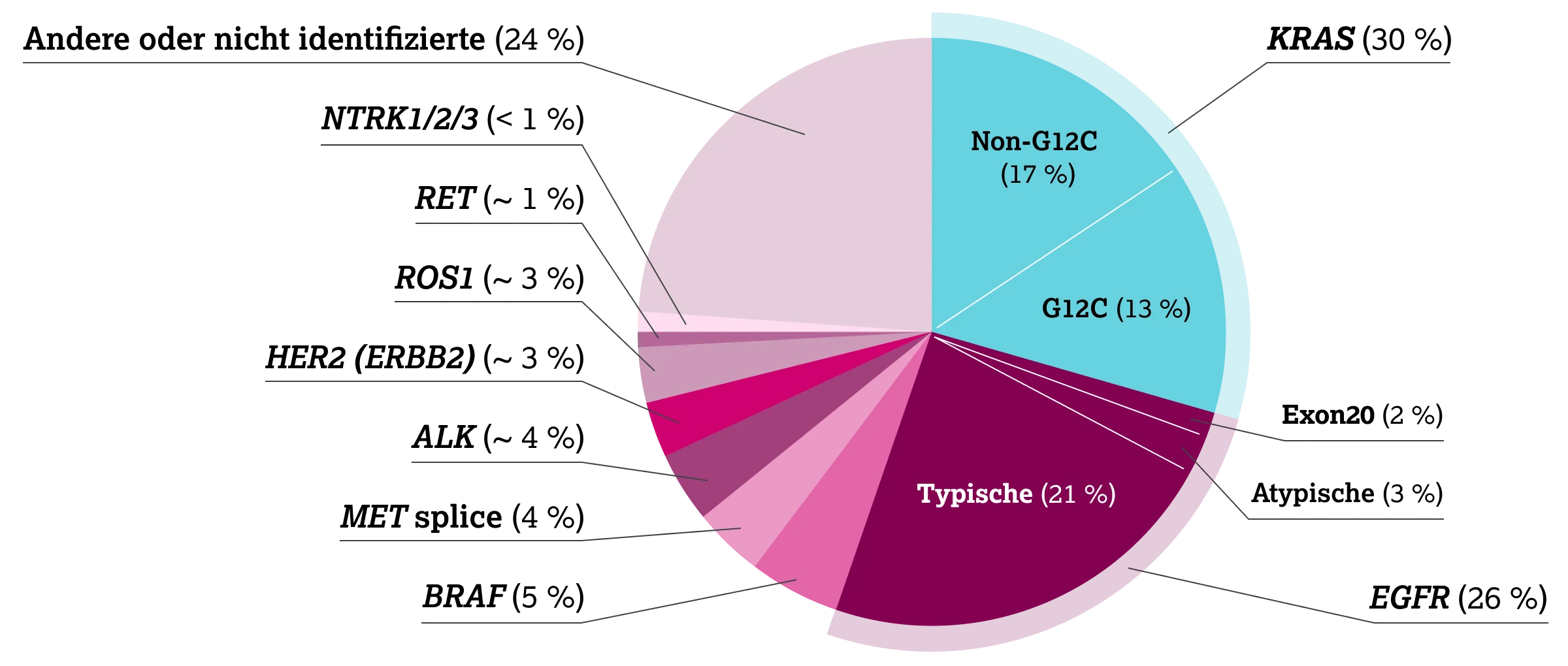
Eine frühe und umfassende molekulare Testung – idealerweise durch Next-Generation-Sequencing (NGS) – bildet somit die Grundlage für die personalisierte Behandlung und eine verbesserte Prognose bei NSCLC.1,4
Relevanz der umfassenden molekularen Testung beim NSCLC
Nationale und internationale Leitlinien, darunter S3-, Onkopedia-, NCCN- und ESMO-Leitlinien, empfehlen für Patient:innen mit fortgeschrittenem NSCLC eine breite molekulare Testung, die über die Analyse einzelner Biomarker hinausgeht.4–7 Ziel ist es, alle therapeutisch relevanten genomischen Veränderungen frühzeitig zu identifizieren und eine zielgerichtete Therapie zu ermöglichen.
Design einer retrospektiven Kohortenstudie (Aggarwal et al., 2022)
Eine retrospektive Kohortenstudie von Aggarwal et al. (2022) untersuchte 335 Patient:innen mit neu diagnostiziertem nicht-plattenepithelialen NSCLC im Stadium IV. Erfasst wurden die getesteten Gene, das verwendete Probenmaterial (Gewebe, Plasma) und der Zeitpunkt der Testung.8
Die Studienpopulation wurde in drei Gruppen unterteilt:8
Umfassende Testung
Analyse von Mutationen der Biomarker EGFR, ALK, BRAF, ROS1, MET, RET und NTRK
Unvollständige Testung
Testung von 2 bis 6 Genen
Keine molekulare Testung
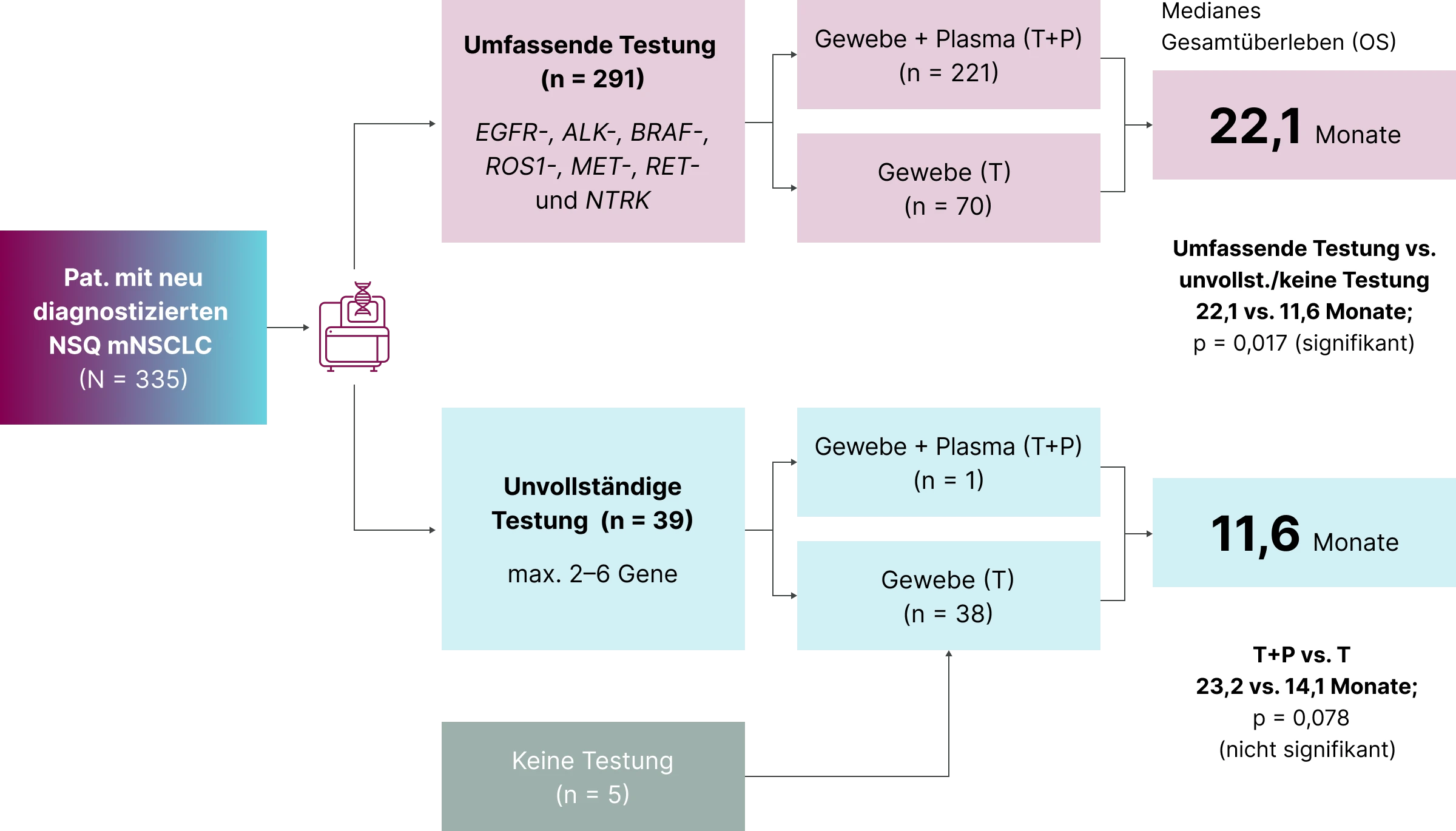
Die molekulare Diagnostik erfolgte mittels NGS entweder aus Gewebe (T), Plasma (P) oder beiden Probenquellen (T+P).8
Bei einer medianen Nachbeobachtungszeit von 20,5 Monaten betrug das mediane OS 18,6 Monate. Das mediane OS für Patient:innen mit einer NGS-Analyse von Gewebe und Plasma (T+P) war mit 23,2 Monaten gegenüber 14,1 Monaten für Patient:innen, bei denen nur Gewebe (T) getestet wurde, numerisch länger, jedoch statistisch nicht signifikant (p = 0,078). Unabhängig von der Testmethode hatten Patient:innen mit umfassender molekularer Genotypisierung jedoch ein signifikant überlegenes OS im Vergleich zu Patient:innen mit unvollständiger oder keiner Testung (22,1 Monate vs. 11,6 Monate, p = 0,017).
Die gleichzeitige Genotypisierung von Gewebe und Plasma erhöhte den Anteil von Erkrankten, die eine leitliniengerechte, umfassende molekulare Testung erhielten, sowohl insgesamt als auch vor Beginn der Erstlinientherapie.8
Die kombinierte Testung aus Gewebe und Plasma erhöhte signifikant die Rate der vor Therapiebeginn vorliegenden Testergebnisse. So lagen bei 100 % der Patient:innen mit kombinierter Analyse (n = 204) die Befunde vor Start der Erstlinientherapie vor. Bei ausschließlich gewebebasierten Testungen traf dies nur auf 60,7 % zu (p < 0,0001).8
Patient:innen, die eine vollständige molekulare Testung erhielten, profitierten von einem signifikant verlängerten medianen Gesamtüberleben (OS) von 22,1 Monaten. Bei unvollständiger oder fehlender Testung betrug das mediane OS lediglich 11,6 Monate (p = 0,017).8 Dies unterstreicht den unmittelbaren Einfluss einer frühzeitigen und umfassenden molekularen Charakterisierung auf die Prognose.
Auch Patient:innen ohne nachweisbare molekulare Zielstruktur können von einer umfassenden molekularen Testung profitieren: In den aktuellen NSCLC-Leitlinien wird empfohlen, in solchen Fällen die Teilnahme an klinischen Studien zu prüfen und nach Möglichkeit anzubieten.4,7 So erhalten genetisch definierte Subgruppen Zugang zu innovativen Wirkstoffen, auch wenn diese noch nicht zum Therapiestandard gehören.
Daten aus der europäischen Prospektivstudie von Passiglia et al. (2025) bestätigen diesen Ansatz: Patient:innen, bei denen durch molekulares Profiling relevante Mutationen identifiziert wurden, hatten durch den Einschluss in geeignete Studien eine signifikant bessere Überlebenschance – selbst wenn keine zugelassene Standardtherapie verfügbar war.9
Abkürzungen
ALK: Anaplastische Lymphomkinase (Gen); BRAF: Serin/Threonin-Kinase B-Raf (Gen); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Protein); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); ERBB: v-erb-b2 erythroblastic leukemia viral oncogene homolog; ESMO: European Society for Medical Oncology; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; KRAS: Kirsten Rat Sarkoma Onkogen (Gen); MET: Mesenchymal-epithelialer Transitionsfaktor (Gen); NCCN: National Comprehensive Cancer Network; NGS: Next-Generation-Sequencing; NSCLC: nicht-kleinzelliges Lungenkarzinom; NTRK: Neurotrophe Tyrosinrezeptor-Kinasen (Gen); OS: Gesamtüberleben; RET: Rearranged during Transfection (Rezeptor-Tyrosinkinase); ROS1: ROS-Protoonkogen 1 (Gen)
- Batra U, et al. Oncol Rev 2024;18:1445826.
- Friedlaender A, et al. Biomark Res 2024;12(1):24.
- Thai AA, et al. Lancet 2021;398(10299):535–54.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig (NSCLC); April 2025. Verfügbar unter onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: August 2025.
- Riely GJ, et al. J Natl Compr Canc Netw 2024;22(4):249–74.
- Hendriks LE, et al. (2025). ESMO Oncogene-Addicted Non-Small Cell Lung Cancer Living Guideline v1.2. Verfügbar unter https://www.esmo.org/guidelines/living-guidelines/esmo-living-guideline-oncogene-addicted-metastatic-non-small-cell-lung-cancer. Letzter Zugriff: August 2025.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: August 2025.
- Aggarwal C, et al. J Clin Oncol 2022;40(16_suppl):9022.
- Passiglia F, et al. J Thorac Oncol 2025;20(5):614–24.

