Was ist HRD?
Zellen verfügen über effektive Mechanismen zur Erkennung und Reparatur von DNA-Schäden (DNA-Damage-Response, DDR), um Mutationen und die Weitergabe fehlerhafter Erbinformationen zu verhindern. Für unterschiedliche Arten von DNA-Schäden existieren unterschiedliche Reparaturmechanismen.
Ein zentraler Mechanismus ist die homologe Rekombinationsreparatur (HRR). Kommt es hier zu einem Funktionsverlust – bezeichnet als homologe Rekombinationsdefizienz (HRD) – häufen sich Genomschäden (sogenannte Genomic Scars) wie Deletionen oder chromosomale Strukturveränderungen an. Dies führt zu einer ausgeprägten genomischen Instabilität.
Defekte in den DNA-Reparaturmechanismen spielen daher eine entscheidende Rolle in der Krebsentstehung. Der Verlust dieser zellulären Kontrollsysteme begünstigt die Akkumulation onkogener Mutationen und fördert die maligne Transformation.
Reparaturmechanismen bei DNA-Schäden
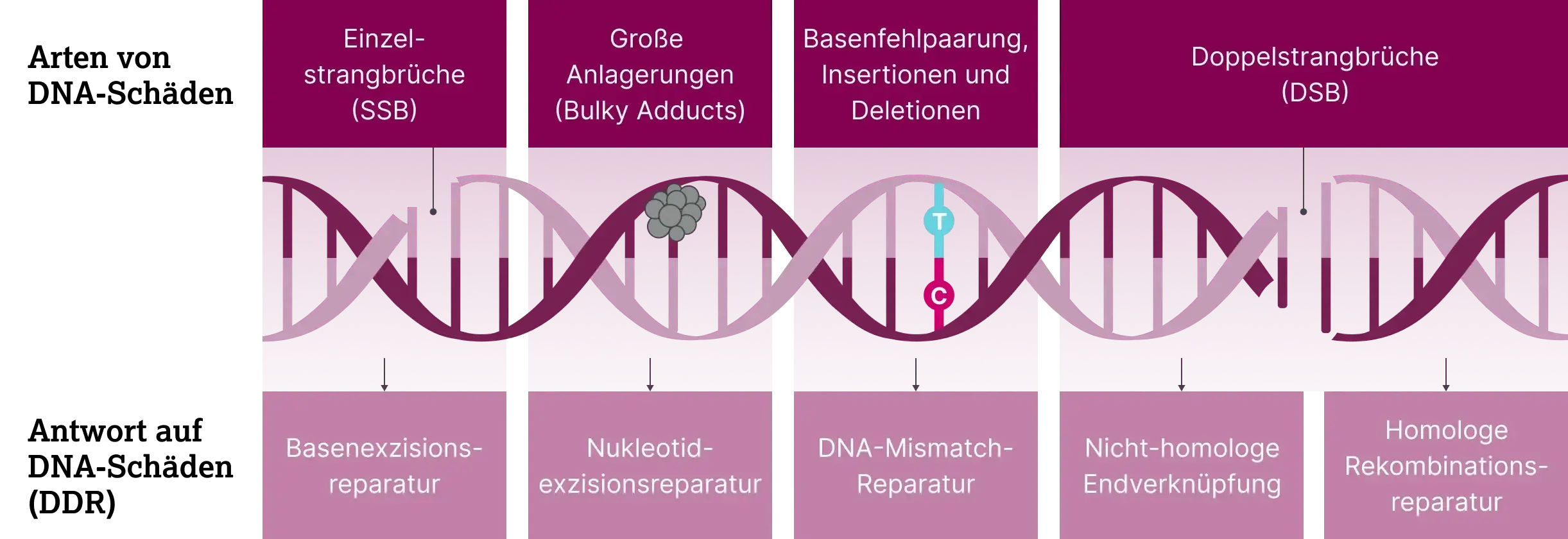
Zellen verfügen über spezialisierte Reparatursysteme, um Schäden an der DNA zu beheben.1,2 Die Wahl des Reparaturmechanismus hängt von Art und Ausmaß des Schadens ab. Beispielsweise werden Einzelstrangbrüche (SSB) und Doppelstrangbrüche (DSB) jeweils über unterschiedliche Enzymkomplexe detektiert und repariert.
Proofreading
Das Korrekturlesen (Proofreading) ist ein grundlegender Reparaturmechanismus, der direkt während der DNA-Replikation erfolgt. DNA-Polymerasen sind in der Lage, ihre eigenen Fehler unmittelbar zu erkennen und zu korrigieren. Auf diese Weise werden viele Replikationsfehler bereits beseitigt, bevor sie sich dauerhaft im Genom verankern. Dennoch sind zusätzliche Reparaturmechanismen notwendig, um Schäden zu beheben, die nach Abschluss der Replikation zurückbleiben oder neu entstehen – etwa infolge von Basenfehlpaarungen oder exogenen Einflüssen.
Reparatur von Einzelstrangschäden
Einzelstrangschäden betreffen nur einen der beiden DNA-Stränge und treten deutlich häufiger auf als Doppelstrangschäden. Die Zelle verfügt über drei spezialisierte Hauptmechanismen, die je nach Art des Einzelstrangschadens zum Einsatz kommen.1,2
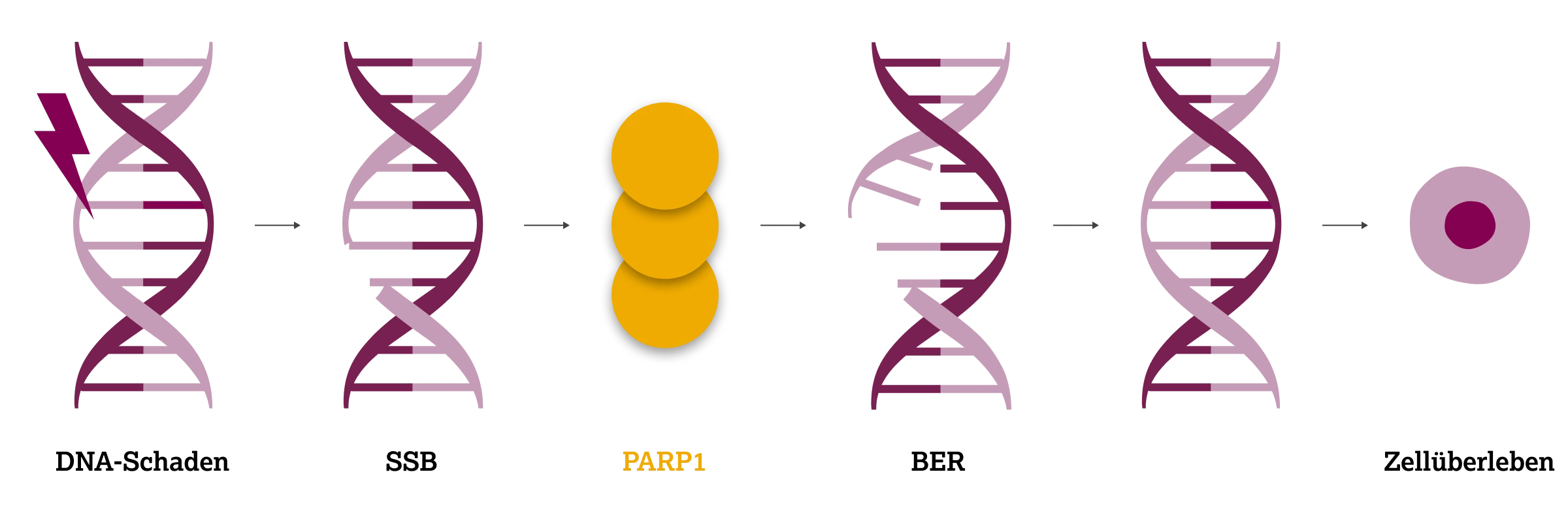
Die Basenexzisionsreparatur (BER) beseitigt DNA-Schäden, die durch Oxidation, Alkylierung oder Desaminierung an einzelnen Basen entstehen. Der Prozess beginnt mit der Bindung des Enzyms Poly(ADPribose)-Polymerase 1 (PARP1) an die geschädigte DNA-Stelle. Dadurch wird der Bereich für das Reparatursystem zugänglich. Nach der Dissoziation von PARP1 erkennt das Enzym DNA-Glykosylase die geschädigte Base und entfernt sie. Anschließend fügt eine DNA-Polymerase die korrekte Base auf Grundlage des komplementären Strangs ein. Je nach Ausmaß der Reparatur wird zwischen zwei Varianten der BER unterschieden: Beim Short Patch Repair wird eine einzelne Base ersetzt, während beim Long Patch Repair ein längeres Fragment von bis zu 20 Nukleotiden erneuert wird. Den Abschluss der Reparatur übernimmt eine DNA-Ligase, die den DNA-Strang wieder vollständig verknüpft.
Im Gegensatz zur Basenexzisionsreparatur erkennt die Nukleotidexzisionsreparatur (NER) vor allem sogenannte „Bulky Lesions“ – DNA-Schäden, die die Helixstruktur durch lokale Verwindungen oder Verformungen stören. Die NER umfasst mehrere Schritte: Zunächst erfolgt die Schadenserkennung, gefolgt vom beidseitigen Einschneiden der DNA und der Entfernung eines etwa 20–30 Basen langen DNA-Abschnitts. Anschließend wird der fehlende Abschnitt durch Neusynthese ergänzt und der Strang durch eine DNA-Ligase verschlossen.
Die Fehlpaarungsreparatur bzw. DNA-Mismatch-Reparatur (MMR) korrigiert Basenfehlpaarungen, die nach der DNA-Replikation in den neu synthetisierten Strängen zurückbleiben. Die Erkennung erfolgt durch ein Heterodimer aus den MutS-Homolog-Proteinen MSH2 und entweder MSH6 oder MSH3, abhängig von der Größe und Struktur der Fehlpaarung. Ein zweites Heterodimer, bestehend aus dem MutL-Homolog-Protein MLH1 und der Endonuklease PMS2, leitet den Schnitt im fehlerhaften Strang ein. Anschließend entfernt eine Exonuklease den betroffenen DNA-Abschnitt. Die entstandene Lücke wird durch Neusynthese mittels einer DNA-Polymerase aufgefüllt und der Strang anschließend durch eine DNA-Ligase verschlossen.5
Reparatur von Doppelstrangschäden
DSB zählen zu den kritischen DNA-Schäden, da sie zu weitreichenden chromosomalen Umlagerungen führen können. Ihre Reparatur ist komplex und nicht immer fehlerfrei. Abhängig von der Phase des Zellzyklus stehen der Zelle zwei Hauptmechanismen zur Verfügung.1,2
Die nicht-homologe Endverknüpfung (Non Homologous End Joining, NHEJ) ist der häufigste Reparaturmechanismus für DSB und funktioniert sequenzunabhängig. Dabei werden die offenen DNA-Enden direkt miteinander verknüpft – auch wenn dabei kleinere Sequenzabschnitte verloren gehen können (DNA-Deletionen). Aufgrund dieser fehlenden Sequenztreue gilt die NHEJ als fehleranfällig. Aktiv ist dieser Mechanismus vor allem in der G1-Phase des Zellzyklus.
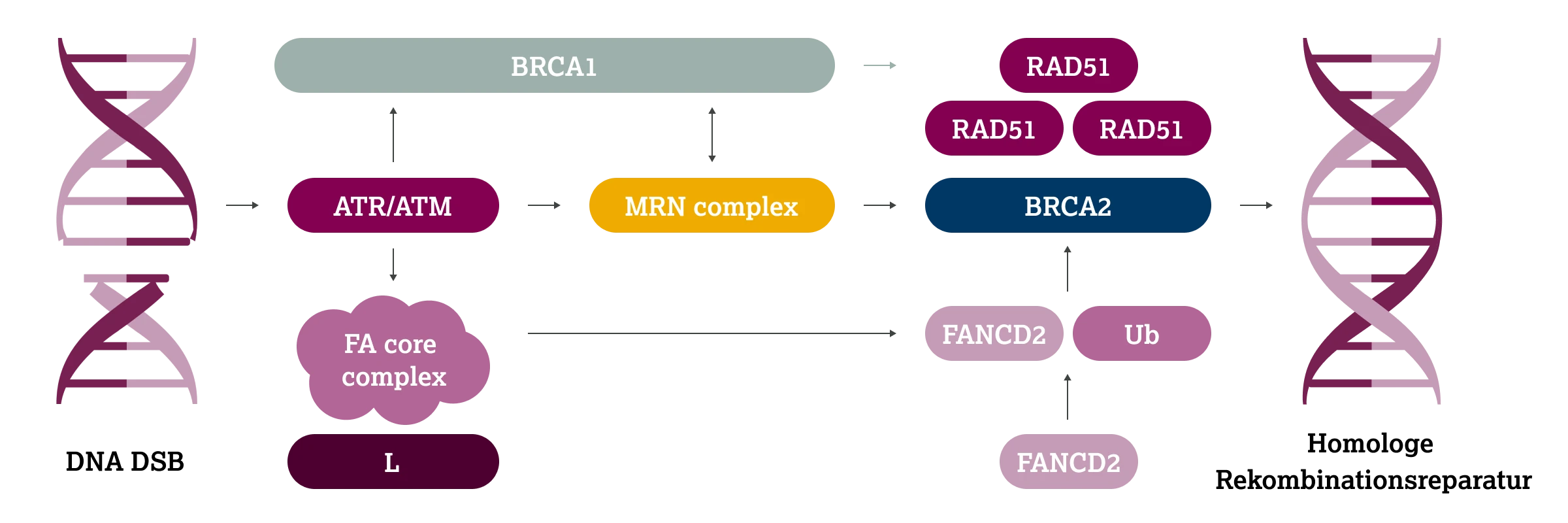
Die homologe Rekombination stellt den einzigen weitgehend fehlerfreien Mechanismus zur Reparatur von DSB dar. Sie nutzt das Schwesterchromatid als exakte Vorlage für die Wiederherstellung der ursprünglichen DNA-Sequenz und ist daher auf die S- und G2-Phase des Zellzyklus beschränkt. Dieser Prozess erfordert das Zusammenspiel zahlreicher Proteine – darunter BRCA1, BRCA2 und weitere Schlüsselfaktoren der DNA-Reparatur.6
Genetische Ursachen der HRD
Eine homologe Rekombinationsdefizienz (HRD), also der Funktionsverlust der HRR, zählt zu den gravierendsten DNA-Reparaturdefekten, da sie zur Anhäufung komplexer struktureller Veränderungen im Genom führen kann und eng mit einer ausgeprägten genomischen Instabilität assoziiert ist.
HRD kann durch Keimbahn- oder somatische Mutationen in Genen verursacht werden, die für Schlüsselproteine der HRR kodieren. Die bekanntesten genetischen Ursachen sind pathogene Varianten in den Genen Breast Cancer Associated Gene 1 (BRCA1) oder Breast Cancer Associated Gene 2 (BRCA2).
Darüber hinaus können auch Veränderungen in weiteren HRR-assoziierten Genen, wie z. B. ATM oder RAD51, zu einem sogenannten BRCAness-Phänotyp führen. Dieser ist durch einen funktionellen Ausfall der HRR charakterisiert, obwohl keine Keimbahnmutation in BRCA1 oder BRCA2 vorliegt.7 Eine Übersicht relevanter HRR-Gene und ihrer Funktionen ist in der Tabelle dargestellt.
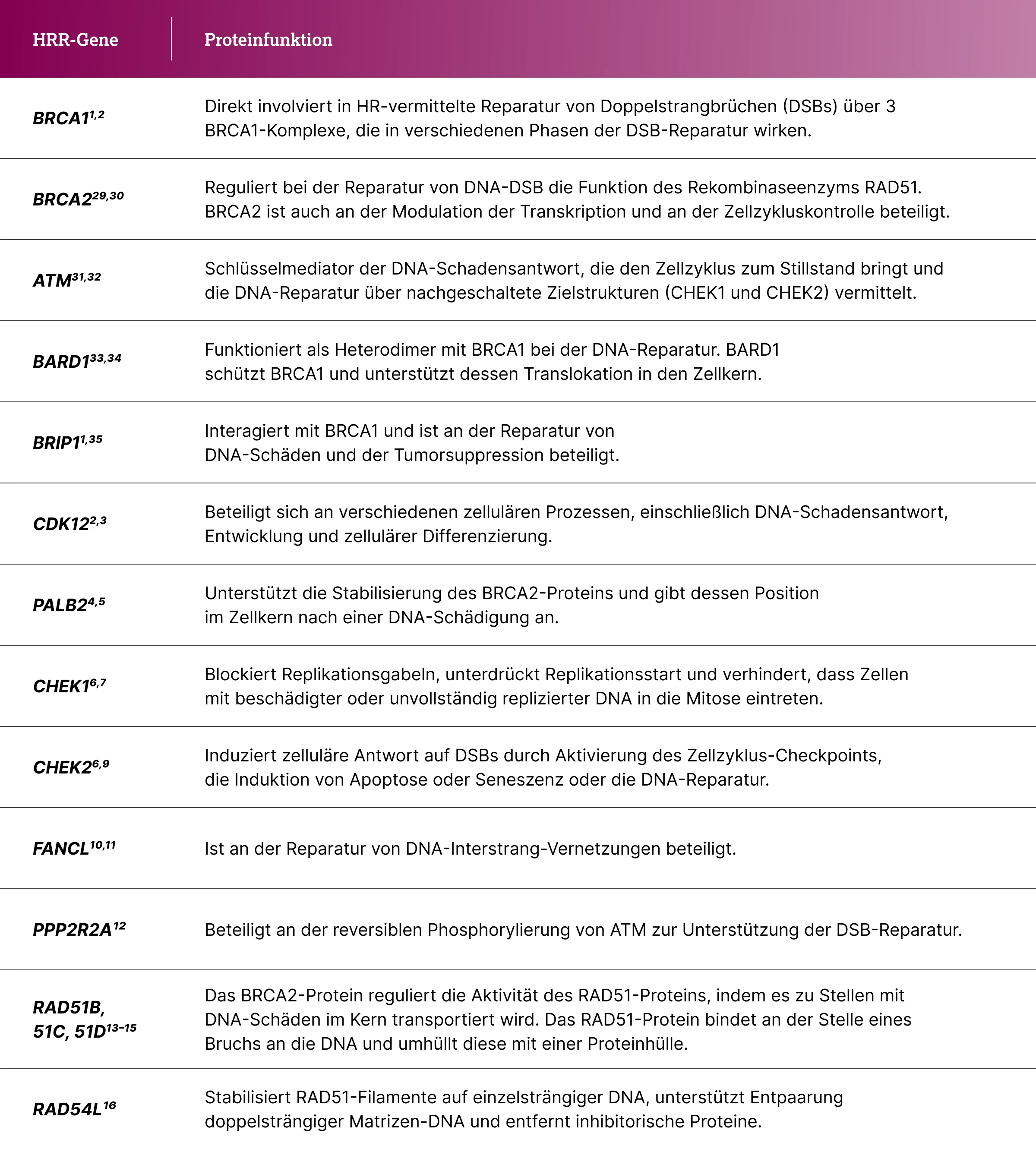
Kommt es in einem dieser Gene zu einer pathogenen Veränderung, die mit einem Funktionsverlust des entsprechenden Proteins einhergeht, kann die HRR beeinträchtigt sein. Nach der Second-Hit-Hypothese ist hierfür in der Regel der Verlust beider Allele erforderlich sowie das Fehlen einer kompensatorischen Mutation, die den Effekt der Genveränderung neutralisieren könnte.32
Ein erklärendes Video zu den genetischen Ursachen und zum Nachweis der HRD finden Sie hier:
Abkürzungen
TM: Ataxia Telangiectasia Mutated (Gen); BARD1: BRCA1 Associated Ring Domain 1 (Gen); BER: Basenexzisionsreparatur; BRCA1: Breast Cancer Associated Gene 1; BRCA2: Breast Cancer Associated Gene 2; BRIP1: BRCA1-Interacting Protein 1 (Gen); CDK12: Cyclin-abhängige Kinase 12 (Gen); CHEK1: Checkpoint Kinase 1 (Gen); CHEK2: Checkpoint Kinase 2 (Gen); DDR: DNADamageResponse; DNA: Desoxyribonukleinsäure; DSB: Doppelstrangbruch; FANCL: Fanconi Anemia Complementation Group L (Gen); HRD: homologe Rekombinationsdefizienz; HRR: homologe Rekombinationsreparatur; MLH1: MutL Homolog 1; MMR: DNA-Mismatch-Reparatur; MSH2: Mutator S Homolog 2; MSH3: Mutator S Homolog 3; MSH6: Mutator S Homolog 6; NER: Nukleotidexzisionsreparatur; NHEJ: nicht-homologe Endverknüpfung; PALB2: Partner and Localizer of BRCA2 (Gen); PARP1: Poly(ADPribose)Polymerase 1; PMS2: Postmeiotic Segregation Increased 2; PPP2R2A: Protein Phosphatase 2 Regulatory Subunit Balpha (Gen); RAD51B: RAD51 Paralog B (Gen); RAD51C: RAD51 Paralog C (Gen); RAD51D: RAD51 Paralog D (Gen); RAD54L: RAD54 Like (Gen); SSB: Einzelstrangbruch
- Lord CJ & Ashworth A. Nature 2012;481(7381):287–94.
- Nickoloff JA. DNA Repair Dysregulation in Cancer: From Molecular Mechanisms to Synthetic Lethal Opportunities. In: Stress Response Pathways in Cancer. Molecular Targets to Novel Therapeutics; Editor: Wondrak GT; Springer. 2015;7–28.
- Walsh CS. Gynecol Oncol 2015;137(2):343–50.
- Konstantinopoulos PA, et al. Cancer Discov 2015;5(11):1137–54.
- Marinus MG. EcoSal Plus 2012;5(1).
- Turner N, et al. Nat Rev Cancer 2004;4(10):814–9.
- Lord CJ & Ashworth A. Nat Rev Cancer 2016;16(2):110–20.
- Takaoka M & Miki Y. Int J Clin Oncol 2018;23(1):36–44.
- Ratajska M, et al. Oncol Rep 2008;19(1):263–8.
- Moro L, et al. J Vis Exp 2015;(102):e52849.
- Weber AM & Ryan AJ. Pharmacol Ther 2015;149:124–38.
- Stankovic T, et al. Am J Hum Genet 1998;62(2):334–45.
- Irminger-Finger I, et al. Int J Biochem Cell Biol 2016;72:1–17.
- Klonowska K, et al. Sci Rep 2015;5:10424.
- Ouhtit A, et al. Front Biosci (Elite Ed) 2016;8(2):289–98.
- Kim H, et al. Cancer Res Treat 2016;48(3):955–61.
- Paculova H & Kohoutek J. Cell Div 2017;12:7.
- Popova T, et al. Cancer Res 2016;76(7):1882–91.
- Wesola M & Jelen M. Adv Clin Exp Med 2017;26(2):339–42.
- Nepomuceno TC, et al. Int J Mol Sci 2017;18(9).
- Smits VA & Gillespie DA. FEBS J 2015;282(19):3681–92.
- Solyom S, et al. Fam Cancer 2010;9(4):537–40.
- Zannini L, et al. J Mol Cell Biol 2014;6(6):442–57.
- Siolek M, et al. Int J Cancer 2015;137(3):548–52.
- Garcia MJ, et al. Carcinogenesis 2009;30(11):1898–902.
- Vetro A, et al. Hum Mutat 2015;36(5):562–8.
- Kalev P, et al. Cancer Res 2012;72(24):6414–24.
- Cousineau I, et al. Cancer Res 2005;65(24):11384–91.
- Silva MC, et al. DNA Repair (Amst) 2016;42:44–55.
- Leone PE, et al. BMC Cancer 2003;3:6.
- Mazin AV, et al. DNA Repair (Amst) 2010;9(3):286-302.
- Knudson AG. Nat Rev Cancer 2001;1(2):157–62.





