HER2-Diagnostik allgemein
Unterschiedliche Testverfahren für unterschiedliche HER2-Alterationen
HER2-Alterationen finden sich bei einer Vielzahl solider Tumoren.1 In der Literatur werden drei unterschiedliche Alterationstypen beschrieben, deren Prävalenz je nach Tumorentität und Studie deutlich variiert.1

Informationen zu HER2-Alterationen
Für die pathologische Diagnostik ist entscheidend, welche HER2-Alteration nachgewiesen werden soll. Insbesondere ist zwischen HER2-Überexpression, HER2 (ERBB2) Gen-Amplifikation und HER2 (ERBB2) Gen-Mutationen zu unterscheiden.
Der Nachweis einer HER2-Überexpression erfolgt primär mittels Immunhistochemie (IHC), während HER2 (ERBB2) Gen-Amplifikationen in der Regel durch In-situ-Hybridisierungstechniken wie FISH oder CISH detektiert werden. HER2 (ERBB2) Gen-Mutationen erfordern den Einsatz molekularer Verfahren, typischerweise das Next-Generation-Sequencing (NGS).
Für eine adäquate HER2-Diagnostik ist somit eine alterationsspezifische Methodenauswahl erforderlich – abhängig von klinischer Fragestellung und Tumorbiologie.2–5

Nachweis von HER2-Überexpression und HER2 (ERBB2) Amplifikation
Für Entitäten, bei denen die HER2-Überexpression im Vordergrund steht (bspw. Brust und Magen), wird zunächst eine schnell und kostengünstig durchzuführende IHC-Testung durchgeführt und nur im Falle eines unklaren IHC-Ergebnisses wird zusätzlich eine aufwändigere und teurere ISH zur Abklärung nachgeschaltet.2,3
Durch eine an einem formalinfixierten, in Paraffin eingebetteten (FFPE) Gewebeschnitt angewendete Färbetechnik mit markierten Antikörpern können die HER2-Rezeptoren an der Zelloberfläche sichtbar gemacht werden. Unter dem Mikroskop werden Intensität und Ausmaß der Färbung beurteilt. Das Ergebnis wird z. B. beim Mammakarzinom über einen qualitativen IHC-Score von 0 bis 3+ ausgedrückt.2,3
Eine ISH kann sowohl an frisch gefrorenem Tumormaterial als auch an FFPE-Tumormaterial durchgeführt werden. Dabei werden die HER2 (ERBB2) Gene durch speziell markierte DNA-Sonden sichtbar gemacht, die komplementär zu den relevanten genomischen Sequenzen sind.6
- Bei der Fluoreszenz-in-situ-Hybridisierung (FISH) werden die Sonden mit Fluoreszenzfarbstoffen markiert und die Signale mithilfe eines Fluoreszenzmikroskops ausgewertet.6
- Die chromogene In-situ-Hybridisierung (CISH) wurde als Alternative zur FISH entwickelt. Dabei werden die DNA-Sonden mit sog. Chromogenen (Farbstoffen) angefärbt. Zur Auswertung genügt ein konventionelles Lichtmikroskop.6
- Die Sondenbindung kann aber auch über silberverstärkte In-situ-Hybridisierung (SISH) sichtbar gemacht werden. Die Auswertung der Signalzahl kann hier ebenfalls im Lichtmikroskop erfolgen.6
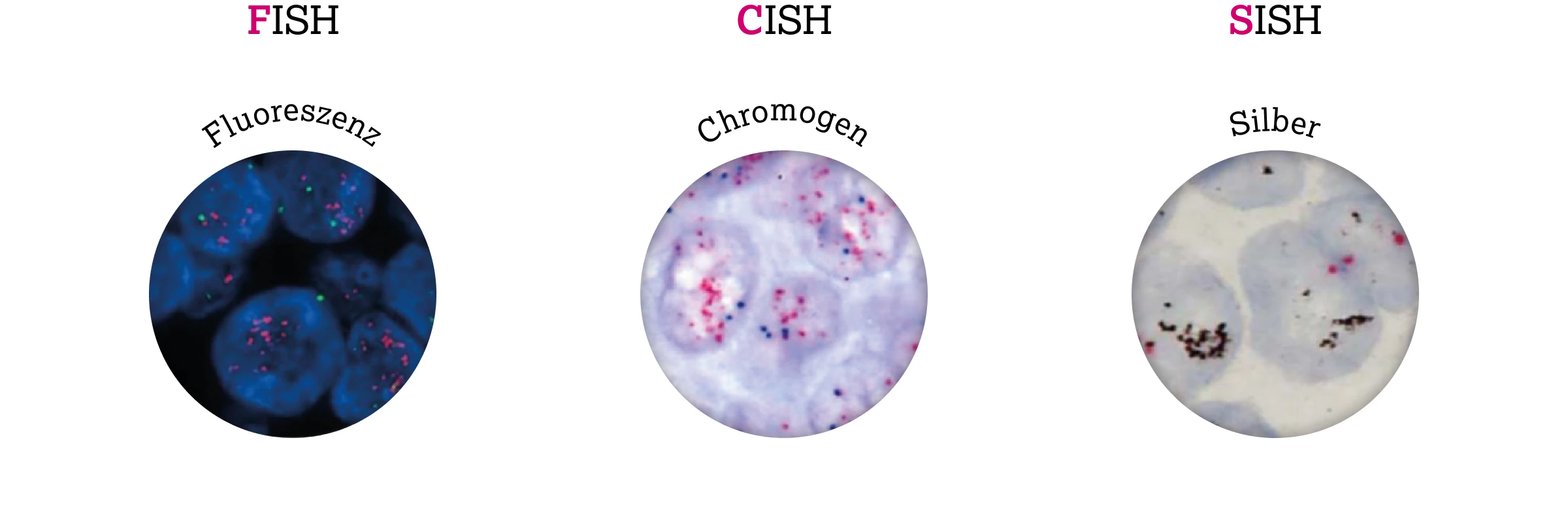
(Bildquellen: F: Sui W, et al. World J Surg Oncol. 2009;7:83.7 C: van de Vijver M, et al. Breast Cancer Res. 2007;9:R68.8 S: Unal B, et al. Asian Pac J Cancer Prev. 2013;14(10):6131-4.9)
Da eine Gen-Amplifikation auch auf einer Polysomie, d. h. einer Vervielfachung des gesamten Chromosoms beruhen kann, wird bei der ISH oftmals noch eine zweite Sonde eingesetzt, die sogenannte Chromosomenzählsonde (Chromosome Enumerating Probe, CEP).10 Diese bindet an die zentrale Verbindungsstelle der beiden Chromatiden des Chromosoms, das Centromer. Bei der HER2 (ERBB2) Testung bindet diese Sonde an die Centromer-Region des Chromosoms 17, auf dem das HER2 (ERBB2) Gen lokalisiert ist. Durch diese duale Markierung werden sowohl das HER2 (ERBB2) Gen als auch das Chromosom 17 (CEP17) identifiziert und quantifiziert. Dadurch ist eine direkte Aussage über den Ploidiegrad parallel zur Bestimmung des HER2 (ERRB2) Amplifikationsstatus möglich.
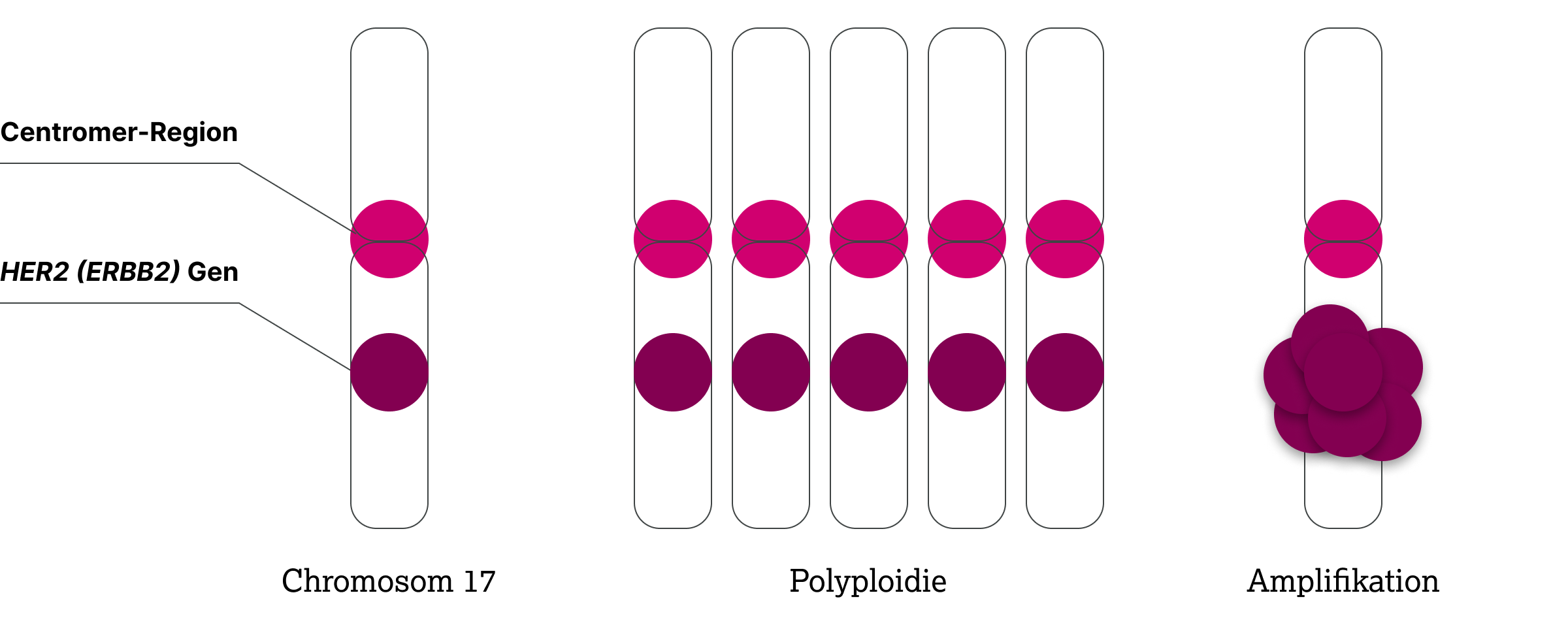
Ein typischer Fall Einsatzfall für eine Doppel-Sonden ISH ist die Analyse der HER2 (ERBB2) Gen-Amplifikation bei Brustkrebspatientinnen, um diejenigen zu ermitteln, die von einer auf HER2 ausgerichteten Therapie tatsächlich profitieren.11 Die ASCO/CAP-Leitlinie empfiehlt zur Bestimmung des HER2-Amplifikationsstatus in IHC 2+ Fällen eine ISH mit zwei Sonden (Dual-Probe-ISH-Assay).2
Präanalytik der HER2-Testung
Die zuverlässige Bestimmung des HER2-Status bei Brustkrebs – einschließlich der Differenzierung in HER2-positiv, HER2-low, HER2-ultralow und HER2-null – erfordert höchste Präzision in allen Phasen der Diagnostik. Fehlerhafte Einstufungen können direkte therapeutische Konsequenzen haben und zu einer Unterversorgung der Patient:innen führen. Daher ist eine besondere Sorgfalt von der Gewebeentnahme über die Fixierung und Aufarbeitung bis hin zur Färbung und Befundung unerlässlich.11,12
Insbesondere der immunhistochemische Nachweis der HER2-Expression ist empfindlich gegenüber präanalytischen Variablen. Faktoren wie die Art und Dauer der Fixierung, die Methoden zur Antigenrückgewinnung, der verwendete Antikörperklon, die enzymatische Aktivität, Reaktionszeiten, Temperaturbedingungen sowie die Substratkonzentration können das Färbebild und damit die Interpretation der Testergebnisse wesentlich beeinflussen. Eine standardisierte, qualitativ hochwertige und reproduzierbare Präanalytik ist daher essenziell für eine valide HER2-Testung und die daraus abgeleiteten therapeutischen Entscheidungen.11,12
- Die HER2-Testung kann sowohl an Stanzbiopsien als auch an Resektionspräparaten erfolgen.2,11,13 Entscheidend ist, dass die Zeit bis zur Fixation und die Fixationsdauer den empfohlenen Standards entsprechen (siehe Probentransport und -aufbereitung).11
- Im Hinblick auf die Therapieplanung wird empfohlen, die primäre Testung vorzugsweise an der Stanzbiopsie vorzunehmen.2,11,13
- Gewebe mit artifiziellen Veränderungen, wie Randartefakten, Retraktionen oder Quetschungen ist von der Beurteilung auszuschließen.11
- Jedes Labor sollte seine Testmethodik validieren, indem die Ergebnisse von Stanzbiopsien und Resektionspräparaten miteinander verglichen werden. Eine hohe Übereinstimmung ist dabei anzustreben (Kappa-Wert ≥ 0,81 bzw. Konkordanz ≥ 95 %).11
- Die Zeitspanne zwischen Gewebeentnahme und Fixation (kalte Ischämiezeit) sollte so kurz wie möglich gehalten werden und 60 Minuten nicht überschreiten.2,11,13 Ist dies nicht realisierbar, muss die Probe durchgehend bei 4 °C gelagert werden, auch während des Transports ins Labor.14
- Größere Gewebeproben sind unmittelbar nach makroskopischer Beurteilung im Abstand von 5–10 mm zu lamellieren (mindestens ein Gewebeblock pro cm Resektatlänge), um eine gleichmäßige und zügige Fixation sicherzustellen und Fixationsgradienten zu minimieren.2,13–15
- Die Fixation sollte in einem ausreichend bemessenen Volumen 10 %igem, neutral gepuffertem Formalin (entspricht ca. 4 % Formaldehyd) erfolgen.2,13–15 Das ideale Verhältnis von Gewebe- zu Fixativvolumen beträgt 1:10,13 mindestens jedoch 1:5.14
- Die minimale Fixationszeit liegt bei 6 Stunden:2,11,13–15
- Stanzbiopsien: optimal 6–72 Std.15
- Resektate: optimal 12–72 Std.15
- Nach 24 Stunden sollte das Fixativ durch eine frische Formalinlösung ersetzt werden.14
- Die Überschreitung einer Fixationszeit von > 72 Stunden ist zu vermeiden, da sie zu unspezifischer Hintergrundfärbung führen kann, aber auch die Antigen-Rückgewinnung verschlechtern und damit zum Verlust immunhistochemischer Signalqualität führen kann.14
- Die Fixation kann bei Raumtemperatur (15–25 °C) 16
- Das Vorwärmen des Formalins kann zwar die Fixationsgeschwindigkeit steigern, erhöht jedoch auch das Risiko der Autolyse. Zudem kann sich eine äußere Fixationsschicht („Fixierschale“) bilden, die das Eindringen des Fixativs in tiefere Gewebeschichten behindert.13,14
- Eine primäre Fixation mit Kühlung kann autolytische Prozesse verlangsamen, hemmt jedoch auch die Fixierung insgesamt. Ein zu frühes Abkühlen im Fixiermedium kann zu unzureichender Fixierung führen.13,14
- Nach der Fixierung werden die Gewebe in einer Alkoholreihe mit aufsteigender Konzentration dehydriert, gefolgt von Xylol. Anschließend werden die Proben mit geschmolzenem Paraffin (≤ 60 °C) infiltriert.16
- Ordnungsgemäß fixiertes und eingebettetes Gewebe ist vor dem Schneiden und Aufbringen auf Objektträger unbegrenzt haltbar hinsichtlich der (HER2-)Proteinexpression, wenn es bei 15–25 °C gelagert wird.16
- Für formalinfixiertes, in Paraffin eingebettetes Gewebe (FFPE) wird eine Schnittdicke von 4–5 μm empfohlen.16
- Die Färbung sollte je nach Testsystem zeitnah nach dem Schneiden erfolgen:
- PATHWAY® anti-HER-2/neu (4B5): innerhalb von 1–2 Tagen17
- HercepTest™ mAb pharmDx (Dako Omnis): innerhalb von 4–6 Wochen16
Schnitte, die älter als 6 Wochen sind, sollten nicht mehr für eine HER2-Färbung verwendet werden.2
- Eine übermäßige Trocknung der Schnitte kann zu einem Verlust des HER2-Antigens führen.14 Daher wird eine Trocknung empfohlen:
- bei 60 °C für 1 Stunde oder
- bei 37 °C über Nacht oder
- bei Raumtemperatur für mindestens 12 Stunden.14,16
- Vor der Färbung müssen die Gewebeschnitte entparaffiniert und anschließend rehydriert werden.
- Die Färbemethode, aber insbesondere die Antigen-Rückgewinnung sowie die Verwendung unterschiedlicher Antikörperklone mit variierender Spezifität, können die Genauigkeit und Reproduzierbarkeit der Ergebnisse maßgeblich beeinflussen. Dies kann die Identifikation von HER2-low oder HER2-ultralow Expressionen erschweren.18
- Zur Sicherstellung der Validität und Reproduzierbarkeit der HER2-Analyse werden standardisierte Testkits empfohlen. Die Durchführung sollte dabei strikt gemäß den Herstellerangaben erfolgen.11
- Für kommerzielle Testsysteme wie PATHWAY® anti-HER-2/neu (4B5) von Ventana und HercepTest™ mAb pharmDx von Dako wird der Einsatz validierter Färbeautomaten und abgestimmter Protokolle empfohlen.16,17
- Der Nachweis einer HER2-Genamplifikation erfolgt mittels In-situ-Hybridisierung (ISH). Dabei stehen verschiedene Verfahren zur Verfügung:
- FISH: fluoreszenzbasierte ISH
- CISH: chromogene ISH
- SISH: silberverstärkte ISH
Auch hier gelten hohe Anforderungen an die Qualitätssicherung in der Routinediagnostik. Bei Einsatz von Testkits ist die Anwendung ausschließlich gemäß Herstellerprotokoll durchzuführen.11
- Studien zeigen, dass die Entkalkung von Knochengewebe die Genauigkeit der HER2-Bestimmung mittels IHC beeinträchtigen kann.19,20 Bislang existiert kein standardisiertes Entkalkungsprotokoll, das als Goldstandard für die anschließende IHC anerkannt ist.21
- Für die Bestimmung des HER2-Status in Knochenmetastasen wird daher bevorzugt die In-situ-Hybridisierung (ISH) empfohlen.22,23
- Die Entkalkung mit Ethylendiamintetraessigsäure (EDTA) hat sich als geeignete Methode für die HER2 FISH-Analyse erwiesen.24,25
- Eine aktuelle Studie ergab, dass eine 10 %ige Ameisensäure keinen negativen Einfluss auf die HER2 IHC-Färbung hatte.26 Die Autor:innen schlussfolgern, dass eine Ameisensäure-Entkalkung prinzipiell zur Beurteilung von HER2-positivem sowie HER2-low Status geeignet sein könnte.26
Nachweis von HER2 (ERBB2) Mutationen
Der Nachweis aktivierender HER2 (ERBB2) Mutationen kann mittels Next-Generation-Sequencing (NGS) oder Polymerase-Kettenreaktion (PCR) erfolgen. Gemäß der aktuellen S3-Leitlinie zur Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms sollen alle Patient:innen mit NSCLC Stadium IV vor der Erstlinientherapieentscheidung eine umfassende NGS-basierte Molekulardiagnostik erhalten.27 Dabei wird u. a. auch die Testung auf HER2 (ERBB2) Mutationen in den Exonen 8, 18, 19, 20 und 21 empfohlen.27
Abkürzungen
ASCO: American Society of Clinical Oncology; CAP: College of American Pathologists; CEP: Chromosome Enumerating Probe; CISH: chromogene In-situ-Hybridisierung; DNA: Desoxyribonukleinsäure; EDTA: Ethylendiamintetraacetat; ERBB2: v-erb-b2 erythroblastic leukemia viral oncogene homolog; FFPE: formalinfixiert, paraffineingebettet; FISH: Fluoreszenz-in-situ-Hybridisierung; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2 (Gen); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2 (Protein); IHC: Immunhistochemie; ISH: In-situ-Hybridisierung; mAb: monoklonaler Antikörper; NGS: Next-Generation-Sequencing; NSCLC: nicht-kleinzelliges Lungenkarzinom; PCR: Polymerase-Kettenreaktion; SISH: silberverstärkte In-situ-Hybridisierung
- Oh D-Y, et al. Nat Rev Clin Oncol 2020;17(1):33–48.
- Wolff AC, et al. J Clin Oncol 2023;41(22):3867-72.
- Wolff AC, et al. J Clin Oncol 2018;36(20):2105–22.
- Nicolò E, et al. J Liq Biopsy 2023;2:100117.
- Horimoto Y, et al. BMC Cancer 2022;22(1):242.
- Rehman ZU, et al. Diagnostics (Basel) 2024;14(18):2089.
- Sui W, et al. World J Surg Oncol 2009;7:83.
- van de Vijver M, et al. Breast Cancer Res 2007;9(5):R68.
- Unal B, et al. Asian Pac J Cancer Prev 2013;14(10):6131–4.
- Varga Z, et al. Kompass Onkol 2024;11(2):63–75.
- S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 5.0, Dez 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mammakarzinom_4_0/Version_5/LL_Mammakarzinom_Langversion_5.0.pdf. Letzter Zugriff: Februar 2026.
- Tarantino P, et al. Ann Oncol 2023;34(8):645–59.
- IQTIG – Institut für Qualitätssicherung und Transparenz im Gesundheitswesen. Berlin; 2021. Verfügbar unter iqtig.org/downloads/auswertung_begleitschreiben/IQTIG_Qualitaetsaspekte-der-HER2-Bestimmung-im-Rahmen-der-esQS_V1.4_Fragenkatalog_2021-01-05.pdf. Letzter Zugriff: Februar 2026.
- The Royal College of Pathologists of Australasia. Guideline: Fixation of Tissues. Verfügbar unter rcpa.edu.au/Manuals/Macroscopic-Cut-Up-Manual/General-information/Fixation. Letzter Zugriff: Februar 2026.
- Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.V. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlungen 2025.1D. Kapitel xy. Verfügbar unter https://www.ago-online.de/leitlinien-empfehlungen/leitlinien-empfehlungen/kommission-mamma. Letzter Zugriff: Februar
- Agilent DAKO. HercepTest™ Interpretation Manual Breast Cancer. Verfügbar unter agilent.com/cs/library/usermanuals/public/28630_herceptest_interpretation_manual-breast_ihc_row.pdf. Letzter Zugriff: Februar 2026.
- Roche VENTANA. PATHWAY anti-HER-2/neu (4B5) Rabbit Monoclonal Primary Antibody Interpretation Guide for Breast Cancer. Verfügbar unter accessdata.fda.gov/cdrh_docs/pdf/P990081S047D.pdf. Letzter Zugriff: Februar 2026.
- Sajjadi E, et al. Cancer Drug Resist 2022;5(4):882–8.
- Schrijver WAME, et al. Mod Pathol 2016;29(12):1460–70.
- Darvishian F, et al. Breast J 2011;17(6):689–91.
- Grassini D, et al. Pathobiology 2022;89(5):278–96.
- Rakha EA, et al. J Clin Pathol 2023;76(4):217–27.
- Penault-Llorca F, et al. Breast 2013;22(2):200–2.
- van Es SC, et al. Am J Surg Pathol 2019;43(10):1355–60.
- Washburn E, et al. Hum Pathol 2021;117:108–14.
- Tsirka A, et al. Cancer Research 2023;83(5_Supplement):P6-04-17-P6-04-17.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: Februar 2026.

