Was ist HER2 und welche Funktion hat es?
Der humane epidermale Wachstumsfaktor-Rezeptor 2 (HER2) ist ein transmembraner Tyrosinkinase-Rezeptor, der auf der Oberfläche vieler normaler Zellen in niedriger Konzentration exprimiert wird und eine zentrale Rolle bei der Regulation von Zellproliferation, Zelladhäsion und Zelldifferenzierung spielt.1,2 Die Aktivierung von HER2 führt zur Dimerisierung mit anderen HER-Familienmitgliedern, wodurch intrazelluläre Signalwege (wie PI3K/AKT und RAS/MAPK) aktiviert werden.3 Diese steuern die Expression von Genen, die an Wachstum und Überleben der Zelle beteiligt sind. Aufgrund dieser Funktionen wird HER2 als Protoonkogen klassifiziert.2 Das HER2-Protoonkogen liegt auf dem langen Arm des Chromosoms 17, genauer gesagt in der Region 17q12–21, in direkter Nachbarschaft zum BRCA1-Gen.1
Bekannte Synonyme für das Gen HER2 sind unter anderem: ERBB2, HER-2/neu, NEU, CD340, NGL, VSCN2, MLN-19, c-erbB-2.1
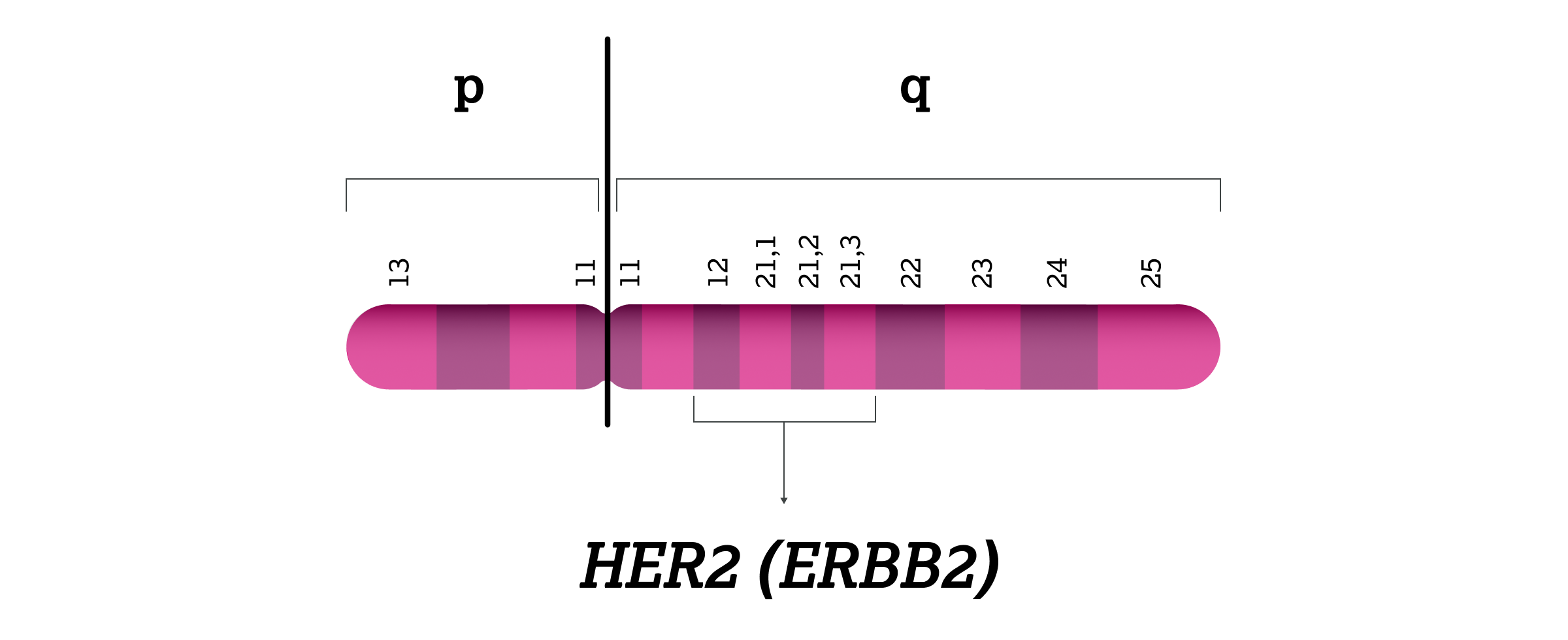
HER-Rezeptorfamilie
HER2 ist ein Mitglied der Familie der humanen epidermalen Wachstumsfaktor-Rezeptoren (HER), zu der HER1 (auch bekannt als ERBB1 oder EGFR), HER2 (ERBB2), HER3 (ERBB3) und HER4 (ERBB4) gehören.2 Diese Familie wird auch als ERBB-Familie bezeichnet.2 Im Gegensatz zu den anderen Familienmitgliedern besitzt HER2 keinen bekannten Liganden und fungiert bevorzugt als Dimerisierungspartner für andere HER-Rezeptoren. Bei Überexpression kann HER2 auch spontan Homodimere bilden und dadurch ligandenunabhängig die nachgeschalteten Signalwege aktivieren.2
Molekulare Struktur von HER2
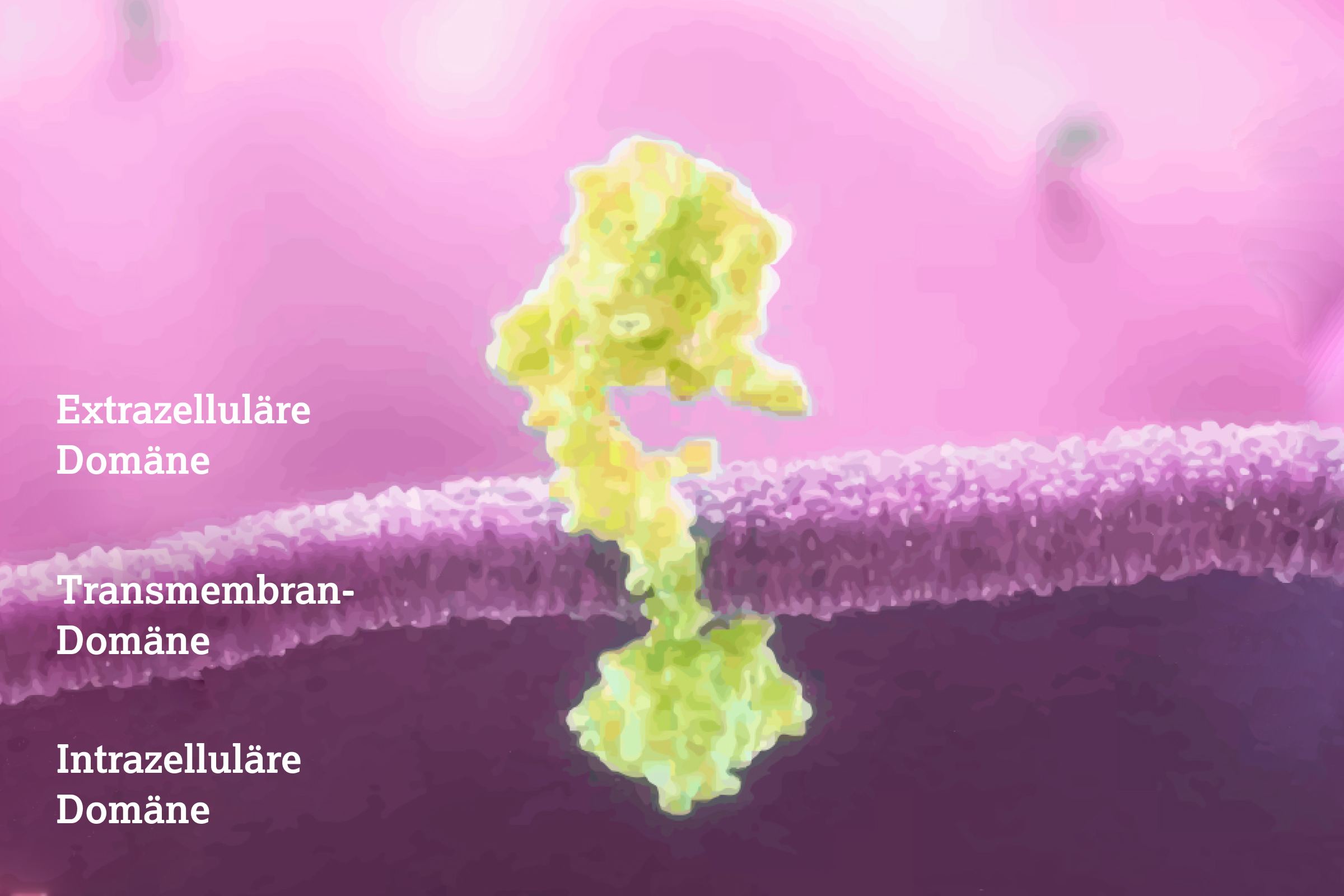
Alle HER-Rezeptoren besitzen gemeinsame strukturelle Merkmale, darunter eine extrazelluläre Domäne, eine Transmembran-Domäne sowie eine intrazelluläre Domäne mit Tyrosinkinase-Aktivität.2
Die extrazelluläre Domäne von HER2 weist eine konstitutiv aktive Konformation auf, die die Dimerisierung mit anderen HER-Rezeptoren begünstigt.
Aktivierung und Signalwege
Die Rezeptoraktivierung von HER1, HER3 und HER4 erfolgt durch Bindung spezifischer extrazellulärer Liganden (z. B. EGF, Neuregulin). Diese Ligandenbindung induziert eine Konformationsänderung, die zur Dimerisierung mit anderen Mitgliedern der HER-Familie führt.5 Die Dimerbildung aktiviert die intrazelluläre Tyrosinkinase-Domäne, wodurch Autophosphorylierung an Tyrosinresten erfolgt.6 Diese Phosphorylierung dient als Andockstelle für Adapterproteine, die Signalkaskaden wie PI3K/AKT oder RAS/MAPK initiieren.3 Über diese Wege werden schließlich Transkriptionsfaktoren (z. B. MYC, STAT) aktiviert, die Gene für Zellproliferation, -adhäsion und -differenzierung regulieren.7,8
HER2 nimmt hierbei eine Sonderrolle ein
Ligandenunabhängige Aktivierung
Bei ausreichender Oberflächenexpression dimerisiert HER2 spontan – sowohl als Homodimer (HER2–HER2) als auch als Heterodimer mit anderen HER-Rezeptoren.6
Bevorzugter Dimerisierungspartner
HER2 bildet die stabilsten Komplexe mit HER3 und HER1.5 Diese Heterodimere zeigen eine höhere Signalaktivität als andere Kombinationen.9
Synergie mit HER3
Da HER3 keine funktionelle Tyrosinkinase-Domäne besitzt, ist es auf die Phosphorylierung durch HER2 angewiesen. Dies erklärt die starke onkogene Wirkung des HER2/HER3-Dimers in Tumoren.2
Cross-Aktivierung
HER2 kann auch mit Nicht-HER-Rezeptoren (z. B. MET, IGF1R) dimerisieren und so alternative Signalwege aktivieren.8
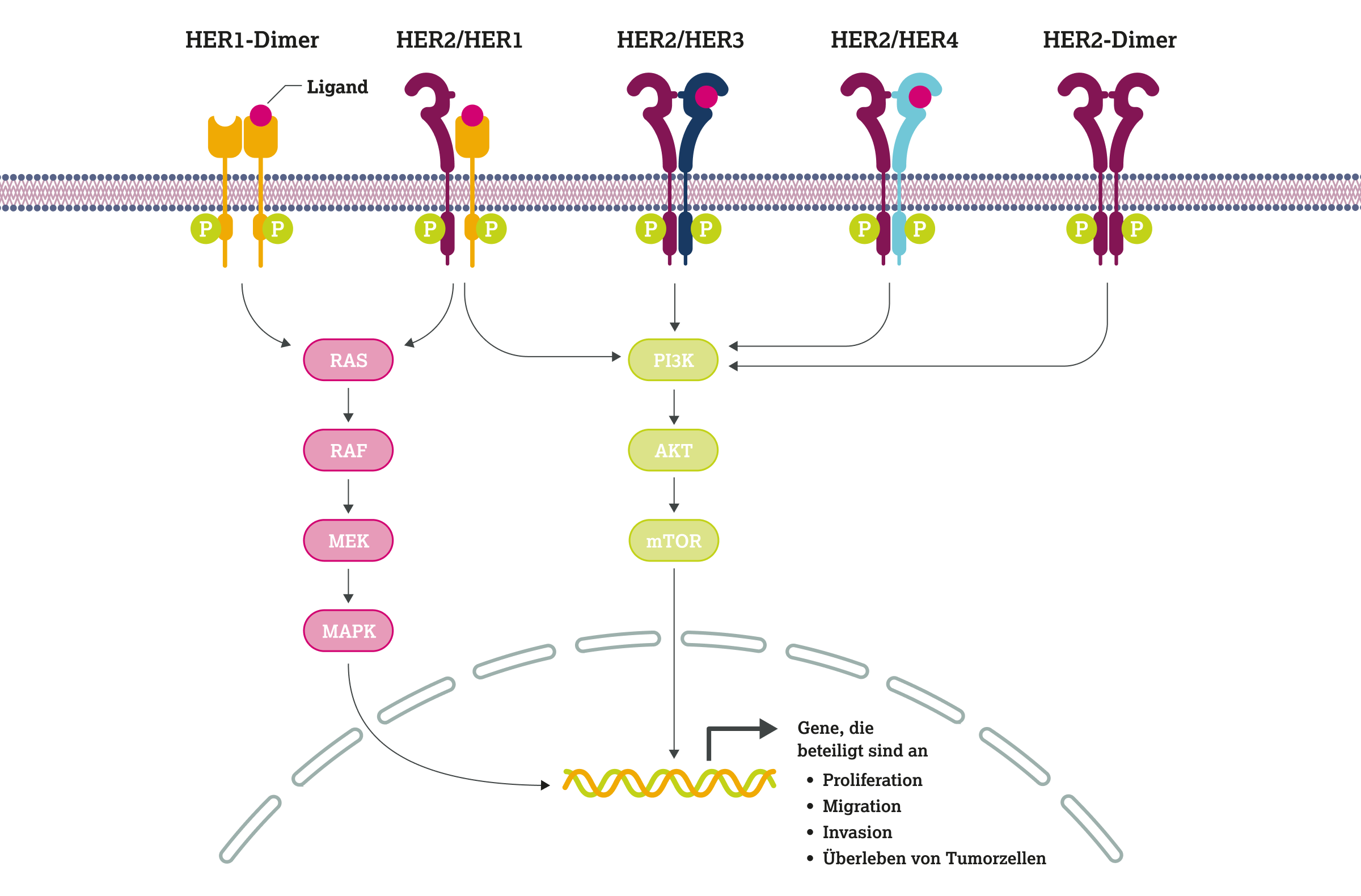
Die Bindung von Liganden an die extrazelluläre Domäne des HER2-Rezeptors stabilisiert die Dimerisierung zwischen HER2 und einem anderen Mitglied der HER-Rezeptorfamilie (HER1, HER2, HER3 und HER4). Durch Transphosphorylierung von Tyrosinresten in den intrazellulären Domänen stimulieren die aktiven Homo- oder Heterodimere anschließend verschiedene Signalwege wie den PI3K/AKT- und/oder den RAS/MAPK-Weg. Diese nachgeschalteten Signalkaskaden führen zur Transkription von Genen, welche die Proliferation, Migration, Invasion und das Überleben von Tumorzellen steuern.9
Verschiedene HER2-Signalwege bei verschiedenen Tumoren
Bei HER2-positiven Brustkrebszellen bspw. führt die Überexpression von HER2 zur ligandenunabhängigen Dimerisierung des Rezeptors und somit zu unkontrollierter Tumorzellproliferation und -progression.11 Welcher Signalweg favorisiert wird, hängt dabei u. a. von der Zusammensetzung des HER2-Dimers, aber auch vom zellulären Kontext ab. Beim Mammakarzinom dominiert typischerweise der PI3K/AKT-Signalweg, während in anderen Tumorentitäten wie Lungen-, Ovarial- und Magenkarzinomen vorwiegend der MAPK/ERK-Signalweg aktiviert wird. Diese kontextabhängigen Unterschiede können die Wirksamkeit HER2-gerichteter Therapien beeinflussen und sollten bei der Entwicklung indikationsspezifischer Behandlungsstrategien berücksichtigt werden.12
Abkürzungen
AKT: Proteinkinase B; BRCA1: Breast Cancer 1; CC: Creative Commons; CD340: cluster of differentiation 340 (Synonym für HER2); EGF: epidermaler Wachstumsfaktor; EGFR: epidermaler Wachstumsfaktor-Rezeptor (HER1); ERBB: v-erb-b2 erythroblastic leukemia viral oncogene homolog (Synonym für HER); HER: humaner epidermaler Wachstumsfaktor-Rezeptor; IGF1R: Insulin-like growth factor 1 receptor; MAPK: mitogen-aktivierte Proteinkinase; MEK: MAPK/ERK-Kinase; MLN-19: metastatic lymph node gene 19 (Synonym für HER2); MET: mesenchymal-epithelial transition factor; mTOR: mechanistic target of rapamycin; MYC: Myelocytomatosis Transkriptionsfaktor; NEU: Neuroblastom-Onkogen (Synonym für HER2); NGL: Neuroblastoma or Glioblastoma-derived Oncogene Homolog (Synonym für HER2); PI3K: Phosphatidylinositol-3-Kinase; RAF: rapidly accelerated fibrosarcoma; RAS: rat sarcoma; STAT: Signal Transducer and Activator of Transcription; VSCN2: visceral neuropathy-2 (Synonym für HER2)
- NIH National Library of Medicine (2025). ERBB2 erb-b2 receptor tyrosine kinase 2 [Homo sapiens (human)]. Verfügbar unter www.ncbi.nlm.nih.gov/gene/2064. Letzter Zugriff: August 2025.
- Albagoush SA, et al. (2025). Tissue Evaluation for HER2 Tumor Marker. Verfügbar unter www.ncbi.nlm.nih.gov/books/NBK537134/. Letzter Zugriff: August 2025.
- Sareyeldin RM, et al. Cancers (Basel) 2019;11(5):646.
- Zhang W, et al. Int J Mol Sci 2011;12(9):5672–83.
- Hart V, et al. Oncotarget 2020;11(46):4338–57.
- Schlam I, et al. NPJ Breast Cancer 2021;7(1):56.
- Baraibar I, et al. Crit Rev Oncol Hematol 2020;148:102906.
- Gutierrez C, et al. Arch Pathol Lab Med 2011;135(1):55–62.
- Gerson JN, et al. Expert Opin Investig Drugs 2017;26(5):531–40.
- Miri A, et al. Cent Asian J Medical Pharm Sci Innov 2021;3:114–30.
- Slamon DJ, et al. N Engl J Med 2001;344(11):783–92.
- Kirouac DC, et al. PLoS Comput Biol 2016;12(4):e1004827.




