HER2 beim Mammakarzinom
Bedeutung und Prävalenz von HER2 beim Mammakarzinom
Der Biomarker HER2 spielt eine zentrale Rolle in der Diagnostik und Therapie des Mammakarzinoms. Lange Zeit wurde hinsichtlich der HER2-Proteinexpression klinisch nur zwischen HER2-positiv und HER2-negativ unterschieden.1 Bis zu ~85 % der Brustkrebstumoren galten damit als HER2-negativ und waren von HER2-gerichteten Therapien ausgeschlossen.2 In den letzten Jahren hat sich jedoch ein differenzierteres Verständnis der HER2-Expression durchgesetzt. Neue immunhistochemische Kategorien wie HER2-low und HER2-ultralow erweitern das diagnostische Spektrum und sind wichtig, um geeignete Therapieentscheidungen zu treffen.3,4
Die klinische HER2-Klassifikation umfasst heute ein Kontinuum von HER2-positiv über HER2-low und HER2-ultralow bis hin zu HER2-null.3,4
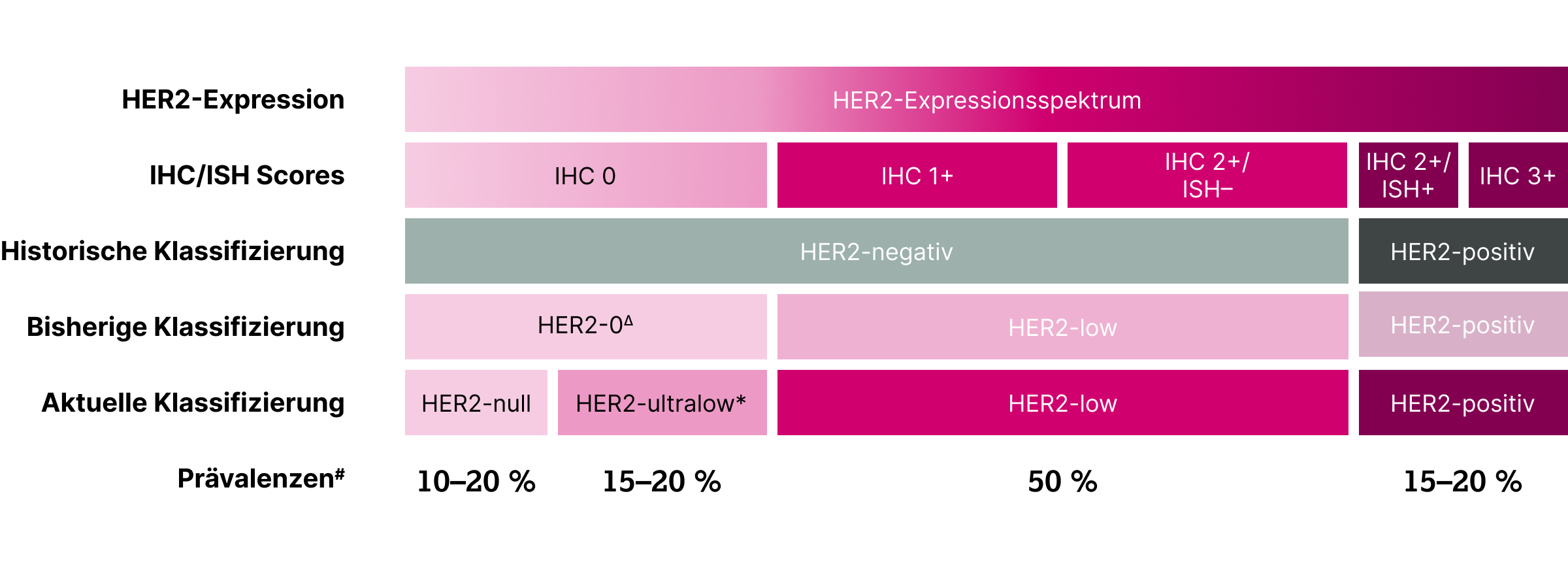
Etwa 50 % der historisch als HER2-negativ eingestuften Mammakarzinome weisen einen HER2-low Status auf; die Prävalenz von HER2‑ultralow Brustkrebs wird mit 15–20 % veranschlagt.5–14
*Der HER2-ultralow Status ist aktuell nur beim inoperablen oder metastasierten hormonrezeptorpositiven Brustkrebs von therapeutischer Relevanz.14
# Die angegebenen Prävalenzen wurden aus publizierten Werten der Quellen 5–14 berechnet.
Δ HER2-0 wird manchmal auch als HER2-zero bezeichnet.12
Wie sind HER2-low und HER2-ultralow definiert?
HER2-low Brustkrebs wird vom ESMO-Expert:innen-Panel in einem Consensus Statement definiert als IHC 1+, also schwache, partielle Membranfärbung bei > 10 % der Tumorzellen, oder IHC 2+/ISH–, also schwache, komplette Membranfärbung bei > 10 % der Tumorzellenmit negativem Ergebnis in der In-situ-Hybridisierung.3 Das heißt, es handelt sich dabei um Tumoren, die eine gewisse Überexpression des HER2-Proteins aufweisen, welche jedoch nicht auf eine HER2 (ERBB2) Genamplifikation zurückzuführen ist.3
HER2-ultralow Brustkrebs wird definiert als IHC 0 mit Membranfärbung, also schwacher, partieller Membranfärbung bei ≤ 10 % der Tumorzellen.3 Das bedeutet, dass schon ab der ersten Tumorzelle mit Membranfärbung ein HER2-ultralow Status vorliegt.
Die Unterscheidung dieser Subgruppen erfordert eine präzise immunhistochemische Beurteilung. Besonders die Differenzierung zwischen HER2-low, HER2-ultralow und HER2-null ist anspruchsvoll, aber für eine adäquate Therapieentscheidung von großer Bedeutung.16
Studien und Leitlinien-Empfehlungen zur HER2-Testung beim Mammakarzinom
Die von der American Society of Clinical Oncology mit dem College of American Pathologists herausgegebenen ASCO/CAP-Leitlinien dienen als Grundlage für die HER2-Diagnostik beim Mammakarzinom.17,18
Etablierter HER2 Scoring-Algorithmus – neue Interpretation
Der HER2 Scoring-Algorithmus zur Bewertung des HER2-Status beim Mammakarzinom gemäß ASCO/CAP-Leitlinien ist seit Jahren etabliert.17,18 Allerdings sind Patholog:innen angesichts der klinischen Relevanz von Tumoren mit geringer und minimaler HER2-Überexpression (HER2-low bzw. HER2-ultralow) nun gefordert, im unteren Teil des HER2-Spektrums (zwischen IHC 0, IHC 1+ bzw. 2+/ISH–) noch präziser und reproduzierbarer zu unterscheiden.16,19 Eine der größten Herausforderungen dabei liegt in der Variabilität und Empfindlichkeit der derzeitigen Testmethoden.19 Die ASCO/CAP-Leitlinie aus dem Jahr 2023 hat dieses Problem erkannt und bietet Empfehlungen für die klinische Praxis zur Unterscheidung von HER2 IHC 0 und IHC 1+.17
Insbesondere die digitale Pathologie bietet die Möglichkeit, mittels KI-gestützter Bildanalyse einen repräsentativen Biomarker-Score auf Basis aller Tumorzellen im gesamten Probenmaterial auf einem Objektträger zu bestimmen und damit sowohl die Tumorheterogenität bestmöglich abzudecken als auch wenige gefärbte Zellen sicher zu erfassen.

Der hier abgebildete HER2 Scoring-Algorithmus zeigt die aktuelle klinische Interpretation in HER2-null, HER2-ultralow und HER2-low.3,4
Wichtiger Hinweis: Die Einführung von HER2-low und HER2-ultralow ändert für die Pathologie nichts an der praktischen Auswertung nach der etablierten ASCO/CAP-Leitlinie in Bezug auf die Bestimmung des IHC-Scores und ggf. des ISH-Status. Was sich jedoch ändert, ist die klinische Interpretation. Die Arbeitsgemeinschaft Gynäkologische Onkologie e.V. (AGO)20 und die European Society For Medical Oncology (ESMO)21 haben das HER2-low und das HER2-ultralow Konzept in ihre Brustkrebsleitlinien integriert.
Empfehlungen zum pathologischen Befundbericht
Die Ergebnisse der HER2-Testung sollten möglichst detailliert aufgeführt werden, um eine fundierte Therapieentscheidung zu ermöglichen. Folgende Angaben sollten enthalten sein:
Detaillierter IHC-Score (0, 1+, 2+, 3+)3,16,17
ISH-Status (HER2 amplifiziert/nicht amplifiziert)3,17
Anteil der Tumorzellen [%] mit Membranfärbung bei IHC 022–24
Klinischer HER2-Status (HER2-null, HER2-ultralow, HER2-low oder HER2-positiv)20,23
Das CAP HER2 Biomarker Reporting Template23 und die AGO20 empfehlen, Brustkrebs mit IHC 1+ oder IHC 2+/ISH– im Befund als "HER2-low" zu kennzeichnen.
Analog sollte bei IHC 0 mit Membranfärbung (ab der ersten Tumorzelle) für Brustkrebs im Befund "HER2-ultralow" mit angegeben werden.3 Eine enge Abstimmung zwischen Behandler:innen und Patholog:innen ist wichtig, um sicherzustellen, dass die Konzepte HER2-low und HER2-ultralow in der Diagnostik und im Pathologiebericht angemessen berücksichtigt werden. Diese detaillierte Klassifizierung ermöglicht eine präzisere Patientenidentifikation für innovative Behandlungsansätze.
Leitlinienempfehlungen zur HER2 (Re-)Testung
Bei allen neu diagnostizierten Patient:innen mit Brustkrebs soll ein HER2-Test durchgeführt werden. Bei Patient:innen, die eine metastasierende Erkrankung entwickeln, soll ein HER2-Test an einer Metastase durchgeführt werden, sofern eine Gewebeprobe verfügbar ist.17
IHC und ISH sind die wichtigsten Methoden zur Beurteilung des HER2-Status bei Brustkrebs.17
Beim metastasiertem Mammakarzinom sollte die Biopsie bevorzugt an einer Metastase durchgeführt werden, um den HER2-Rezeptorstatus zu bestimmen.20
Bei einem bereits vorliegenden HER2-0 (IHC 0) Status kann eine Nachbestimmung des HER2-Status sinnvoll sein, um zu schauen, ob nicht eigentlich ein HER2-ultralow Status vorliegt.20
Bei Patient:innen mit neu diagnostiziertem oder rezidivierendem metastasiertem Mammakarzinom sollte eine Biopsie der Metastase durchgeführt werden, um die Histologie zu bestätigen und erneut den Hormonrezeptor- und HER2-Status zu bestimmen.21,25
Bei signifikanten Unterschieden im Östrogenrezeptor(ER)/Progesteronrezeptor(PR)- und HER2-Status zwischen Primärtumor und Rezidiv sollten die Patient:innen entsprechend dem Rezeptorstatus der Rezidivbiopsie behandelt werden.25
Weitere therapeutisch relevante Biomarker, die im Rahmen der klinischen Routine untersucht werden sollten, sind
- bei HER2-negativem metastasiertem Brustkrebs (mBC): HER2-low Status durch IHC/ISH, gBRCA1/2 und gPALB2-Mutationsstatus21
- bei TNBC: PD-L1 Status21
- bei HR+ HER2-negativem mBC: HER2-ultralow Status durch IHC und Mutationsstatus von PIK3CA, AKT1/PTEN und ESR1 (nach AI-Behandlung).21
Beim invasiven Mammakarzinom sollen in der Primärdiagnostik der Östrogen- und Progesteronrezeptorstatus sowie der HER2-Status bestimmt werden, vorzugsweise bereits an der Stanzbiopsie.24
Bei Verdachtsdiagnose eines lokoregionären Rezidivs soll zunächst eine histologische Sicherung mit erneuter Bestimmung von ER, PR und HER2 und ein komplettes Re-Staging erfolgen.24
Die HER2-Expression bei Brustkrebs ist dynamisch
Studien haben gezeigt, dass die HER2-low Expression bei Brustkrebs sehr dynamisch ist, wobei ein Teil der HER2-0 Tumoren zu HER2-low Tumoren wird und umgekehrt, z. B. bei einer Resterkrankung nach neoadjuvanter Therapie26 oder nach einem Rezidiv des Tumors.26–28
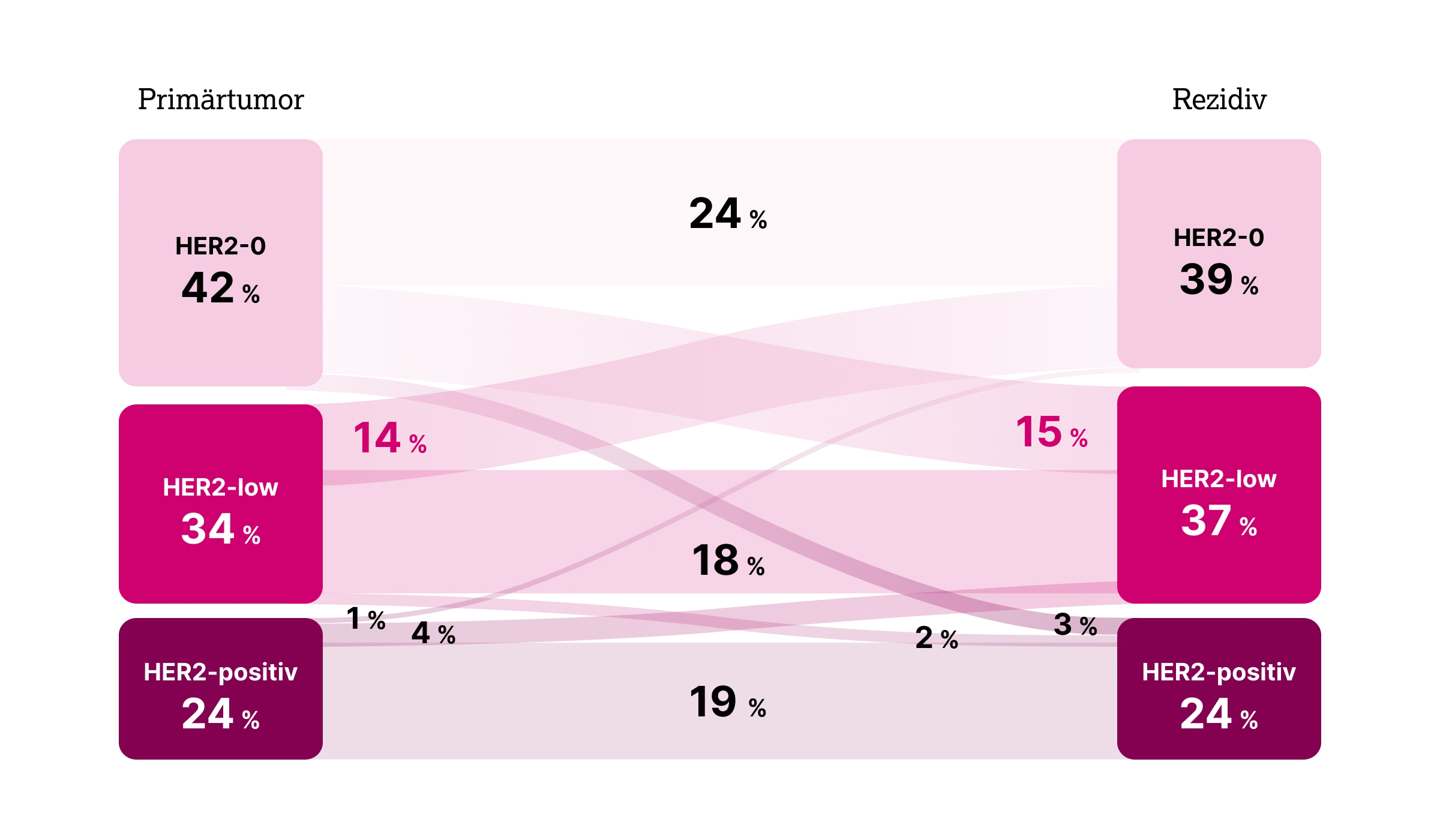
In einer Kohorte von 547 Brustkrebspatient:innen wurde bei ca. 38 % eine Änderung des HER2-Status zwischen Primärtumor und Rezidiv festgestellt. Am häufigsten, in 15 % der Fälle, war ein Wechsel von HER2-0 zu HER2-low zu beobachten und bei 14 % von HER2-low zu HER2-0.27 Der HER2-positive Phänotyp bei primärem und rezidiviertem Brustkrebs änderte sich am wenigsten; in nur ca. 5 % der Fälle kam es zu einer Verringerung oder einer Zunahme der HER2-Expression.27
Diese Dynamik ist wahrscheinlich auf mehrere Faktoren zurückzuführen. So kann die HER2-Expression durch verschiedene Stimuli innerhalb der Tumormikroumgebung sowie durch die Auswirkungen einer vorherigen Behandlung moduliert werden.29 Auch präanalytische und analytische Herausforderungen bei der HER2-Testung können zu einer hohen Diskordanz bei der Beurteilung führen.29
Unabhängig von den beteiligten Faktoren unterstreicht diese Beobachtung die Notwendigkeit, den HER2-Status im Krankheitsverlauf der Patient:innen neu zu bewerten, selbst wenn der Tumor bei einer vorherigen Biopsie HER2-0 war, und es empfiehlt sich, die HER2-Testung möglichst am neuesten Probenmaterial durchzuführen und Biopsien Resektaten vorzuziehen.29,30
Abkürzungen:
ADC: Antikörper-Wirkstoff-Konjugat; AGO: Arbeitsgemeinschaft Gynäkologische Onkologie e.V.; AKT1: Serin/Threonin-Kinase AKT 1 (Gen); ASCO: American Society of Clinical Oncology; BRCA1: Breast Cancer Associated Gene 1; BRCA2: Breast Cancer Associated Gene 2; CAP: College of American Pathologists; ER: Östrogenrezeptor; ERBB: v-erb-b2 erythroblastic leukemia viral oncogene homolog; ESMO: European Society for Medical Oncology; ESR1: Östrogenrezeptor 1 (Gen); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; IHC: Immunohistochemie; ISH: In-situ-Hybridisierung; KI: Konfidenzintervall; PALB2: Partner and Localizer of BRCA2 (Gen); PD-L1: Programmed cell death ligand-1; PIK3CA: Phosphoinositid-3-Kinase katalytische Untereinheit alpha (Gen); PR: Progesteronrezeptor; PTEN: Phosphatase- und Tensin-Homolog (Gen); PTEN: Phosphatase- und Tensin-Homolog (Protein); TNBC: triple-negatives Mammakarzinom
- Wolff AC, et al. Arch Pathol Lab Med 2014;138(2):241–56.
- Tarantino P, et al. J Clin Oncol 2020;38(17):1951–62.
- Tarantino P, et al. Ann Oncol 2023;34(8):645–59.
- Venetis K, et al. Front Mol Biosci 2022;9:834651.
- Rüschoff J, et al. Mod Pathol 2017;30(2):217–26.
- Schettini F, et al. NPJ Breast Cancer 2021;7(1):1–13.
- Viale G, et al. ESMO Open 2023;8(4):1–11.
- Peiffer DS, et al. JAMA Oncol 2023;9(4):500–10.
- Hein A, et al. Eur J Cancer 2021;155:1–12.
- Untch et al. Colloquium Senologie 2023/2024. 1. Aufl. München: Lukon; 2023.
- Denkert C, et al. Lancet Oncol 2021;22(8):1151–61.
- Chen Z, et al. Breast Cancer Res Treat 2023;202(2):313–23.
- Mehta S, et al. J Clin Oncol 2024;42(16_suppl):e13156-e13156.
- Bardia A, et al. N Engl J Med 2024(391):2110–22 inkl. Supplement.
- Curigliano G, et al. ESMO Open 2024;9(4):102989.
- Ivanova M, et al. Virchows Arch 2024;484(1):3–14.
- Wolff AC, et al. J Clin Oncol 2023;41(22):3867-72.
- Wolff AC, et al. Arch Pathol Lab Med 2018;142(11):1364–82.
- Rüschoff J, et al. Arch Pathol Lab Med 2025;149(5):431–8.
- Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.V; Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlungen 2025.1D. Verfügbar unter https://www.ago-online.de/leitlinien-empfehlungen/leitlinien-empfehlungen/kommission-mamma. Letzter Zugriff: Februar 2026.
- ESMO Metastatic Breast Cancer Living Guideline, v1.2 April 2025; Verfügbar unter esmo.org/guidelines/living-guidelines/esmo-living-guideline-metastatic-breast-cancer/diagnosis-and-staging/biopsy-of-metastatic-lesion-to-confirm-diagnosis. Letzter Zugriff: Februar 2026.
- Denkert C, et al. Pathologie (Heidelb) 2023;44(Suppl 2):53–60.
- College of American Pathologists (März 2025). Cancer Protocol Templates. Verfügbar unter cap.org/protocols-and-guidelines/cancer-reporting-tools/cancer-protocol-templates. Letzter Zugriff: September 2025.
- S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 5.0, Dezember 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mammakarzinom_4_0/Version_5/LL_Mammakarzinom_Langversion_5.0.pdf. Letzter Zugriff: Februar 2026.
- Gennari A, et al. Ann Oncol 2021;32(12):1475–95.
- Miglietta F, et al. NPJ Breast Cancer 2022;8(1):66.
- Miglietta F, et al. NPJ Breast Cancer 2021;7(1):137.
- Tarantino P, et al. Eur J Cancer 2022;163:35–43.
- Bornstein-Quevedo L, et al. J Pers Med 2024;14(5):467.
- Shang J, et al. Transl Breast Cancer Res 2024;5:29.




