BRCA1/2 beim Mammakarzinom
Bedeutung und Prävalenz von BRCA1/2 Mutationen beim Mammakarzinom
Mutationen in BRCA1 und BRCA2 sind von hoher klinischer Relevanz für Diagnostik, Therapie und Risikobewertung beim Mammakarzinom. Pathogene BRCA1/2-Mutationen in der Keimbahn (gBRCA1/2) finden sich bei etwa 5 % aller Patientinnen;1 in Risikokollektiven mit jungem Erkrankungsalter oder familiärer Belastung sind über 30 % möglich.2,3 Somatische BRCA1/2-Mutationen (sBRCA1/2), die nur im Tumorgewebe nachweisbar sind, treten in rund 3 % der Fälle auf.4
BRCA1/2-assoziierte Mammakarzinome weisen häufig aggressive Eigenschaften auf. Sie sind meist invasiv, hochgradig differenziert (G3) und zeigen nicht selten medulläre Anteile. Häufig liegt ein triple-negatives Profil (ER-, PR-, HER2-negativ) vor, verbunden mit einem erhöhten Rezidivrisiko.1 Histologisch handelt es sich überwiegend um invasive duktale Karzinome. Invasive lobuläre Karzinome sind deutlich seltener und kommen bei BRCA1-Mutationen nur in etwa 1 % der Fälle vor, während sie bei BRCA2-Mutationen mit etwa 7 % häufiger sind.1
Die Assoziation von BRCA-Mutationen mit bestimmten molekularen Subtypen ist gut belegt.1 BRCA1-Mutationen treten vor allem bei triple-negativen Mammakarzinomen (TNBC) auf, während BRCA2-Mutationen häufiger mit ER-positiven/HER2-negativen Tumoren assoziiert sind. Insgesamt weisen bis zu 10 % der Patientinnen mit HER2-negativem Mammakarzinom eine gBRCA-Mutation auf.1 In TNBC-Kollektiven werden Prävalenzen von über 30 % beschrieben, bei Hormonrezeptor(HR)-positiven Tumoren liegt die Häufigkeit hingegen bei etwa 5 %.1 Da HR-positiv/HER2-negativ der häufigste Subtyp ist, entfallen in absoluten Zahlen die meisten BRCA-Mutationen dennoch auf dieses Erkrankungsbild.
Die Young Women’s Breast Cancer Study, eine multizentrische prospektive Kohortenstudie, untersuchte 1.143 Tumoren von Frauen ≤ 40 Jahren mit neu diagnostiziertem Brustkrebs. Dabei wurde unter anderem die Verteilung der molekularen Subtypen bei Patientinnen mit BRCA1- oder BRCA2-Mutationen analysiert.5
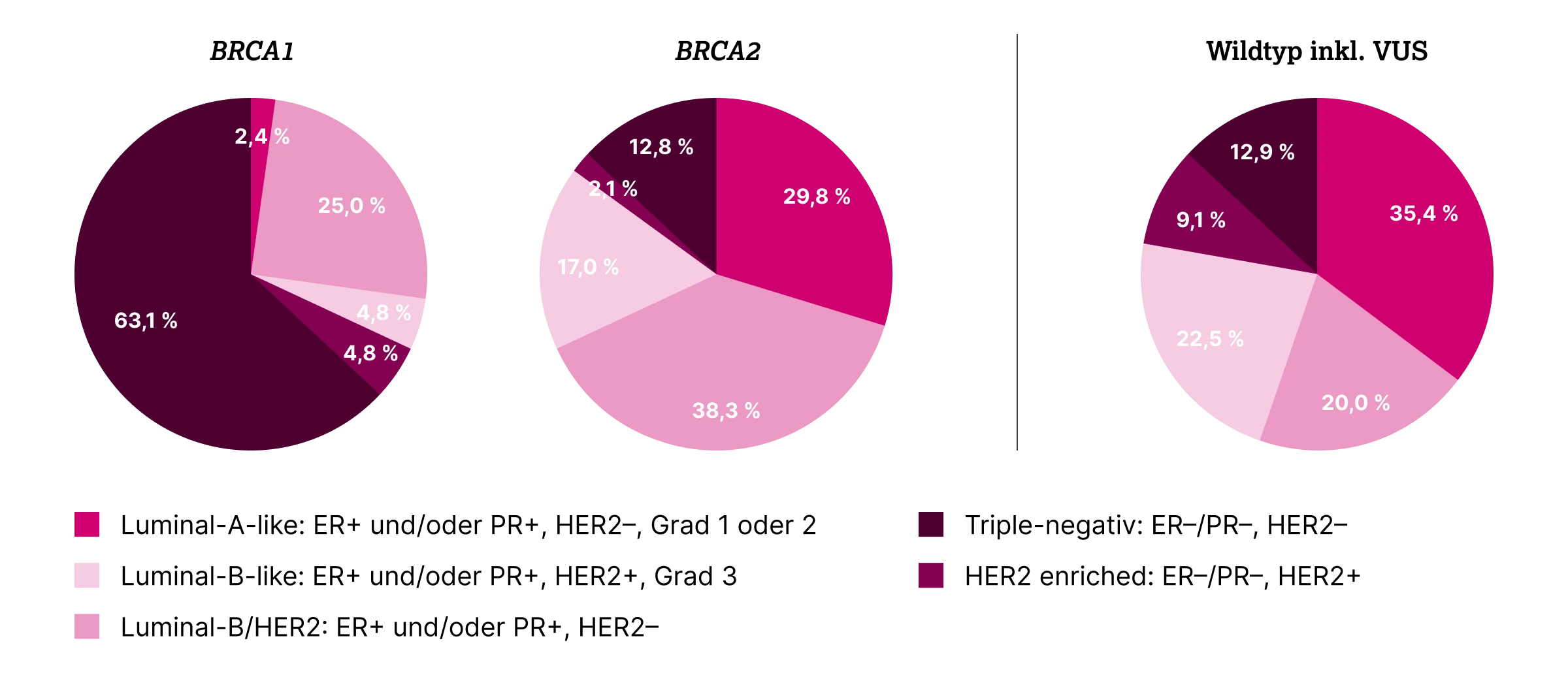
Die Analyse der molekularen Subtypen zeigt deutliche Unterschiede zwischen BRCA1- und BRCA2-Mutationsträgerinnen: Bei BRCA1 dominierten triple-negative Karzinome (63,1 %), gefolgt von Luminal-B-like (29,8 %), HER2-enriched (4,8 %) und Luminal-A-like (2,4 %). Tumoren mit BRCA2-Mutationen wiesen hingegen überwiegend einen Luminal-B-like Subtyp auf (55,3 %), gefolgt von Luminal A-like (29,8 %), triple-negativ (12,8 %) und HER2-enriched (2,1 %).5
Diese Ergebnisse unterstreichen die Bedeutung der molekularen Subtypisierung bei jungen Patient:innen mit Mammakarzinom. Der enge Zusammenhang von TNBC mit BRCA1- und von Luminal-B-like mit BRCA2-Mutationen liefert wertvolle Hinweise bezüglich Tumorprofil und Risiken.5
Lebenszeitrisiko und Risiko für weitere Malignome
Träger:innen pathogener BRCA1- oder BRCA2-Mutationen haben ein erheblich erhöhtes Lebenszeitrisiko für Brustkrebs und Ovarialkarzinome. Das Erkrankungsrisiko für Brustkrebs liegt bei durchschnittlich 70%, für Ovarialkarzinom bei unter 20 % (BRCA2) bis etwa 45 % (BRCA1).2 Betroffene Frauen erkranken im Mittel 20 Jahre früher als Patient:innen ohne familiäre Belastung. Das Risiko für ein kontralaterales Mammakarzinom hängt stark vom Alter bei Erstdiagnose ab und beträgt innerhalb von 20 Jahren nach der Ersterkrankung rund 25 % bei BRCA2- und bis zu 40 % bei BRCA1-Mutationen.2
Kuchenbaecker et al. untersuchten in einer prospektiven Kohortenstudie das altersabhängige Risiko für Brust- und Ovarialkarzinome bei insgesamt über 9.800 BRCA1- und BRCA2-Mutationsträgerinnen aus internationalen genetischen Hochrisikokollektiven.6
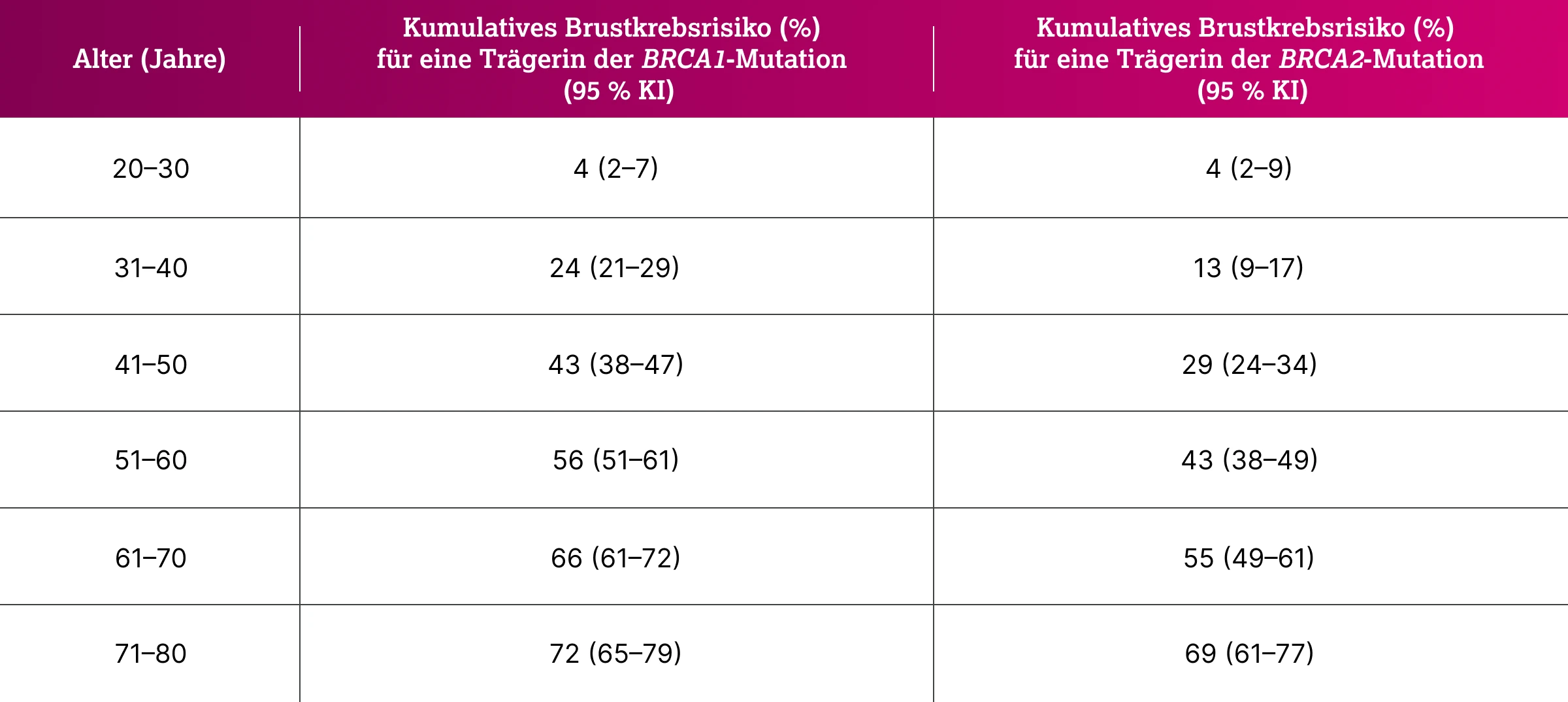
Die Ergebnisse zeigen, dass das kumulative Risiko für ein Mammakarzinom für BRCA1-Trägerinnen mit 43 % bereits bis zum 50. Lebensjahr sehr hoch liegt und bei BRCA2-Trägerinnen zum gleichen Zeitpunkt etwa 29 % erreicht. Mit steigendem Alter nehmen die Risiken weiter zu und erreichen bis zum 80. Lebensjahr rund 72 % für BRCA1- und 69 % für BRCA2-Mutationsträgerinnen (siehe Tabelle).6
Relevanz der BRCA1/2‑Testung beim Mammakarzinom
Für die Therapieplanung beim Mammakarzinom ist insbesondere bei HER2‑negativen Erkrankungen der Nachweis einer BRCA1/2‑Keimbahnmutation prädiktiv für den potenziellen Nutzen einer Behandlung mit Poly(ADP‑Ribose)-Polymerase (PARP)-Inhibitoren. Dies gilt sowohl für Patient:innen mit fortgeschrittenem oder metastasiertem Mammakarzinom als auch für Erkrankte im frühen Stadium mit hohem Rezidivrisiko. Auch beim TNBC ist die BRCA1/2‑Testung therapeutisch relevant, auch für die Abschätzung des Ansprechens auf eine Chemotherapie. Um alle Therapieoptionen rechtzeitig berücksichtigen zu können, sollte die Testung daher möglichst früh im Krankheitsverlauf erfolgen.2,7
Studien & Leitlinienempfehlungen zur BRCA1/2 Testung beim Mammakarzinom
S3-Leitlinie und AGO: Empfehlungen zur frühzeitigen BRCA1/2‑Keimbahntestung
Laut S3‑Leitlinie sollte beim Mammakarzinom eine möglichst frühe BRCA1/2‑Keimbahntestung erfolgen – idealerweise bereits bei Diagnosestellung, spätestens jedoch vor therapieentscheidenden Schritten (z. B. zur Prüfung von PARP‑Inhibitor‑Optionen). Sie ist besonders relevant beim HER2‑negativen fortgeschrittenen oder metastasierten Mammakarzinom, beim TNBC sowie bei familiärer Belastung.2
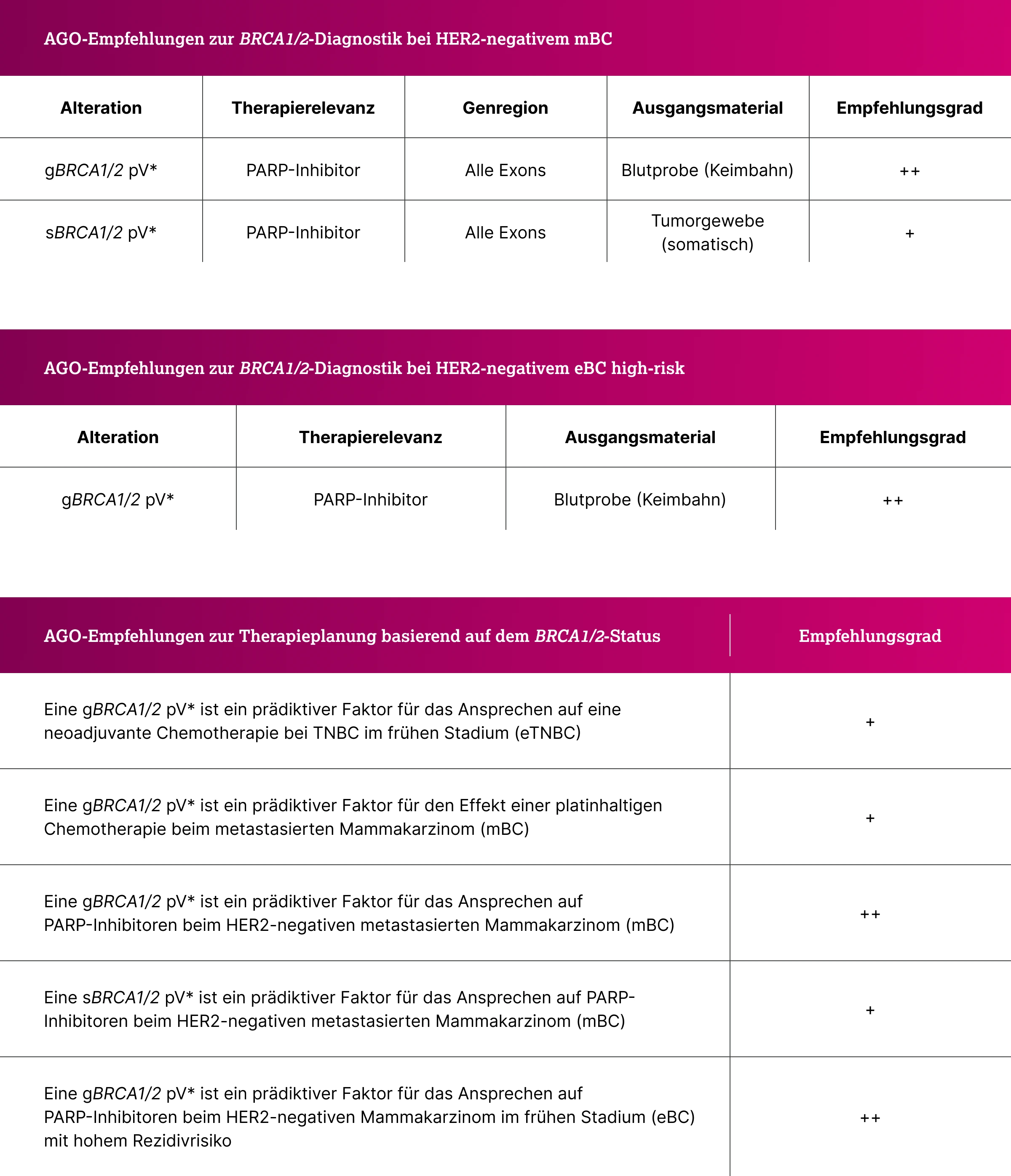
*pV: wahrscheinlich pathogene/pathogene Variante (Klasse 4/5 Mutation)
Die Arbeitsgemeinschaft Gynäkologische Onkologie e.V. (AGO) spricht sich ebenfalls für eine frühzeitige BRCA1/2‑Keimbahntestung aus, sofern das Ergebnis für die Therapieplanung relevant ist. Besonders wichtig ist dies bei HER2‑negativen metastasierten Mammakarzinomen (mBC) sowie bei HER2‑negativen frühen Mammakarzinomen (eBC) mit hohem Rezidivrisiko, da hier je nach Zulassungskriterien eine Behandlung mit PARP‑Inhibitoren in Frage kommen kann. Auch bei Patient:innen mit TNBC ist die Keimbahntestung von zentraler Bedeutung für die weitere Therapieplanung.7

Laut S3-Leitlinie und AGO‑Empfehlungen sollte unabhängig von der Tumorbiologie des Mammakarzinoms eine BRCA1/2‑Testung auch dann erfolgen, wenn eine familiäre Belastung nach den Kriterien des Deutschen Konsortiums Familiärer Brust- und Eierstockkrebs vorliegt. Hier besteht die Indikation bereits bei definierten Konstellationen in der Eigen- oder Familienanamnese:2,7
Internationale Empfehlungen: BRCA1/2-Keimbahntestung zur Therapieentscheidung und Risikoabschätzung
Internationale Fachgesellschaften sprechen sich für eine frühzeitige BRCA1/2‑Keimbahntestung aus, sofern das Ergebnis therapeutische Konsequenzen oder eine Relevanz für die familiäre Risikoabschätzung hat:
Die European Society for Medical Oncology (ESMO) betont die Bedeutung der Testung insbesondere bei fortgeschrittenem Mammakarzinom – dazu zählen das ER‑positive/HER2‑negative Mammakarzinom, das TNBC, sowie das Mammakarzinom beim Mann. Eine Testung wird auch empfohlen, wenn ein erbliches Risiko vermutet wird.8,9
Laut gemeinsamer Leitlinie der American Society of Clinical Oncology (ASCO) und der Society of Surgical Oncology (SSO) sollte allen neu diagnostizierten Patient:innen im Alter von ≤ 65 Jahren eine BRCA1/2‑Keimbahntestung angeboten werden. Bei Patient:innen > 65 Jahren sollte die Testung angeboten werden, wenn eine therapeutische Relevanz besteht (z. B. Einsatz von PARP‑Inhibitoren), wenn eigen-/familienanamnestische Hinweise auf ein erhöhtes Risiko vorliegen oder eine bestimmte ethnische Herkunft (z. B. aschkenasisch-jüdisch) gegeben ist. Bei einem rezidivierten Mammakarzinom (lokal oder metastasiert) wird die Testung unabhängig von der Familienanamnese empfohlen, sofern der Einsatz von PARP‑Inhibitoren in Frage kommt.10
Auch das National Comprehensive Cancer Network (NCCN) unterstreicht in seinen aktuellen Leitlinien die Bedeutung der BRCA1/2‑Keimbahntestung sowohl für die systemische Therapieentscheidung – insbesondere beim metastasierten HER2‑negativen Mammakarzinom – als auch im Rahmen der Abklärung eines möglichen hereditären Risikos. Hierbei sollen ebenfalls sowohl die persönlichen als auch die familiären Anamnesekriterien berücksichtigt werden.11,12
Abkürzungen:
AGO: Arbeitsgemeinschaft Gynäkologische Onkologie e.V.; ASCO: American Society of Clinical Oncology; BC: Brustkrebs¸BRCA1: Breast Cancer Associated Gene 1; BRCA2: Breast Cancer Associated Gene 2; eBC: Mammakarzinom im frühen Stadium; ER: Östrogenrezeptor; ESMO: European Society for Medical Oncology; eTNBC: triple-negatives Mammakarzinom im frühen Stadium; gBRCA1/2 pV: pathogene oder wahrscheinlich pathogene BRCA1/2K‑Keimbahnvariante; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HR: Hormonrezeptor; HRD: homologe Rekombinationsdefizienz; KI: Konfidenzintervall; mBC: metastasiertes Mammakarzinom; NCCN: National Comprehensive Cancer Network; OC: Ovarialkarzinom; PARP: Poly(ADP-Ribose)-Polymerase; PD-L1: Programm cell death ligand-1; pV: pathogene oder wahrscheinlich pathogene Variante; sBRCA1/2 pV: pathogene oder wahrscheinlich pathogene somatische BRCA1/2‑Variante; SSO: Society of Surgical Oncology; TNBC: triple-negatives Mammakarzinom
- Arun B, et al. Br J Cancer 2024;131(9):1400–14.
- S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 5.0, Dezember 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mammakarzinom_4_0/Version_5/LL_Mammakarzinom_Langversion_5.0.pdf. Letzter Zugriff: Februar 2026.
- Armstrong N, et al. Clin Epidemiol 2019;11:543–61.
- Tung NM, et al. Br J Cancer 2018;119(2):141–52.
- Guzmán-Arocho YD, et al. Br J Cancer 2022;126(2):302–9.
- Kuchenbaecker KB, et al. JAMA 2017;317(23):2402–16.
- Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.V. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlungen 2025.1D. Verfügbar unter https://www.ago-online.de/leitlinien-empfehlungen/leitlinien-empfehlungen/kommission-mamma. Letzter Zugriff: Januar 2026.
- Loibl S, et al. Ann Oncol 2024;35(2):159–82.
- Turnbull C, et al. Ann Oncol 2025;36(8):853–65.
- Bedrosian I, et al. J Clin Oncol 2024;42(5):584–604.
- National Comprehensive Cancer Network. Genetic/Familial High-Risk Assessment: Breast, Ovarian, Pancreatic, and Prostate. Version 2.2026. October 10, 2025. Verfügbar unter nccn.org/professionals/physician_gls/pdf/genetics_bopp.pdf. Letzter Zugriff: Januar 2026.
- National Comprehensive Cancer Network. Breast Cancer Version 5.2025. October 16, 2025. Verfügbar unter www.nccn.org/professionals/physician_gls/pdf/breast.pdf. Letzter Zugriff: Januar 2026

