PD-L1 beim Lungenkarzinom
Bedeutung und Prävalenz von PD-L1 beim Lungenkarzinom
PD-L1 (Programmed cell death ligand-1) ist ein immunologischer Biomarker zur Charakterisierung der Immunaktivität im Tumormikromilieu. Beim Lungenkarzinom wird die PD-L1 Expression auf Tumorzellen durch eine erhöhte Zytokinfreisetzung im Tumorumfeld hochreguliert.1 Über die Bindung an den PD-1 Rezeptor auf T-Zellen kann PD-L1 deren Aktivität supprimieren und so die Erkennung und Elimination der Tumorzellen durch das Immunsystem verhindern.2
Diese Immunevasion macht PD-L1 zu einem relevanten prädiktiven Biomarker für Immuntherapien, die gegen PD-1 oder PD-L1 gerichtet sind.1
Zur Identifikation potenziell therapieansprechender Patient:innen haben sich Schwellenwerte von ≥1 % und ≥50 % PD-L1 positiver Tumorzellen etabliert.3–6 Allerdings ist die Aussagekraft der PD-L1 Expression begrenzt: Ein hoher Expressionsgrad korreliert nicht immer mit einem klinischen Ansprechen, während auch Patient:innen mit niedriger oder fehlender Expression von einer Immuntherapie profitieren können.3
Trotz dieser Einschränkungen gilt PD-L1 derzeit als der einzige etablierte prädiktive Biomarker zur Therapieentscheidung in der immunonkologischen Behandlung des NSCLC.7
PD-L1 Nachweisvarianz beim NSCLC
Die ermittelte PD-L1 Expressionsrate beim NSCLC unterliegt deutlichen Schwankungen, beeinflusst durch methodische und biologische Faktoren wie:3
Verwendeter Antikörper-Assay
Färbeplattform
Lagerungsdauer der Gewebeproben
Histologischer Subtyp
Molekulare Alterationen
Tumorstadium
Grob lässt sich die Verteilung der Tumoren anhand des Tumor Proportion Score (TPS) in drei etwa gleich häufige Kategorien einteilen: < 1 %, 1–49 % und ≥ 50 %.3
Eine aktuelle Metaanalyse von 78 unselektierten NSCLC-Kohorten (publiziert zwischen 2015 und 2023) ergab eine gepoolte Prävalenz von ca. 54 % für eine PD-L1 Expression ≥ 1 % und rund 25 % für eine Expression ≥ 50 %.3

Welche Bedeutung hat die Bestimmung der PD-L1 Expression?
Die Bestimmung der PD-L1 Expression auf Tumorzellen ist von zentraler Bedeutung für die moderne Krebstherapie. Insbesondere beim NSCLC konnte in zahlreichen klinischen Studien gezeigt werden, dass der Einsatz von Anti-PD-1/PD-L1 Antikörpern mit einem relevanten klinischen Benefit verbunden ist.8–12 Patient:innen mit Tumoren, die eine hohe PD-L1 Expression aufweisen, zeigen signifikant höhere Ansprechraten auf eine Monotherapie mit diesen Immuncheckpoint-Inhibitoren als jene mit geringer oder fehlender PD-L1 Expression.13 Die Bestimmung des PD-L1 Status ist daher essenziell, um die Indikation für eine Immuntherapie fundiert stellen zu können.14,15 PD-L1 ist derzeit der einzige etablierte prädiktive Biomarker zur Festlegung von Immuncheckpoint-Therapien beim NSCLC.16,17
Studien & Leitlinienempfehlungen zur PD-L1 Testung beim Lungenkarzinom
Indikation zur PD-L1 Testung
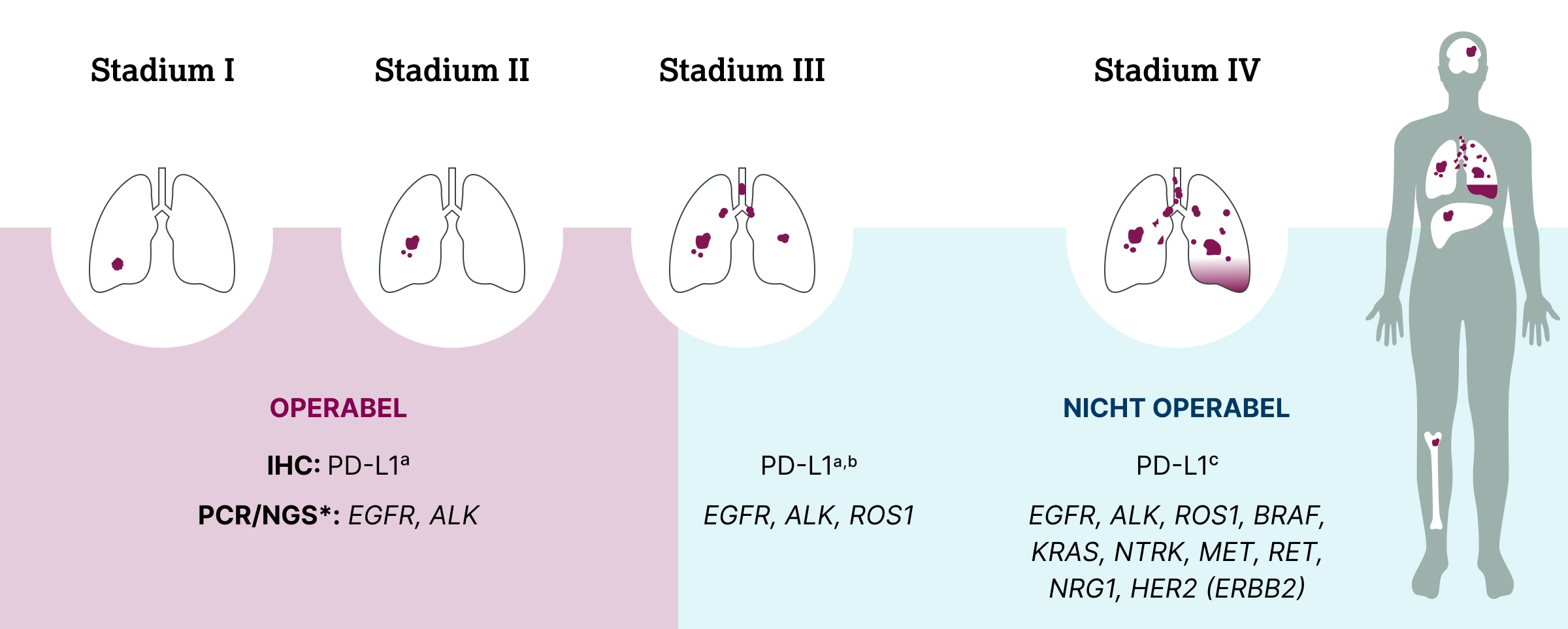
a) Die PD-L1 Testung wird gemäß Onkopedia-Leitlinie in den Stadien IB–IIIC empfohlen,14 laut S3-Leitlinie in den frühen Stadien IB–IIIA des nichtkleinzelligen Lungenkarzinoms.15
b) Im Stadium III wird in der Onkopedia- und der S3-Leitlinie eine PD-L1 Testung im Rahmen der Primärdiagnostik empfohlen,14,15 darüber hinaus eine Testung auf EGFR, ALK und ROS1 bei allen nicht resezierbaren NSCLC.15
c) Im Stadium IV wird die PD-L1 Testung laut S3-Leitlinie generell für alle histologischen NSCLC-Typen empfohlen;15 die Onkopedia-Leitlinie empfiehlt sie vor Beginn einer medikamentösen Erstlinientherapie.14
Bei Patient:innen mit NSCLC der Stadien IB–III sowie bei allen histologischen Subtypen im Stadium IV soll eine immunhistochemische PD-L1 Testung parallel zu molekularpathologischen Standarduntersuchungen erfolgen.15
Die immunhistochemische Auswertung der PD-L1 Expression beim NSCLC soll derzeit nach mindestens zwei verschiedenen Auswertealgorithmen erfolgen, abhängig vom einzusetzenden Immuncheckpoint-Inhibitor. Der Tumor Proportion Score (TPS) erfasst und dokumentiert dabei den prozentualen Anteil PD-L1 positiv gefärbter Tumorzellen bezogen auf alle vitalen Tumorzellen.15
Bei Stadium-IV-Tumoren ist zusätzlich der Immune Cell Score (IC-Score) anzugeben, der den Flächenanteil PD-L1 positiver Immunzellen widerspiegelt. Letzterer ist in zytologischen Präparaten und vielen EBUS-TBNA-Proben nicht valide, da die Flächenberechnung hier methodisch limitiert ist.15
Weitere Scores für die PD-L1 Auswertung (CPS, TAP), die bei anderen Tumorarten zum Einsatz kommen, finden Sie hier.

Informationen zum PD-L1 Biomarker beim Lungenkarzinom
Paralleltestung molekularer Biomarker
Bei Nachweis eines therapierelevanten PD-L1 TPS-Schwellenwerts ist in den frühen operablen Stadien ergänzend eine EGFR-Mutationsanalyse sowie ALK-Fusionsdiagnostik obligat. Diese Untersuchungen können bereits parallel zur PD-L1 Immunhistochemie initiiert werden, um zeitnahe Therapieentscheidungen zu ermöglichen.15 In Stadium IV wird eine deutlich umfangreichere Testung an molekularen Markern empfohlen, die alle therapeutisch relevanten molekularen Alterationen einbezieht (siehe Abb. oben).15

Informationen zum EGFR-Biomarker beim Lungenkarzinom
PD-L1 Nachweis im Rahmen der Erstdiagnose
Die immunhistochemische Bestimmung von PD-L1 hat sich als fester Bestandteil der Primärdiagnostik beim NSCLC etabliert. Eine Reflex-Testung bei allen neu diagnostizierten NSCLC-Fällen ermöglicht eine effiziente Integration in die diagnostischen Abläufe. Dies reduziert sowohl den organisatorischen als auch den materiellen Aufwand, da ein erneutes Heraussuchen oder Anschneiden des Tumorblocks vermieden wird.18
Die frühzeitige PD-L1 Diagnostik stellt sicher, dass der Immunstatus rechtzeitig zur Therapieentscheidung vorliegt – ein entscheidender Vorteil insbesondere bei der Indikationsstellung für Immuncheckpoint-Inhibitoren.19
Entsprechend empfiehlt die aktuelle S3-Leitlinie, den PD-L1 Status bei Patient:innen mit NSCLC bereits im Rahmen der Primärdiagnostik zu erheben.15

Abkürzungen
ALK: Anaplastische Lymphomkinase (Gen); APZ: Antigenpräsentierende Zelle; BRAF: Serin/Threonin-Kinase B-Raf (Gen); CPS: kombinierter Positivitäts-Score; CTLA-4: Cytotoxic T-Lymphocyte Antigen 4; EBUS-TBNA: endobronchialer Ultraschall mit transbronchialer Nadelaspiration; EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); ERBB2: v-erb-b2 erythroblastic leukemia viral oncogene homolog; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2 (Gen); IC-Score: Immune Cell Score; ICI: Immuncheckpoint-Inhibitor; KRAS: Kirsten Rat Sarkoma (Gen); MET: Mesenchymal-epithelialer Transitionsfaktor (Gen); MHC: Haupthistokompatibilitätskomplex; NRG1: Neuregulin 1 (Gen); NSCLC: nicht-kleinzelliges Lungenkarzinom; NTRK: Neurotrophe Tyrosinrezeptor-Kinasen (Gen); PD-1: Programmed cell death-1; PD-L1: Programmed cell death ligand-1; RET: Rearranged during Transfection (Gen); ROS1: ROS-Protoonkogen 1 (Gen); TAP: tumorassoziierter Positivitäts-Score; TPS: Tumor Proportion Score; TZR: T-Zell-Rezeptor
- Kerr KM, et al. Arch Pathol Lab Med 2016;140(3):249–54.
- Sun C, et al. Immunity 2018;48(3):434–52.
- Ngo P, et al. Sci Rep 2025;15(1):4166.
- Reck M, et al. N Engl J Med 2016;375(19):1823–33.
- Forde PM, et al. N Engl J Med 2022;386(21):1973–85.
- Paz-Ares L, et al. Ann Oncol 2020;31(6):798–806.
- Mamdani H, et al. Front Immunol 2022;13:823618.
- Rittmeyer A, et al. Lancet 2017;389(10066):255–65.
- Vallejo J, et al. Oncologist 2024;29(5):422–30.
- Xu Y, et al. Transl Lung Cancer Res 2019;8(4):413–28.
- Gandhi L, et al. N Engl J Med 2018;378(22):2078–92.
- Reck M, et al. J Clin Oncol 2021;39(21):2339–49.
- Passiglia F, et al. J Thorac Oncol 2025;20(5):614–24.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig (NSCLC). April 2025. Verfügbar unter onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: Februar 2026.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: Februar 2026.
- Boudou-Rouquette P, et al. EBioMedicine 2021;73:103630.
- Tostes K, et al. Int J Mol Sci 2023;24(15):11887.
- Gosney JR, et al. ESMO Open 2023;8(4):101587.
- Schildhaus HU. Pathologe 2018;39(6):498–519.



