HER2-Diagnostik beim Mammakarzinom
Für die Diagnostik und Therapieplanung beim Mammakarzinom ist die Bestimmung des HER2-Status von zentraler Bedeutung. Die beiden etablierten Nachweismethoden – Immunhistochemie (IHC) und In-situ-Hybridisierung (ISH) – ergänzen sich gegenseitig durch die Untersuchung unterschiedlicher, molekularer Aspekte, wobei sich aufgrund der eingesetzten Technologien die Bearbeitungszeit unterscheidet.

HER2-Nachweismethoden beim Mammakarzinom
HER2-Testung mittels Immunhistochemie (IHC)
Gemäß der 2018 und 2023 aktualisierten ASCO/CAP-Leitlinien soll der HER2-Status zunächst mittels Immunhistochemie unter Verwendung eines semiquantitativen Scoring-Systems beurteilt werden.6,7 Je nach Färbegrad wird dem Gewebeschnitt einer von vier IHC-Scores zugewiesen – von IHC 0 (keine Färbung) bis IHC 3+ (starke Färbung).6 Ein IHC-Score von 3+ wird demnach als eindeutig HER2-positiv bewertet, ein IHC-Score von 2+ als unklar. In den unklaren Fällen ist die Untersuchung einer möglichen HER2-Genamplifikation mittels In-situ-Hybridisierung (ISH) als Reflex-Testung zur Abklärung erforderlich. Bei einem IHC-Score von 2+ ohne Genamplifikation sowie einem Score von 1+ oder 0 wurden Tumoren klassischerweise klinisch als HER2-negativ beurteilt.8
Weitere HER2-Subgruppen beim Brustkrebs
Mittlerweile sind auch Patient:innen mit inoperablem oder metastasiertem (HR+ und HR–) Brustkrebs und geringer HER2-Überexpression klinisch behandelbar,9,10 weshalb eine rein binäre Einteilung in HER2-positiv und HER2-negativ nicht mehr ausreichend ist: Die aktualisierte ASCO/CAP-Leitlinie weist explizit darauf hin, dass Tumoren mit einem HER2-Status von IHC 1+ oder IHC 2+ / ISH-negativ für eine Behandlung infrage kommen können, also solche mit geringerer HER2-Expression und ohne Genamplifikation.6
Die European Society for Medical Oncology (ESMO) schlägt daher vor, für die Untergruppe von HER2-negativen Tumoren mit IHC 1+ oder IHC 2+ / ISH-negativ den Begriff „HER2-low“ zu verwenden.11
„HER2-0" (manchmal auch „HER2-zero“ genannt) soll entsprechend für Tumoren mit IHC 0 verwendet werden.11
Neue Subgruppe: „HER2-ultralow“
Am unteren Ende des HER2-Expressionsspektrums wurde kürzlich auch noch die Kategorie „HER2-ultralow“ eingeführt.11 Sie beschreibt Tumoren, die klassisch als IHC 0 klassifiziert werden, bei denen jedoch einzelne Tumorzellen eine schwache oder inkomplette Membranfärbung zeigen. Der Anteil dieser Zellen überschreitet 10 % nicht, sodass noch kein HER2-low Status vorliegt.11 Bereits eine einzige gefärbte Tumorzelle genügt für diese Einordnung, weshalb der klinische Begriff HER2-ultralow manchmal auch mit dem Kommentar „IHC 0 mit Membranfärbung“ berichtet wird oder auch nur durch die zusätzliche Angabe des genauen Prozentsatzes der Tumorzellen mit Membranfärbung bei IHC 0. Um die Identifikation dieser und zukünftig ggf. noch weiterer relevanter Subgruppen in der Breite zu gewährleisten, empfiehlt die aktuelle S3-Leitlinie Mammakarzinom explizit die Angabe des IHC-Scores (0, 1+, 2+, 3+) zusammen mit dem genauen Prozentsatz der für den IHC-Score maßgeblichen Tumorzellen mit Membranfärbung.12 Tumoren ohne Tumorzellen mit Membranfärbung gelten als HER2-null, werden aber manchmal auch mit dem Kommentar „IHC 0 ohne Membranfärbung“ berichtet bzw. als IHC 0 und 0 % Tumorzellen mit Membranfärbung.11
Die Unterscheidung zwischen HER2-low, HER2-ultralow und HER2-null hat zunehmend therapeutische Relevanz. Bereits heute ist ein Antikörper-Wirkstoff-Konjugat (ADC) für Patient:innen mit HR+, HER2-ultralow Mammakarzinom zugelassen.13 Eine differenziertere HER2-Bewertung hat somit nochmals erheblich an Bedeutung gewonnen für die pathologische Befundung und die onkologische Therapieentscheidung.
In-situ-Hybridisierung (ISH) mit zwei Sonden
Bei einem IHC-Score von 2+ kann die mäßig erhöhte HER2-Proteinexpression durch eine Gen-Amplifikation hervorgerufen sein, aber auch andere Ursachen haben und gilt somit als unklar. Daher empfiehlt die ASCO/CAP-Leitlinie hier zur Bestimmung des HER2-Amplifikationsstatus eine ISH-Testung mit zwei Sonden (Dual-Probe-ISH-Assay).6,7 Dabei wird neben der genspezifischen Sonde eine Chromosomenzählsonde (Chromosome Enumerating Probe, CEP) eingesetzt. Durch diese duale Markierung werden sowohl das HER2-Gen als auch das Chromosom 17 (CEP17) identifiziert und quantifiziert. Der folgende Algorithmus zeigt die vorgeschlagene Klassifizierung der Ergebnisse in fünf Gruppen in Abhängigkeit vom HER2/CEP17-Verhältnis.
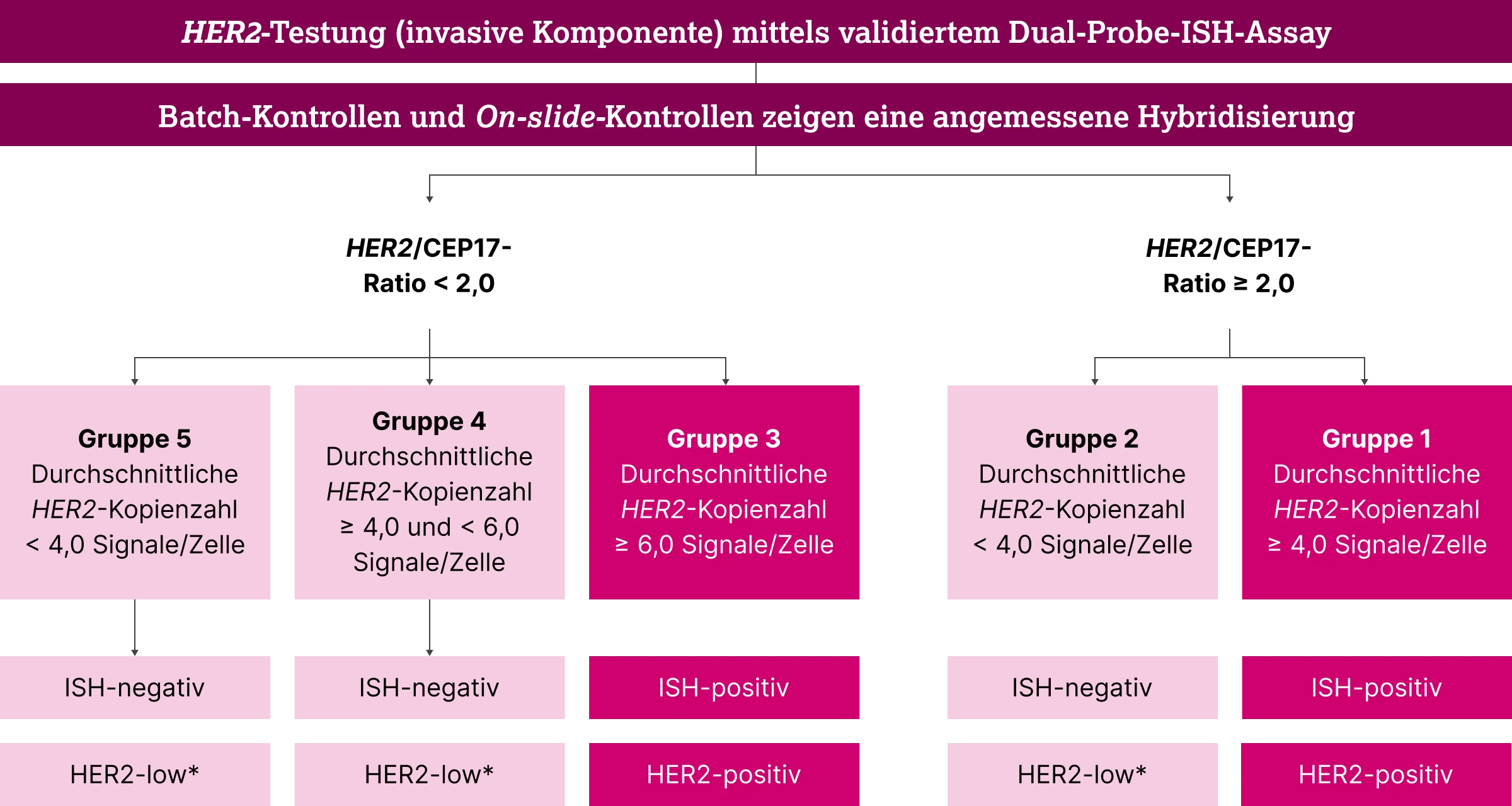
* Im Fall von IHC 1+ oder 2+
Gruppe 1 (HER2/CEP17-Verhältnis ≥ 2, HER2-Kopienzahl ≥ 4) und Gruppe 5 (HER2/CEP17-Verhältnis < 2, HER2-Kopienzahl < 4) stellen die beiden Extreme des Spektrums der HER2-Bewertung dar (Vorhandensein bzw. Fehlen einer HER2-Amplifikation). Etwa 95 % der mittels Dual-Probe-ISH-Assay auf HER2(ERBB2) Gen-Amplifikation getesteten Tumore fallen in diese beiden Gruppen.7
Nur etwa 5 % der Fälle werden den Gruppen 2, 3 oder 4 zugeordnet, die schwierige Szenarien mit nicht eindeutiger Interpretation aufweisen.7 Daher wird für diese drei Gruppen eine zusätzliche Überprüfung der IHC-Objektträger empfohlen, um auf der Grundlage der kombinierten Interpretation von ISH- und IHC-Testung die genaueste Zuordnung des HER2-Status zu erreichen.7
Tipps und Infos zur HER2-low und HER2-ultralow Diagnostik
Präzise und reproduzierbare Teststrategien sind entscheidend, um Patient:innen zu identifizieren, die von einer HER2-gerichteten Therapie profitieren können.
Herausforderungen durch HER2-low und HER2-ultralow
HER2-gerichtete Therapien zeigen auch bei fortgeschrittenem Brustkrebs mit geringer oder minimaler HER2-Überexpression (HER2-low und HER2-ultralow) eine starke Anti-Tumor-Wirkung.9,10,14 Damit gewinnen diese Subgruppen zunehmend an therapeutischer Relevanz – und stellen Patholog:innen vor die Herausforderung, insbesondere Grenzfälle zwischen IHC 0 und IHC 1+ sicher und reproduzierbar zu differenzieren.15–17
Fehlklassifikationen im unteren Teil des HER2-Spektrums (HER2-low vs. HER2-ultralow vs. HER2-null) können dazu führen, dass Patient:innen von einer potenziell wirksamen Therapie ausgeschlossen werden.18 Die Interpretation der IHC bleibt jedoch semiquantitativ und in Teilen subjektiv, was sie anfällig für interindividuelle Variabilität macht. Um die Diagnosesicherheit zu erhöhen, ist ein standardisiertes Vorgehen essenziell. Die zunehmende Verfügbarkeit von Bildern digitalisierter Objektträger (Whole Slide Images, WSI) eröffnet neue Möglichkeiten: Durch KI-gestützte Bildanalyse kann die Bewertung objektiviert und die Reproduzierbarkeit verbessert werden, indem z. B. nicht nur ein Ausschnitt (FOV, Field of View) des Gewebes auf dem Objektträger analysiert wird, sondern das gesamte Gewebe, was die Tumorheterogenität viel besser abdeckt. Auch können nur wenige gefärbte Zellen auf einem Objektträger mit KI-Unterstützung zuverlässig gefunden werden. Zudem sollten alle präanalytischen und analytischen Faktoren, die die Sensitivität und Aussagekraft der HER2-Testung beeinflussen können, konsequent berücksichtigt und optimiert werden.
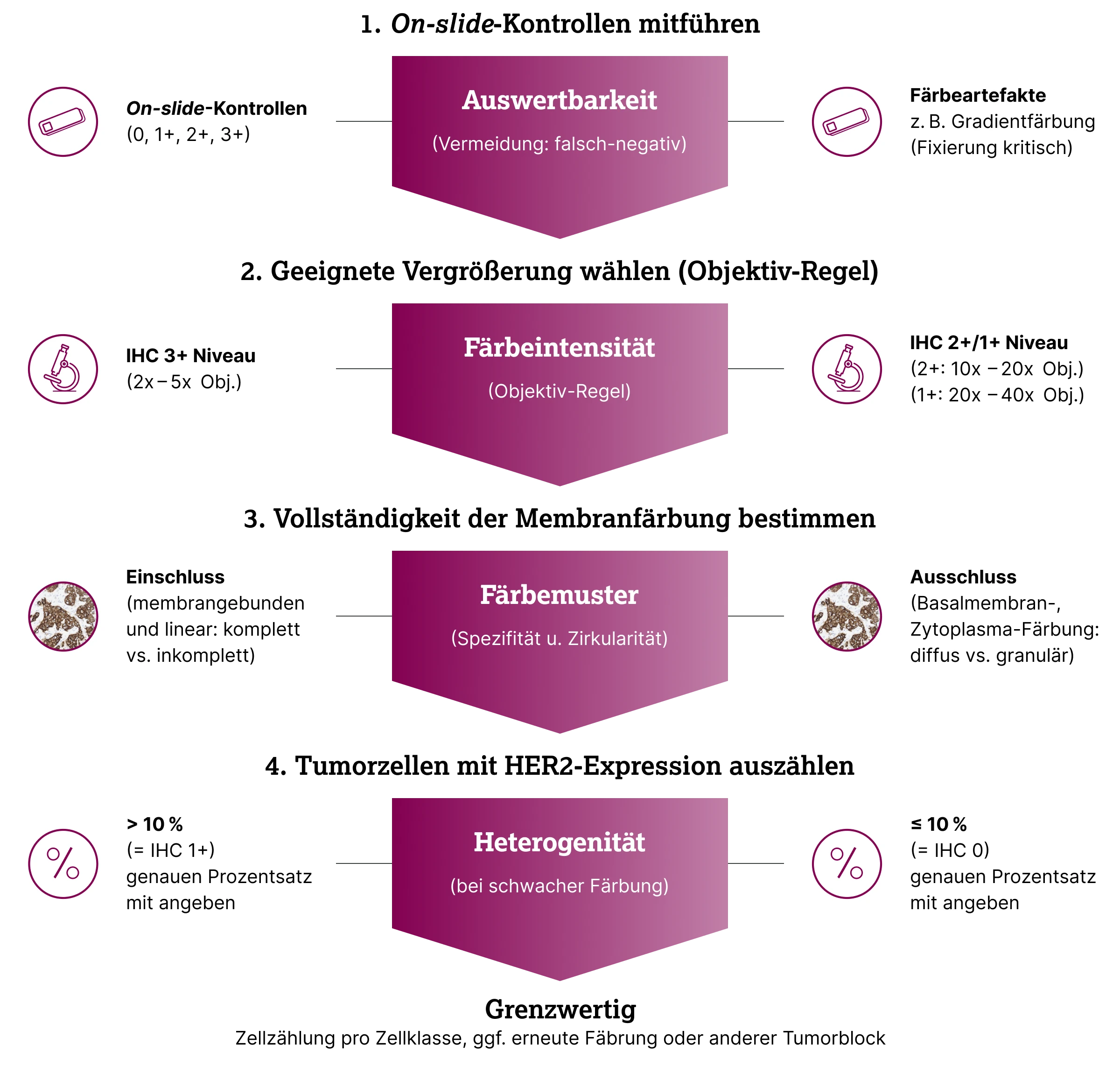
Tipps zum Vorgehen bei der HER2-low Diagnostik
Die HER2-Diagnostik mittels IHC und ISH erfolgt auch in Deutschland gemäß der ASCO/CAP Leitlinie von 2018 (aktualisiert 2023) basierend auf der Färbeintensität, dem Färbemuster und dem prozentualen Anteil der vier Klassen von Tumorzellen in der Probe (ungefärbt vs. schwach, partiell vs. schwach bis mäßig, komplett vs. stark, komplett).6,7 Denkert et al. schlagen in einer Übersichtsarbeit17 folgende Konkretisierung der Vorgehensweise zur Beurteilung der HER2-Färbungen vor und geben praktische Tipps für schwierige Fälle:
- Es wird empfohlen, Gewebeblöcke, die das gesamte HER2-Spektrum abdecken, als On-slide-Kontrollen mitzuführen.17 Hierfür stehen mittlerweile Zelllinien mit definierter HER2-Expression zur Verfügung.
- Mithilfe solcher Kontrollen lässt sich die Validität des Färbeprozesses prüfen und mögliche Färbeartefakte erkennen.
Unter Anwendung der „Objektiv- bzw. Vergrößerungsregel“ sollten alle Tumorbereiche auf einem Objektträger durchgemustert werden.17,19 Dabei werden die verschiedenen Vergrößerungen der Objektive dazu genutzt, eine Art Triage zwischen den Scores durchzuführen:
- Eine intensive Membranfärbung ist schon bei geringer Vergrößerung (2,5–5x Objektiv) deutlich erkennbar und entspricht IHC 3+.19
- Eine schwache bis mäßige Membranfärbung kann nur bei mittlerer Vergrößerung (10x–20x Objektiv) eindeutig identifiziert werden und entspricht IHC 2+.19
- Schwache Färbungen können nur mit einer höheren Vergrößerung (20–40x Objektiv) sicher erkannt werden19 und entsprechen einem IHC 1+ Ergebnis (HER2-low) oder „IHC 0 mit Membranfärbung“ (HER2-ultralow).
Zur Unterscheidung der für die IHC-Scores 1+ und 2+ maßgeblichen Tumorzellen muss neben der Färbeintensität auch die Vollständigkeit der Membranfärbung (Zirkularität) mit betrachtet werden:17
- Eine schwache, komplette Membranfärbung ist für IHC 2+ maßgeblich, während Tumorzellen mit einer schwachen, partiellen Membranfärbung als IHC 1+ bewertet werden.
- Sonderfälle sind u. a. drüsenbildende Tumoren, die ein U-förmiges Färbemuster aufweisen können, das dennoch als IHC 2+ zu bewerten ist und einer ISH-Analyse zugeführt werden muss.17
- Sind zytoplasmatische Anfärbungen oder lineare Färbungen nur im Bereich der Basalmembran zu beobachten, so sind diese nicht zu berücksichtigen und als ungefärbt für IHC 0 zu bewerten.17
In der Praxis wäre es sinnvoll, das Vorhandensein dieser begrenzten HER2-positiven Komponente im Bericht zu vermerken, um bei einem Rezidiv oder einer metastasierten Erkrankung im weiteren Krankheitsverlauf der Patientin/des Patienten eine sofortige exakte Neubewertung des HER2-Status vorzunehmen.17
Im letzten Schritt ist der Anteil Tumorzellen mit HER2-Expression zu bestimmen:17
- Sind keine Tumorzellen mit Membranfärbung zu finden (0 %), so werden Tumoren als „IHC 0 ohne Membranfärbung“ klassifiziert, was dem klinischen Status HER2-null entspricht.
- Eine schwache, partielle Membranfärbung bei ≤ 10 % der Tumorzellen wird als „IHC 0 mit Membranfärbung“ klassifiziert und entspricht dem klinischen Status „HER2-ultralow“.11 Ein HER2-ultralow Status liegt schon ab der ersten Tumorzelle mit Membranfärbung vor.
- Bei einer schwachen, partiellen Membranfärbung bei > 10 % der Tumorzellen wird vom Status IHC 1+ gesprochen, was dem klinischen Status „HER2-low“ entspricht.11
- Mit einer schwach bis mäßigen, kompletten Membranfärbung bei > 10 % der Tumorzellen gilt ein Tumor als IHC 2+, wofür zur weiteren Einordnung mittels ISH eine mögliche Amplifikation des HER2-Gens untersucht werden muss. Während Tumoren mit IHC 2+/ISH-negativ dann ebenfalls dem klinischen Status „HER2-low“ zugeordnet werden, gelten Tumoren mit IHC 2+/ISH-positiv hingegen als „HER2-positiv“.11
- Eine starke, komplette Membranfärbung bei > 10 % der Tumorzellen gilt als IHC 3+ und entspricht damit klinisch dem Status „HER2-positiv“.11
- Bei schwacher Membranfärbung und tubulärem oder lobulärem Wachstumsmuster kann es zu einer Unterschätzung der Tumorzellzahl und damit des IHC-Scores kommen.17 Im Zweifelsfall gilt es die Zellen blickfeldweise auszuzählen, um die Gesamtzahl der Tumorzellen und die Zahl gefärbter Tumorzellen besser zu bestimmen. Gegebenenfalls sollten Kolleg:innen um Mitbefundung gebeten werden oder auch eine Nachtestung am selben oder einem zweiten Tumorblock durchgeführt werden.17
HER2-Nachtestungen nicht immer zielführend
Eine Nachtestung bei uneindeutigen Ergebnissen kann mögliche technische Probleme ausschließen, führt jedoch häufig nicht zu einem eindeutigen Ergebnis.20 In der postanalytischen Phase können das Fehlen einer konsistenten internen epithelialen Positivkontrolle für HER2 in nicht-neoplastischem Brustgewebe, die intratumorale Heterogenität der HER2-Expression und die semiquantitative und subjektive Art der HER2-Bewertung zu einer hohen Diskordanz der IHC-Testergebnisse führen, insbesondere wenn sie von verschiedenen Patholog:innen bewertet werden.20
Reproduzierbarkeit der HER2-low Einstufung
Die Einstufung von HER2-low stellt in der täglichen diagnostischen Praxis eine Herausforderung dar, insbesondere im Hinblick auf ihre Reproduzierbarkeit. Verschiedene Studien haben gezeigt, dass die Abgrenzung zwischen den IHC-Kategorien, insbesondere im unteren Expressionsbereich, mit einer gewissen Unsicherheit behaftet ist.
In einer Untersuchung von Schettini et al.21 wurden 100 Brustkrebsfälle von fünf erfahrenen, auf Brustgewebe spezialisierten Patholog:innen gemäß den ASCO/CAP-Leitlinien von 20187 bewertet. Die Gesamtübereinstimmung war mit einem Kappa-Wert von 0,79 (p < 0,001) gut. Allerdings zeigten sich bei 35 Fällen Diskrepanzen, vor allem zwischen den Kategorien IHC 0 und 1+ (15 Fälle) sowie zwischen IHC 1+ und 2+ (12 Fälle).21
Eine größere Studie von Fernandez et al. analysierte 170 archivierte Brustkrebsbiopsien, die von 18 Patholog:innen aus 15 verschiedenen Einrichtungen neu bewertet wurden.22 Bei 92 Fällen, die von mindestens einer Person als IHC 0 klassifiziert wurden, erreichten nur 26 % (24/92) der Bewerter:innen eine Übereinstimmung von ≥ 90 %. Im Vergleich dazu lag die Übereinstimmung bei Fällen mit IHC 3+ deutlich höher bei 58 %, was die höhere Objektivierbarkeit starker HER2-Überexpression unterstreicht.22
Diese Ergebnisse verdeutlichen, dass die IHC-basierte Einordnung im HER2-low Bereich derzeit mit begrenzter Genauigkeit erfolgt und somit das Risiko einer Fehlklassifikation besteht – mit potenziellen Auswirkungen auf Therapieentscheidungen. Die Autor:innen schlagen vor, dass neue, sensitivere Assays sowie eine Standardisierung mittels Kalibrierungsobjektträgern zur Verbesserung der Reproduzierbarkeit beitragen könnten.22 Zudem gibt es Hinweise darauf, dass selbst kurze, gezielte Schulungen für Patholog:innen die Bewertungssicherheit in den Grenzbereichen zwischen IHC 0 und HER2-low signifikant verbessern können.23
HER2-ultralow kann ebenfalls herausfordernd sein
Während bereits die reproduzierbare Einstufung von HER2-low anspruchsvoll ist, stellt die Abgrenzung von HER2-ultralow von HER2-null manchmal eine noch größere diagnostische Herausforderung dar.
In einer aktuellen Studie wurden HER2 IHC-Objektträger von 50 Brustkrebs-Resektionspräparaten, die zuvor alle als IHC 0 klassifiziert worden waren, von 36 Patholog:innen erneut beurteilt.15 Trotz dieser gezielten Fragestellung wurde in nur 4 % der Fälle eine hohe Übereinstimmung bei der Differenzierung zwischen HER2-null und HER2-ultralow gefunden.24 Diese geringe Reproduzierbarkeit deutet darauf hin, dass die präzise Erkennung von HER2-ultralow in der Praxis noch besonders schwierig ist. Als Ursachen werden mehrere Faktoren diskutiert:
Die Unterscheidung basiert auf dem Vorhandensein oder Fehlen einer sehr schwachen, inkompletten Membranfärbung, die oft nur unter starker mikroskopischer Vergrößerung (40x) sichtbar ist.6,17,19
Bei der initialen Beurteilung unter geringer Vergrößerung könnten repräsentative Tumorbereiche übersehen worden sein, was zu einer Unterschätzung der HER2-ultralow Fälle führte.24
Zusätzlich beeinflussen individuelle Unterschiede in der Farbwahrnehmung, zytoplasmatische oder unspezifische Färbungen sowie das Fehlen klarer Referenzpunkte die konsistente Bewertung.24
KI-gestützte Bildanalysesoftware könnte helfen, u. a. die Abgrenzung zwischen HER2-null, HER2-ultralow und IHC 1+ objektiver und standardisierter zu gestalten und so die Patient:innen-Identifikation zu verbessern.24
Unterschiedliche Sensitivität der IHC-Assays
Die aktuell verfügbaren HER2 IHC-Testsysteme wurden ursprünglich entwickelt, um eine HER2-Überexpression nachzuweisen, die um das 100- bis 10.000-Fache über dem physiologischen Niveau normaler Brustepithelzellen liegt.25 Für die Detektion geringer HER2-Expressionslevel, wie sie bei HER2-low oder HER2-ultralow Tumoren vorliegen, sind diese Assays primär jedoch nicht optimiert.22,25,26
Ob bestimmte IHC-Testsysteme in der Lage sind, auch im unteren Expressionsbereich zuverlässigere und sensitivere Ergebnisse zu liefern, ist derzeit Gegenstand intensiver Diskussion. So berichteten Scott et al., dass der PATHWAY® HER-2/neu (Klon 4B5) einen höheren Anteil an HER2-low Fällen identifizierte als der HercepTest™.27 Demgegenüber zeigten Rüschoff et al., dass der neue monoklonale HercepTest™ mAb pharmDx (Klon DG44) im Vergleich zum etablierten Ventana PATHWAY® HER-2/neu (4B5) eine höhere Sensitivität bei der Detektion von HER2-low Tumoren (IHC 1+ oder IHC 2+/ISH-negativ) aufwies.28
Software zur KI-gestützten Bildanalyse
Voraussetzung für den Einsatz von KI-Software zur Bildanalyse sind hoch-aufgelöste, digitale Bilder ganzer Objektträger mit gefärbten Gewebeschnitten (WSI, Whole Slide Images). Mit dem Aufkommen neuer, leistungsfähiger Methoden für das sog. Machine Learning (ML) und Deep Learning (DL) haben verschiedene kommerzielle Anbieter KI-gestützte Bildanalysesoftware entwickelt. Sie eignen sich zur Mustererkennung (z. B. zur Identifizierung invasiver Tumorbereiche im Vergleich zum Stroma oder DCIS), zur reproduzierbaren Zellklassifizierung („schwach, partiell“ vs. „schwach, komplett“) und zum Auffinden nur sehr weniger abnormer Zellen („die Nadel im Heuhaufen finden“).29
Die KI-Software kann Tausende bis Millionen Tumorzellen in allen invasiven Tumorbereichen im gesamten Gewebe auf einem Objektträger automatisch detektieren, klassifizieren und quantifizieren. Damit unterstützt sie Patholog:innen bei repetitiven Aufgaben wie dem Auszählen von Zellen und hilft die Tumorheterogenität besser abzudecken, die Reproduzierbarkeit zu erhöhen und die IHC-Diagnostik insgesamt weiter zu standardisieren.29

Verschiedene kommerzielle Anbieter bieten heute entsprechende KI-Software zur Unterstützung des Scorings von IHC-Biomarkern mit Zulassung als Medizinprodukt (CE-IVD) für den klinischen Einsatz an. Für das HER2-Scoring bei Brustkrebs haben AstraZeneca und Daiichi Sankyo mit Ibex Medical Analytics eine Vereinbarung über die Entwicklung, klinische Validierung und Einführung einer solchen KI-Software geschlossen.30
Neuartige HER2-Assays

Aktuell werden außerdem neuartige quantitative Assays entwickelt, welche die Identifizierung von Patient:innen mit HER2-low und HER2-ultralow Brustkrebs verbessern sollen, u. a. immunfluoreszenzbasierte, automatisierte, quantitative Analyseverfahren und quantitative IHC-Testsysteme.31 Darüber hinaus könnte die Evaluation der HER2 mRNA-Expressionsniveaus eine mögliche Ergänzung oder Alternative zur IHC/ISH darstellen, um abzuschätzen, welche Patient:innen von der Therapie profitieren könnten.31 Allerdings müssen all diese neuen Methoden zum HER2-Nachweis noch umfassend analytisch und klinisch validiert werden, bevor sie Eingang in die klinische Praxis finden können.
Was bringt ein Training für die HER2-Diagnostik: HER2-low?
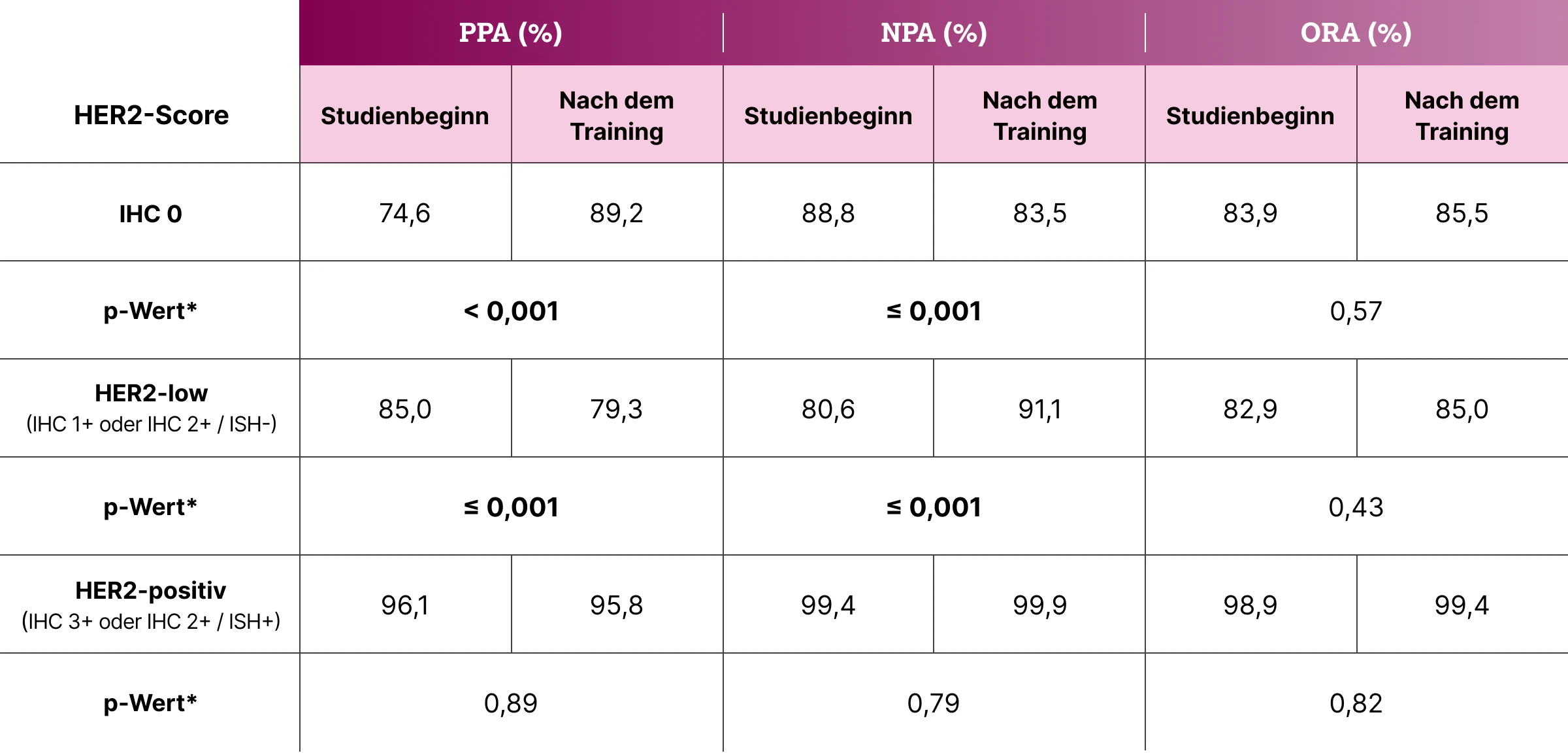
*Gemäß Chi-Quadrat-Statistik und Chi-Quadrat-Statistik mit Yates-Korrektur, Signifikanz bei p < 0,05; signifikante p-Werte fett dargestellt
In einer weltweiten Praxisstudie haben Rüschoff et al. untersucht, wie sich ein Training von Patholog:innen auf die Ergebnisse der HER2-low Interpretation auswirkt.23 Dazu wurde die Kompetenz von 77 Patholog:innen aus 14 Ländern in Bezug auf die Unterscheidung von HER2-low (IHC 1+ und IHC 2+/ISH-negativ) und IHC 0 vor und nach einem vierstündigen virtuellen Training mit digitalisierten IHC-Schnitten (WSI, Whole Slide Images) bewertet.23
Die Übereinstimmung in der HER2-low Kategorie lag sowohl für den PATHWAY® 4B5 Assay (Ventana) als auch für den HercepTest™ (Dako) über dem Overall Rater Agreement (ORA) Benchmark von 80 %,23 was höher war als z. B. in der Studie von Fernandez et al.22
Durch das Training verbesserte sich die Fähigkeit von Patholog:innen, Fälle mit IHC 0 von HER2-low zu unterscheiden und korrekt zu identifizieren:
Vor der Schulung wurden 74,6 % der Tumoren mit IHC 0 korrekt diagnostiziert, nach der Schulung waren es 89,2 % (p < 0,001), was sowohl eine Verbesserung der positiven prozentualen Übereinstimmung (PPA) als auch eine Verringerung der falsch-positiven Bewertungen bedeutet. Die negative prozentuale Übereinstimmung (NPA) bei der HER2-low Bewertung verbesserte sich nach dem Training für den 4B5-Test auch von 80,6 % auf 91,1 % (p < 0,001).23

Das zeigt, dass Patholog:innen schon nach einem kurzen, zielgerichteten Training ein hohes Maß an Präzision bei der Identifizierung von HER2-low Patient:innen erzielen können.23
Abkürzungen
ADC: Antikörper-Wirkstoff-Konjugat; ASCO: American Society of Clinical Oncology; CAP: College of American Pathologists; CEP: Chromosome Enumerating Probe; CE-IVD: CE-Kennzeichnung für In-vitro-Diagnostika; DCIS: duktales Carcinoma in situ; DL: Deep Learning; ESMO: European Society for Medical Oncology; FOV: Gesichtsfeld; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HR: Hormonrezeptor; IHC: Immunhistochemie; ISH: In-situ-Hybridisierung; KI: Künstliche Intelligenz; mRNA: messenger-Ribonukleinsäure; ML: maschinelles Lernen; NA: unzutreffend/nicht verfügbar; NPA: negative prozentuale Übereinstimmung; ORA: Gesamtübereinstimmung der Bewertenden; PPA: positive prozentuale Übereinstimmung; WSI: Whole Slide Images
- Agilent DAKO. HercepTest™ Interpretation Manual Breast Cancer. Verfügbar unter agilent.com/cs/library/usermanuals/public/28630_herceptest_interpretation_manual-breast_ihc_row.pdf. Letzter Zugriff: Februar 2026.
- Roche VENTANA. PATHWAY anti-HER-2/neu (4B5) Rabbit Monoclonal Primary Antibody Interpretation Guide for Breast Cancer. Verfügbar unter accessdata.fda.gov/cdrh_docs/pdf/P990081S047D.pdf. Letzter Zugriff: Februar 2026.
- Leica Biosystems. Bond™ Oracle™ HER2 IHC System Gebrauchsanleitung. Verfügbar unter leicabiosystems.com/sites/default/files/2020-10/Bond_Oracle_HER2_IHC_System_TA9145_ROW-DE-CE_Rev_D.pdf. Letzter Zugriff: Februar 2026.
- DAKO Omnis. HER2 IQFISH pharmDX™. Verfügbar unter agilent.com/cs/library/packageinsert/public/127859001.PDF. Letzter Zugriff: Februar 2026.
- Roche Diagnostics. VENTANA HER2 Dual ISH Assay. Verfügbar unter roche.de/diagnostik/produkte-loesungen/tests-parameter/ventana-dual-colour-ish. Letzter Zugriff: Februar 2026.
- Wolff AC, et al. J Clin Oncol 2023;41(22):3867-72.
- Wolff AC, et al. J Clin Oncol 2018;36(20):2105–22.
- Yi Z, et al. NPJ Breast Cancer 2020;6:59.
- Bardia A, et al. N Engl J Med 2024(391):2110–22 inkl. Supplement.
- Modi S, et al. N Engl J Med 2022;387(1):9–20.
- Tarantino P, et al. Ann Oncol 2023;34(8):645–59.
- S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 5.0, Dez 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mammakarzinom_4_0/Version_5/LL_Mammakarzinom_Langversion_5.0.pdf. Letzter Zugriff: Februar
- Fachinformation ENHERTU®. März 2025.
- Zhang H, et al. Am J Clin Pathol 2022;157(3):328–36.
- Ivanova M, et al. Virchows Arch 2024;484(1):3–14.
- Venetis K, et al. Front Mol Biosci 2022;9:834651.
- Denkert C, et al. Pathologie (Heidelb) 2023;44(Suppl 2):53–60.
- Bornstein-Quevedo L, et al. J Pers Med 2024;14(5):467.
- Scheel AH, et al. Diagn Pathol 2018;13(1):19.
- Sajjadi E, et al. Cancer Drug Resist 2022;5(4):882–8.
- Schettini F, et al. NPJ Breast Cancer 2021;7(1):1–13.
- Fernandez AI, et al. JAMA Oncol 2022;8(4):1–4.
- Rüschoff J, et al. Arch Pathol Lab Med 2025;149(5):431–8.
- Wu S, et al. ESMO Open 2025;10(2):104127.
- Baez-Navarro X, et al. Eur J Cancer 2022;175:187–92.
- Xu K, et al. J Mol Diagn 2022;24(7):775–83.
- Scott M, et al. J Clin Oncol 2021;39(15_suppl):1021.
- Rüschoff J, et al. Virchows Arch 2022;481(5):685–94.
- Albuquerque DAN, et al. NPJ Digit Med 2025;8(1):144.
- Kemp A; 2019. Verfügbar unter https://www.astrazeneca.com/media-centre/press-releases/2019/astrazeneca-and-daiichi-sankyo-enter-collaboration-for-novel-her-2-targeting-antibody-drug-conjugate.html#. Letzter Zugriff: Februar 2026.
- Nicolò E, et al. Ther Adv Med Oncol 2023;15:17588359231152842.

