KEAP1 beim Lungenkarzinom
Bedeutung und Prävalenz von KEAP1 beim NSCLC
KEAP1-Mutationen beim NSCLC
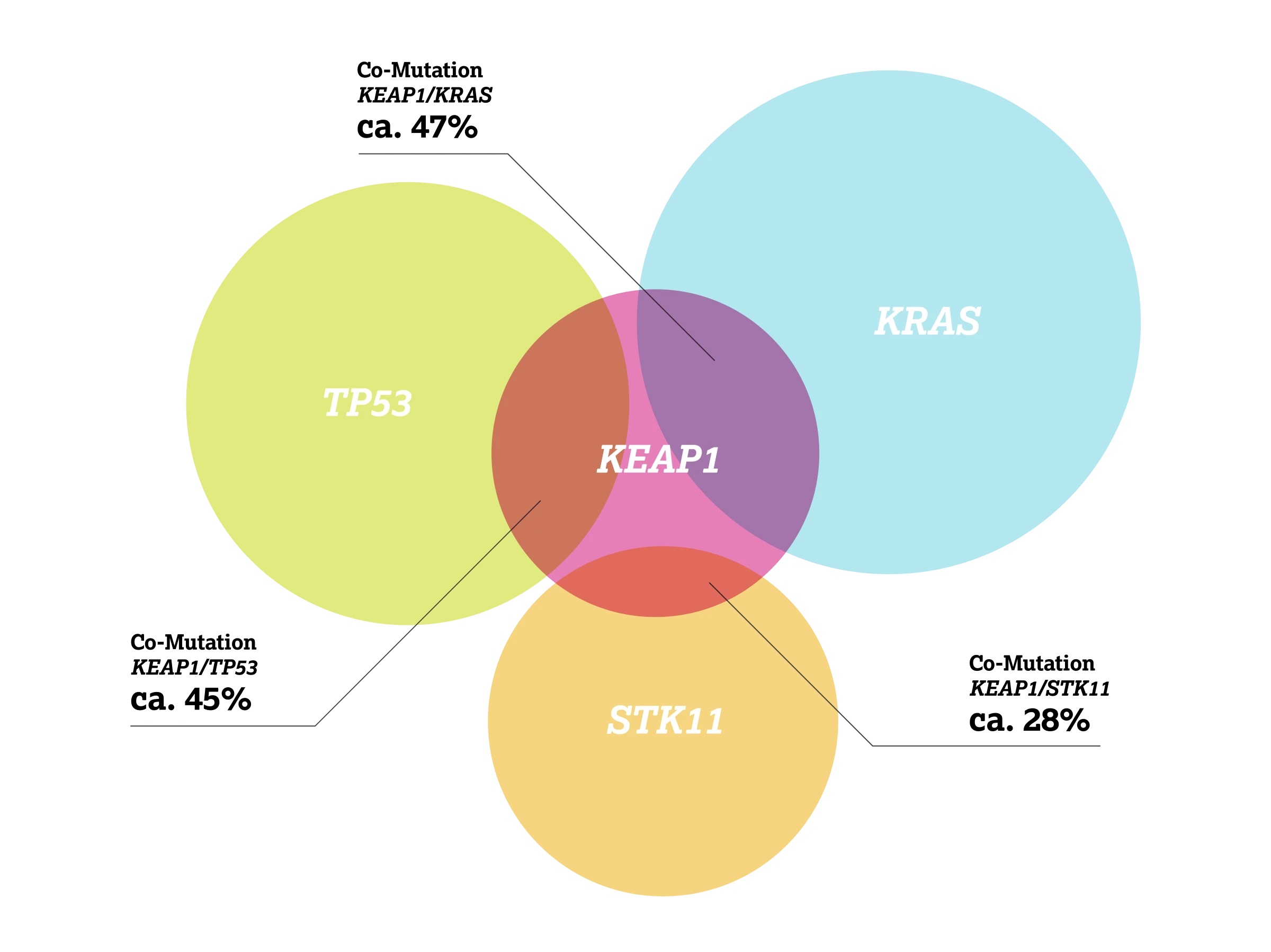
Loss-of-function-Mutationen im Tumorsuppressor-Gen KEAP1 treten bei Patient:innen mit fortgeschrittenem nicht-kleinzelligen Lungenkarzinom (NSCLC) in etwa 11–27 % der Fälle auf, abhängig von der Studie.1 Diese Mutationen zeigen eine hohe Rate an Co-Mutationen, z. B. im TP53-Gen bei etwa 45 %, im KRAS-Gen bei bis zu 47 % oder im STK11-Gen bei 28 % der untersuchten KEAP1-mutierten NSCLC-Tumoren.1
Solche genetischen Veränderungen wurden sogar im histologisch unauffälligen Atemwegsepithel von Patient:innen mit frühem NSCLC nachgewiesen.2 KEAP1-Mutationen wurden auch schon zusammen mit MET-Amplifikationen (18 %) oder EGFR-Mutationen (6 %) detektiert.1
Mutationen in KEAP1 und NFE2L2 (kodierend für NRF2) treten in der Regel nicht gemeinsam auf – ein Hinweis auf funktionelle Redundanz im oxidativen Stress-Response-Signalweg.1

Informationen zum Wirkmechanismus von KEAP1.
KEAP1-Mutationen führen zu „kalten“ Tumoren
KEAP1-mutierte NSCLC-Tumoren zeichnen sich durch ein supprimiertes Immunmilieu aus und gelten immunologisch als „kalte“ Tumoren.1,3 In diesen Tumoren sind zentrale Immunzellpopulationen – darunter B-Zellen, CD4⁺- und CD8⁺-T-Zellen, dendritische Zellen, Makrophagen und neutrophile Granulozyten – signifikant reduziert.3 Diese immunologische Inaktivität hat klinische Relevanz, insbesondere im Hinblick auf eine reduzierte Ansprechrate auf Immuncheckpoint-Inhibitoren wie PD-L1 Blocker.3
Diese Ergebnisse unterstreichen den potenziellen Nutzen einer erweiterten molekularen Diagnostik: Die routinemäßige Integration von KEAP1- und STK11-Analysen in NGS-Panels kann eine sinnvolle Ergänzung zur umfassenden molekularen Charakterisierung von NSCLC darstellen.14

Informationen zu „kalten" Tumoren und deren Reprogrammierung.
Studien & Leitlinienempfehlungen zur KEAP1-Testung beim Lungenkarzinom
KEAP1 als potenzieller Biomarker beim NSCLC
KEAP1-mutierte NSCLC-Tumoren zeichnen sich durch ein supprimiertes Immunmilieu aus und gelten immunologisch als „kalte“ Tumoren.1,3 In diesen Tumoren sind zentrale Immunzellpopulationen – darunter B-Zellen, CD4⁺- und CD8⁺-T-Zellen, dendritische Zellen, Makrophagen und neutrophile Granulozyten – signifikant reduziert.3 Diese immunologische Inaktivität hat klinische Relevanz, insbesondere im Hinblick auf eine reduzierte Ansprechrate auf Immuncheckpoint-Inhibitoren wie PD-L1 Blocker.3
Diese Ergebnisse unterstreichen den potenziellen Nutzen einer erweiterten molekularen Diagnostik: Die routinemäßige Integration von KEAP1- und STK11-Analysen in NGS-Panels kann eine sinnvolle Ergänzung zur umfassenden molekularen Charakterisierung von NSCLC darstellen.14
Abkürzungen
CD4⁺: T-Helferzellen (CD4-positive T-Lymphozyten); CD8⁺: Zytotoxische T-Zellen (CD8-positive T-Lymphozyten); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); KEAP1: Kelch-like ECH-associated protein 1 (Gen); KRAS: Kirsten Rat Sarcoma (Gen); MAPK: Mitogen-aktivierte Proteinkinase; MET: Mesenchymal-epithelialer Transitionsfaktor (Gen); NFE2L2: Nuclear factor, erythroid 2-like 2 (Gen); NGS: Next-Generation-Sequencing; NRF2: Nuclear factor erythroid 2-related factor 2; NSCLC: nicht-kleinzelliges Lungenkarzinom; OS: Gesamtüberleben; PD-1: Programmed cell death-1; PD-L1: Programmed cell death ligand-1; PFS: Progressionsfreies Überleben; RTK: Rezeptortyrosinkinase; STK11: Serin/Threonin-Kinase 11 (Gen); TP53: Tumorsuppressor-Protein P53 (Gen)
- Di Federico A, et al. Eur J Cancer 2021;157:108–13.
- Kadara H, et al. Am J Respir Crit Care Med 2019;200(6):742–50.
- Cheng W, et al. Thorac Cancer 2021;12(18):2458–67.
- Proulx-Rocray F, et al. Cancer Treat Res Commun 2023;37:100767.
- Arbour KC, et al. Clin Cancer Res 2018;24(2):334–40.
- Ricciuti B, et al. J Thorac Oncol 2022;17(3):399–410.
- Saleh MM, et al. J Thorac Oncol 2022;17(1):76–88.
- Mograbi B, et al. Diagnostics (Basel) 2021;11(2):196.
- Papillon-Cavanagh S, et al. ESMO Open 2020;5(2):e000706.
- Zhu H, et al. Front Oncol 2021;11:659200.
- Shiller M, et al. Front Oncol 2024;14:1459737.
- Scalera S, et al. J Thorac Oncol 2022;17(6):751–7.
- Peters S, et al. Journal of Thoracic Oncology 2022;17(9):S39-S41.
- Skoulidis F, et al. Nature 2024;635(8038):462–71.