Therapiemöglichkeiten bei einem veränderten PD-L1 Status
Der PD-L1 Status ist wegweisend für die Behandlungsauswahl, insbesondere für den Einsatz immunbasierter Therapien bei fortgeschrittenen soliden Tumoren – etwa beim NSCLC.1 Insbesondere eine erhöhte PD-L1 Expression ist ein prädiktiver Marker für das potenzielle Ansprechen auf Immuncheckpoint-Inhibitoren (ICI). Grundlage dieses Konzepts ist die Reaktivierung zytotoxischer T-Zellen, deren Aktivität im Tumormikromilieu häufig durch inhibitorische Signale unterdrückt wird.2
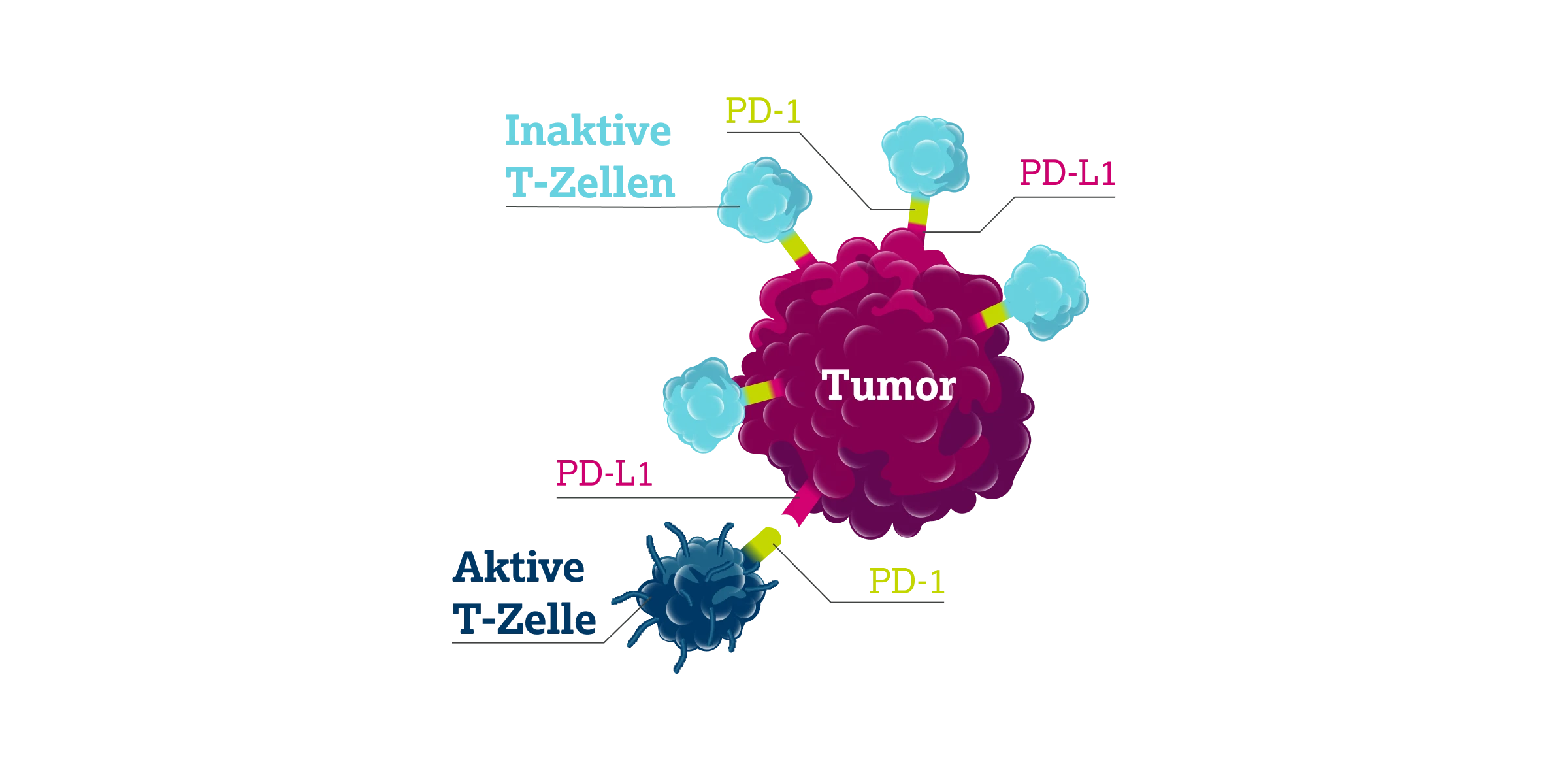
Grundprinzip der Immuncheckpoint-Inhibition
Im Mittelpunkt steht die Interaktion zwischen dem inhibitorischen Rezeptor PD-1 auf aktivierten T-Lymphozyten und seinem Liganden PD-L1, welcher auf Tumorzellen sowie antigenpräsentierenden Zellen exprimiert werden kann. Die Bindung von PD-L1 an PD-1 führt zu einer funktionellen Suppression der T-Zell-Antwort, u. a. durch Inhibition der Proliferation, verminderte Zytokinfreisetzung und eine reduzierte zytotoxische Aktivität. Tumorzellen nutzen diesen Mechanismus aktiv zur Immunevasion, insbesondere durch konstitutive oder inflammatorisch induzierte PD-L1 Expression.
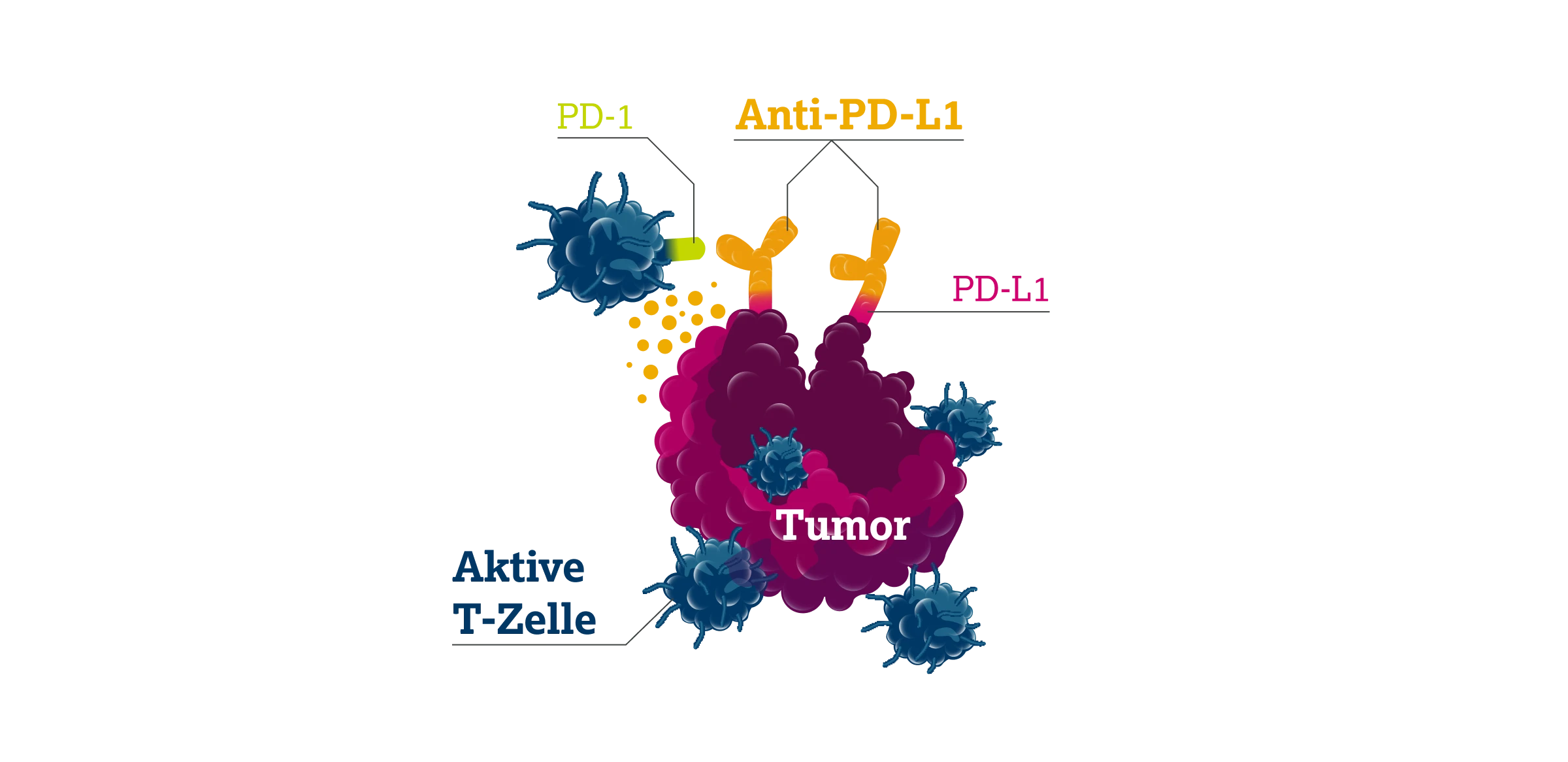
Immuncheckpoint-Inhibitoren (ICI) – monoklonale Antikörper gegen PD-1, PD-L1 oder CTLA-4 – blockieren diese inhibitorischen Signale. Durch die gezielte Unterbrechung der PD-1/PD-L1 Achse wird Aktivität körpereigener T-Zellen gegen Tumorzellen wiederhergestellt und die immunvermittelte Tumorabwehr gestärkt.
PD-L1 Expression im kurativen Therapiekontext
Neben der palliativen Therapiesituation hat sich die Immuncheckpoint-Inhibition auch in der kurativ intendierten Behandlung etabliert.4 Neue Real-World-Daten zeigen darüber hinaus: Bei hoher PD-L1 Expression (≥ 50 %) führt die Kombination aus Immuncheckpoint-Inhibition und platinbasierter Chemotherapie häufiger zu einem frühzeitigen Überlebensvorteil als eine Monotherapie. Diese Erkenntnisse unterstützen den Trend zur Kombinationstherapie auch in frühen Stadien bei geeigneter Expression.5
Relevanz der PD-L1 Expression für Diagnostik und Therapieplanung
Für die pathologische Diagnostik ist die präzise Bestimmung der PD-L1 Expression essenziell, da sie sowohl prädiktive als auch prognostische Relevanz besitzt. Die Bewertung erfolgt standardisiert über den Tumor Proportion Score (TPS). Ein Cut-off von ≥ 1 % gilt derzeit in vielen Zulassungen als minimaler Schwellenwert für den Einsatz einer Immuntherapie beim NSCLC.1 Ein TPS ≥ 50 % gilt in vielen Zulassungen als Schwellenwert für eine Immunmonotherapie und ist mit einer höheren Wahrscheinlichkeit für ein Ansprechen assoziiert.1
Umgekehrt können auch Patient:innen mit niedriger (< 1 %) oder fehlender PD-L1 Expression von einer Kombinationstherapie aus ICI und Chemotherapie profitieren – vorausgesetzt, Treibermutationen wie z. B. EGFR oder ALK wurden molekularpathologisch ausgeschlossen.1
Neuere Studiendaten zeigen zudem, dass die PD-L1 Bestimmung auch im perioperativen Setting ab Stadium II des NSCLC an Bedeutung gewinnt. Hier kann sie helfen, Patient:innen zu identifizieren, die von einer ergänzenden immunonkologischen Therapie im Rahmen einer neoadjuvanten oder adjuvanten Behandlungsstrategie profitieren könnten.6
Diese Konstellationen unterstreichen die Bedeutung einer präzisen PD-L1 Diagnostik in Verbindung mit einer umfassenden molekularen Charakterisierung des Tumors für die therapeutische Entscheidungsfindung.

Informationen zur Auswertung und Befundung des PD-L1 Status beim Lungenkarzinom
Zusätzliche Biomarker mit Einfluss auf das Immuntherapie-Ansprechen
Das therapeutische Ansprechen auf Immuncheckpoint-Inhibitoren wird nicht allein durch die PD-L1 Expression bestimmt. Weitere molekulare Marker liefern ergänzende Informationen mit prognostischer und prädiktiver Relevanz. So ist eine hohe Tumormutationslast (TMB) mit einer erhöhten Wahrscheinlichkeit für ein Ansprechen auf Immuntherapie assoziiert – insbesondere im Kontext eines Rauchverhaltens.1
Demgegenüber gelten molekulare Alterationen in STK11 und KEAP1 als ungünstige prognostische Marker.7,8 Darüber hinaus konnte gezeigt werden, dass insbesondere das gleichzeitige Vorliegen von STK11- und KEAP1-Mutationen mit einer deutlich reduzierten Wirksamkeit von PD-(L)1 Inhibitoren assoziiert sein kann.9 Auch KRAS-Mutationen – v. a. in Kombination mit STK11- oder KEAP1-Veränderungen – beeinflussen das Therapieansprechen.8,10
Darüber hinaus spielen klinische Parameter eine Rolle: Ein positiver Rauchstatus, männliches Geschlecht sowie das Fehlen therapierbarer Onkogene wie EGFR- oder ALK-Rearrangements korrelieren mit einem besseren Ansprechen auf ICI-basierte Therapien.10,11

Informationen zur Auswertung und Befundung des PD-L1 Status beim Lungenkarzinom
Abkürzungen
ALK: anaplastische Lymphomkinase (Gen); CTLA-4: Cytotoxic T-Lymphocyte Antigen 4; EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); ICI: Immuncheckpoint-Inhibitoren; KEAP1: Kelch-like ECH-associated protein 1 (Gen); KRAS: Kirsten Rat Sarkoma (Gen); NSCLC: nicht-kleinzelliges Lungenkarzinom; PD-1: Programmed cell death-1; PD-L1: Programmed cell death ligand-1; STK11: Serin/Threonin-Kinase 11 (Gen); TMB: Tumormutationslast; TPS: Tumor Proportion Score
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: November 2025.
- Wu Y, et al. Front Immunol 2019;10:2022.
- Nishino M, et al. Nat Rev Clin Oncol 2017;14(11):655–68.
- Paz-Ares L, et al. Ann Oncol 2020;31(6):798–806.
- Hektoen HH, et al. ESMO Open 2025;10(5):105073.
- Heymach JV, et al. N Engl J Med 2023;389(18):1672–84.
- Chen X, et al. Ann Transl Med 2020;8(4):141.
- Papillon-Cavanagh S, et al. ESMO Open 2020;5(2):e000706.
- Ricciuti B, et al. J Thorac Oncol 2022;17(3):399–410.
- Di Federico A, et al. J Natl Cancer Inst 2023;115(1):29–42.
- Gainor JF, et al. Clin Cancer Res 2016;22(18):4585–93.




