EGFR beim Lungenkarzinom
Bedeutung und Prävalenz von EGFR beim Lungenkarzinom
Aktivierende Mutationen im epidermalen Wachstumsfaktor-Rezeptor-Gen (EGFR) zählen zu den wichtigsten molekularen Alterationen beim nicht-kleinzelligen Lungenkarzinom (NSCLC). Sie sind insbesondere beim Lungenadenokarzinom von hoher klinischer Relevanz, da sie eine zielgerichtete Therapie ermöglichen und damit die Prognose betroffener Patient:innen erheblich verbessern.1
Regionale und demografische Unterschiede in der EGFR-Prävalenz
Weltweit weist etwa ein Drittel der NSCLC-Patient:innen eine EGFR-Mutation auf, wobei regionale Unterschiede deutlich ausgeprägt sind.1 In westlichen Ländern liegt die EGFR-Prävalenz bei etwa 10–15 % der NSCLC-Patient:innen,2 in asiatischen Populationen hingegen bei 40–60 %.3
In einer Metaanalyse mit 456 Studien und 115.815 an NSCLC erkrankten Personen traten EGFR-Mutationen insgesamt mit einer Prävalenz von 32,3 % auf.1 Diese variierte in den verschiedenen Stadien des NSCLC nur geringfügig. Betrachtet man die Prävalenz allerdings nach verschiedenen Regionen, zeigen sich deutliche Unterschiede mit höheren Prävalenzen in Asien als in Amerika und Europa.1
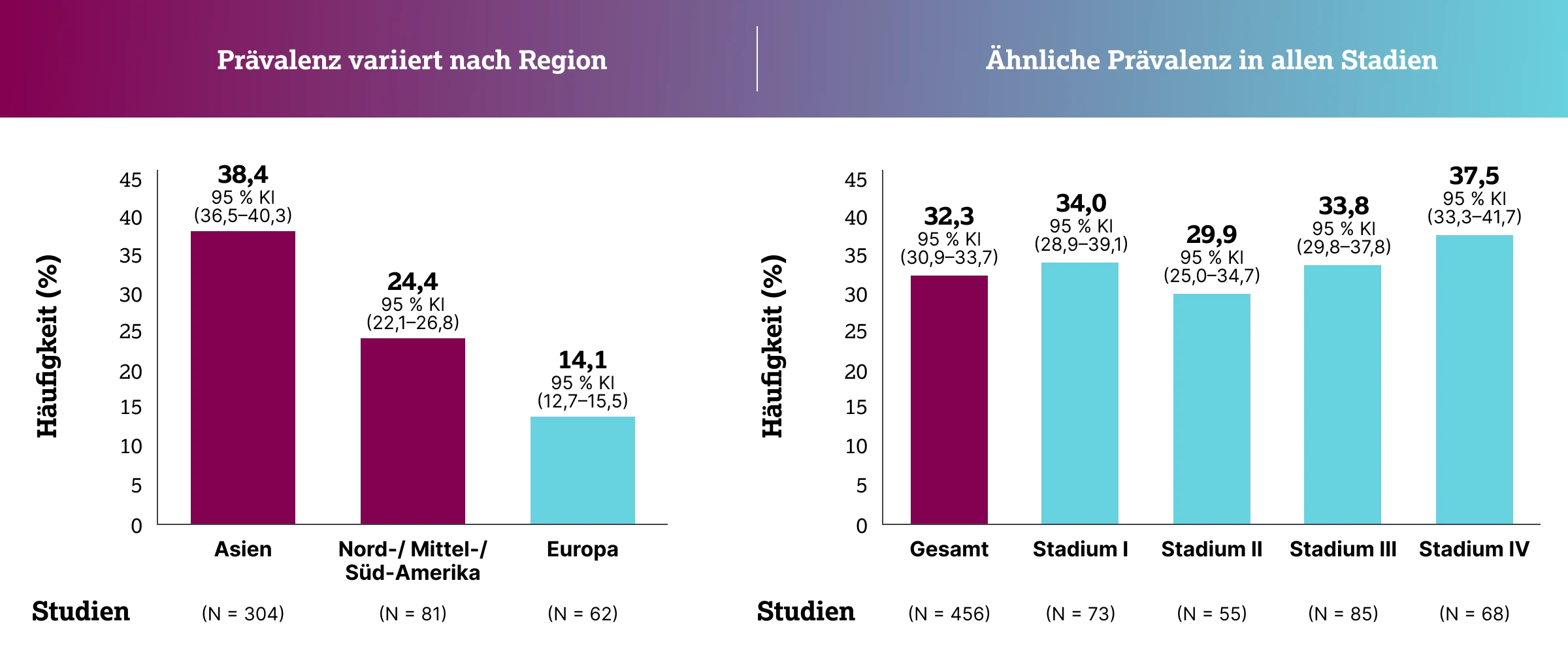
Auch demografische und patientenspezifische Merkmale sind mit einer erhöhten EGFR-Mutationshäufigkeit assoziiert:1
Frauen:
43,7 %
Nichtraucher:innen:
49,3 %
Patient:innen mit Adenokarzinom:
38,0 %
Im Vergleich dazu sind die Prävalenzraten bei Männern (24,0 %), Raucher:innen (21,5 %) und Nicht-Adenokarzinomen (11,7 %) deutlich geringer.1
EGFR im Kontext anderer molekularer Alterationen
Es wird geschätzt, dass bei der Diagnose insgesamt 50 % bis 60 % der Patient:innen mit fortgeschrittenem NSCLC eine behandelbare Treibermutation aufweisen – ähnliche Schätzungen liegen für Erkrankungen im Frühstadium vor.4 Die Häufigkeit wichtiger Treibermutationen veranschaulicht folgendes Tortendiagramm:
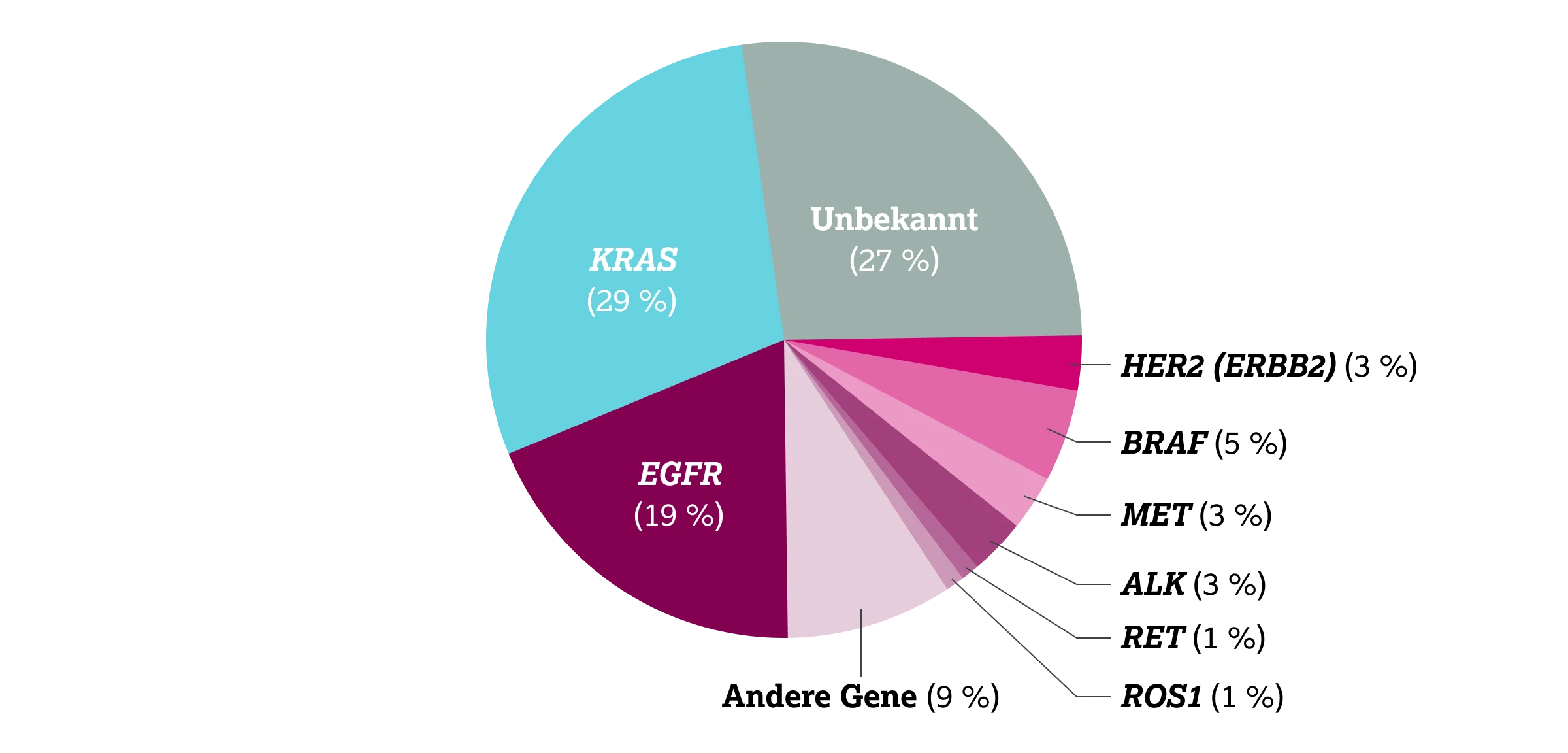
Diese Übersicht zeigt: EGFR gehört zu den häufigsten therapierelevanten molekularen Biomarkern beim NSCLC und sollte integraler Bestandteil jedes diagnostischen Panels sein.
Neben EGFR-Mutationen (inkl. TKI-sensitiver Varianten) finden sich häufig KRAS-Mutationen [KRAS-Mutation links to: article 1.2.4. KRAS beim Lungenkarzinom], die derzeit noch eingeschränkt therapeutisch adressierbar sind. Weitere therapierbare Alterationen betreffen u. a. die Biomarker ALK, ROS1, RET, MET, BRAF, HER2 (ERBB2) [HER2 (ERBB2) links to: article 1.2.7 HER2 beim Lungenkarzinom] und NTRK1. Ein relevanter Anteil der Tumoren bleibt bislang molekular unklassifiziert, was den Bedarf an umfassender molekularpathologischer Testung unterstreicht.6
Häufige (typische) EGFR-Mutationen
Etwa 85 % der EGFR-Mutationen entfallen auf zwei molekulare Subtypen:7
- Exon-19-Deletionen und
- L858R-Punktmutation im Exon 21
Diese sog. klassischen oder typischen Mutationen (common mutations) befinden sich in der Nähe der ATP-Bindungstasche und verringern die Affinität des Rezeptors für ATP, was in der Folge zu einer ligandenunabhängigen Aktivierung des EGFR-Rezeptors und einer erhöhten Migration, Proliferation und apoptotischen Resistenz von Krebszellen führt.8
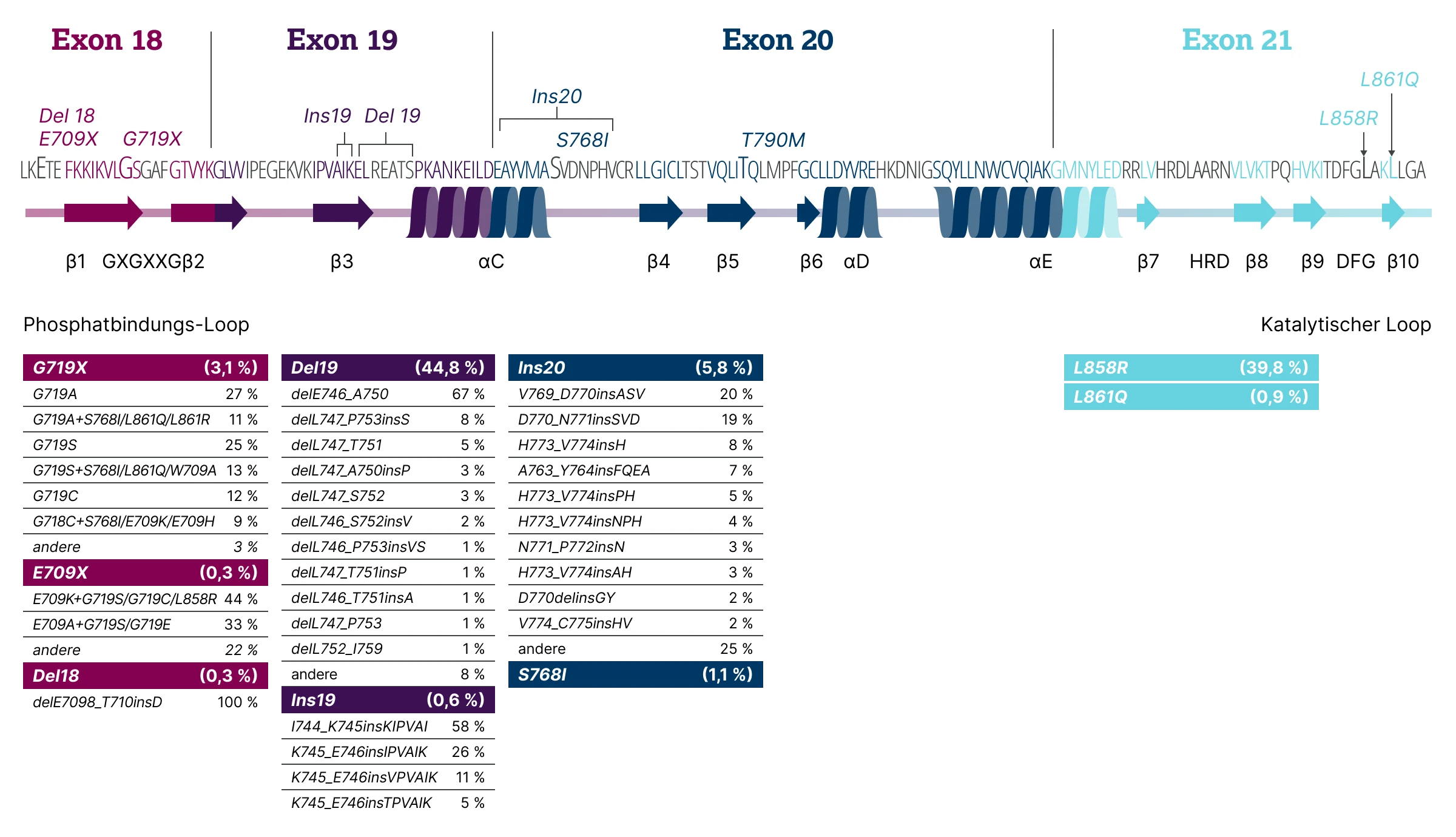
Die Darstellung basiert auf einer Auswertung aktueller groß angelegter Studien. Die Codons repräsentativer Mutationen sind auf der Proteinsequenz der EGFR-Kinasedomäne verortet. Codons in den Exons 18, 19, 20 und 21 sind farblich unterschiedlich hervorgehoben; Spiralstrukturen symbolisieren Alpha-Helices, dicke Pfeile stehen für Beta-Faltblätter.
Seltene (atypische) EGFR-Mutationen
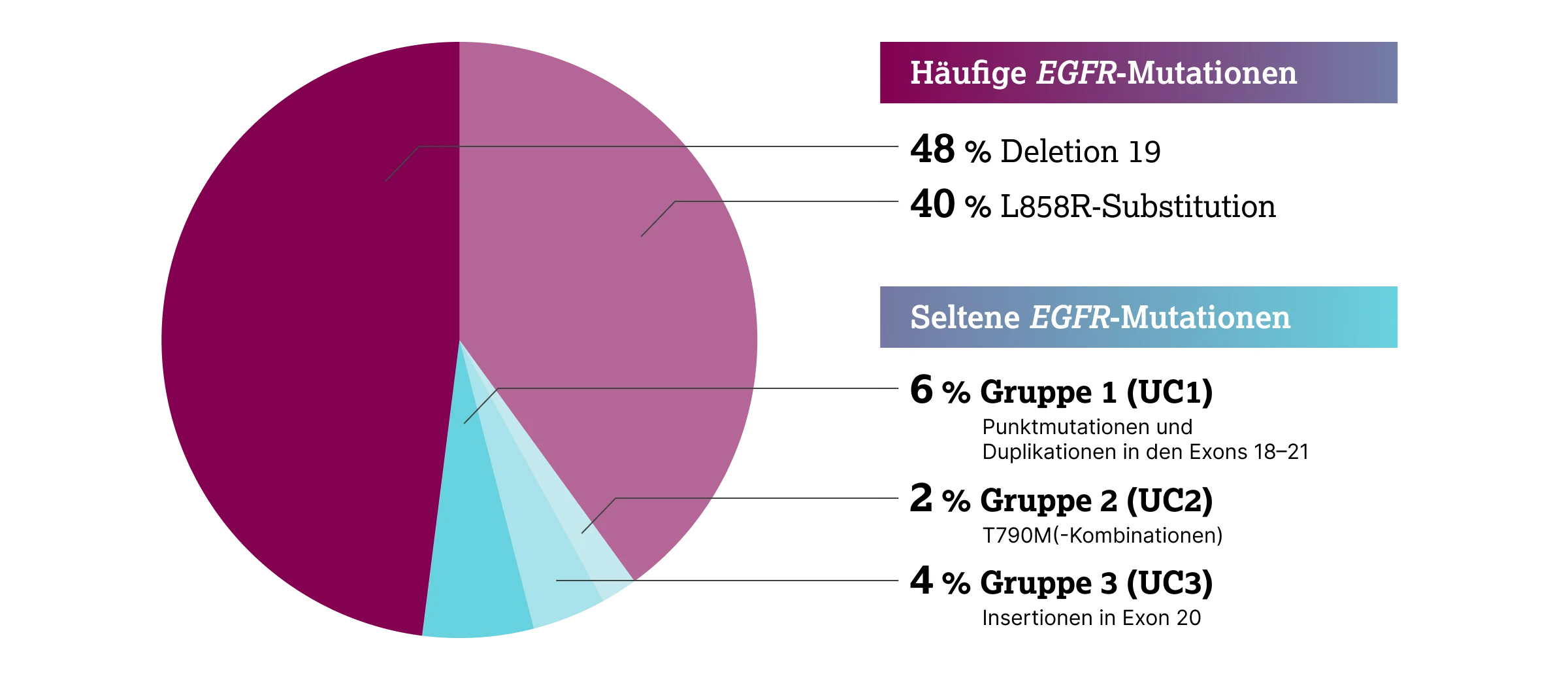
Die übrigen ~15 % der Mutationen gelten als selten oder atypisch (uncommon) und umfassen eine heterogene Gruppe von Punktmutationen, Insertionen und Deletionen in den Exons 18–21 der EGFR-Kinasedomäne.7 Neben diesen unterscheidet man als spezielle Untergruppe auch die EGFR-Kinasedomänen-Duplikationen (EGFR-KDD), bei denen eine in-frame-Tandemduplikation der Exons 18–25 bzw. 18–26 vorliegt, wodurch die komplette Kinasedomäne des EGFR-Gens verdoppelt wird.7
Diese seltenen Mutationen werden auf Basis ihrer funktionellen und therapeutischen Eigenschaften in die Untergruppen UC1–UC3 eingeteilt.9
Zur Gruppe UC 1 gehören:2
- komplexe Mutationen, die eine klassische (del19 oder L858R) EGFR-Mutation enthalten
- G719X-, L861Q- und S768I-Mutation allein oder komplex mit atypischen EGFR-Mutationen
- Exon-19-Insertionsmutationen
- spezifische Exon-20-Insertionsmutationen
- spezifische, sehr seltene Punktmutationen.
Bei der Punktmutation T790M in Exon 20 handelt es sich um eine sogenannte Resistenzmutation, da sie meist als Resistenz unter der Therapie mit einem EGFR-TKI der 1. und 2. Generation vorkommt.2 Häufig liegen diese Mutationen in Kombinationen mit anderen EGFR-Mutationen vor.2
Diese Gruppe ist mit über 60 verschiedenen Mutationen äußerst heterogen.2 Exon-20-insertionsspezifische EGFR-TKIs befinden sich aktuell in der klinischen Entwicklung.2
In diese Gruppe fallen alle anderen seltenen EGFR-Mutationen, insbesondere sehr seltene Punktmutationen der Exons 18–21 des EGFR.2
Häufigkeit von EGFR-Mutationen in frühen und späten Stadien
In einer monozentrischen Beobachtungsstudie aus Deutschland wurden bei NSCLC-Adenokarzinomen im Frühstadium (Stadium I–IIIA) bei 72,2 % der EGFR-mutierten Tumoren häufige EGFR-Mutationen nachgewiesen. Darunter fanden sich in 45,8 % der Fälle Exon-19-Deletionen und in 26,4 % L858R-Substitutionen.10 Seltene EGFR-Mutationen traten in 19,4 % der Fälle auf; bei 8,3 % lagen kombinierte Mutationen vor.10 Die Klassifikation nach Yang et al. ergab eine Zuordnung seltener Mutationen zu Gruppe I in 9,7 %, zu Gruppe II in 0 % und zu Gruppe III in weiteren 9,7 % der Fälle.10
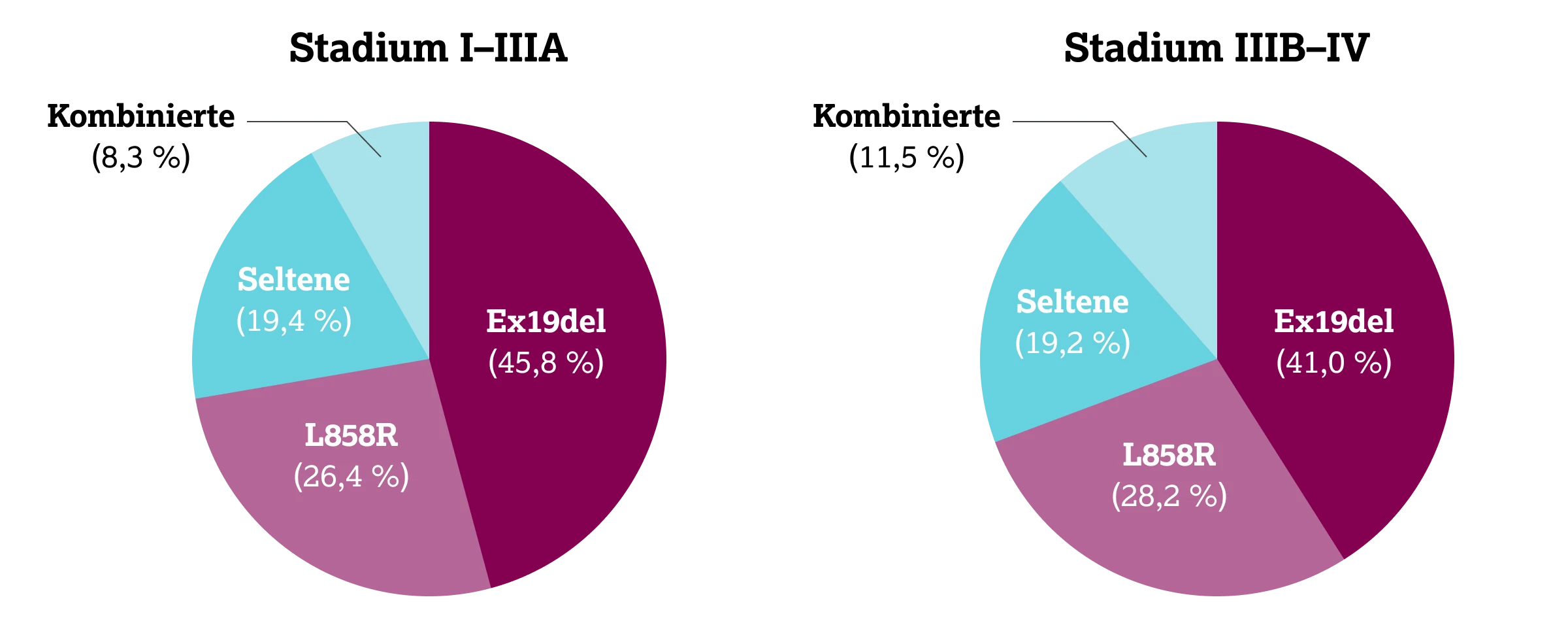
In den fortgeschrittenen Stadien (Stadium IIIB-IV) zeigten 69,2 % der EGFR-mutierten Adenokarzinome häufige Mutationen, mit 41,0 % Exon-19-Deletionen und 28,2 % L858R-Substitutionen. Seltene Mutationen wurden in 19,2 % der Fälle detektiert, davon 10,3 % in Gruppe I, keine in Gruppe II und 9,0 % in Gruppe III. Kombinierte Mutationen traten bei 11,5 % der Patient:innen auf. 10
Insgesamt entsprach die Verteilung der EGFR-Subtypen in frühen NSCLC-Stadien der in fortgeschrittenen Stadien. Es zeigte sich jedoch ein tendenziell geringerer Anteil kombinierter Mutationen im Frühstadium im Vergleich zu fortgeschrittenen Erkrankungen (8,3 % vs. 11,5 %; p = 0,7991).10
Studien & Leitlinien-Empfehlungen zur EGFR-Testung beim Lungenkarzinom
Die beiden häufigsten aktivierenden EGFR-Mutationen – Exon-19-Deletionen und die L858R-Punktmutation in Exon 21 – sind in allen Stadien des EGFR-mutierten NSCLC von therapeutischer Bedeutung. Sie sind prädiktiv für das Ansprechen auf EGFR-Tyrosinkinase-Inhibitoren (TKI) und bilden die Grundlage für eine personalisierte Therapieentscheidung.
Eine molekulare EGFR-Testung ist daher bei allen Patient:innen mit NSCLC obligat, unabhängig vom Erkrankungsstadium.2,11
EGFR-Testung in frühen Stadien (IB–IIIA)
Ursprünglich auf metastasierte Erkrankungen fokussiert, wird die EGFR-Testung inzwischen auch für frühe, potenziell resektable Stadien (IB–IIIA) empfohlen. Nationale Leitlinien schlagen explizit die Analyse der Exons 19 und 21 (p.L858R und del19) vor.2,11
Neben EGFR sollten in operablen Stadien Marker bestimmt werden, die für die Steuerung der perioperativen, systemischen Therapie entscheidend sind:
- EGFR-Mutationen del19 und L858R
- ALK-Translokationen
- PD-L1 Expression
Eine umfassende molekulare Testung analog zum metastasierten Setting wird zunehmend diskutiert.2 Die Leitlinienempfehlungen stützen sich auf Studien wie ADAURA, die belegen, dass Patient:innen mit vollständig reseziertem NSCLC im Stadium IB–IIIA signifikant vom Einsatz adjuvanter EGFR-TKI profitieren.12 Auch neoadjuvante Therapieansätze mit EGFR-TKI befinden sich in klinischer Prüfung.
Wichtig: Da EGFR-mutierte Tumoren in der Regel nicht auf Immuncheckpoint-Inhibitoren ansprechen, ist die EGFR-Testung bereits in frühen Stadien unerlässlich.13
EGFR-Testung in fortgeschrittenen Stadien (IIIB–IV)
Für EGFR-mutierte NSCLC im Stadium IIIB–IV haben sich EGFR-TKI als Therapiestandard in der Erstlinie etabliert. Die Wirksamkeit von TKI der ersten14,15, zweiten16–18 und dritten Generation19,20 wurde in zahlreichen Studien durch signifikante Verbesserungen des progressionsfreien Überlebens gegenüber Chemotherapie belegt.
Daher gilt der Test auf EGFR-Mutationen in den Exons 18–21 in diesem Setting als diagnostische Mindestanforderung vor dem Einleiten einer Erstlinientherapie. In den Leitlinien wird eine umfassende molekulare Diagnostik auf alle therapeutisch relevanten Alterationen empfohlen.2,11
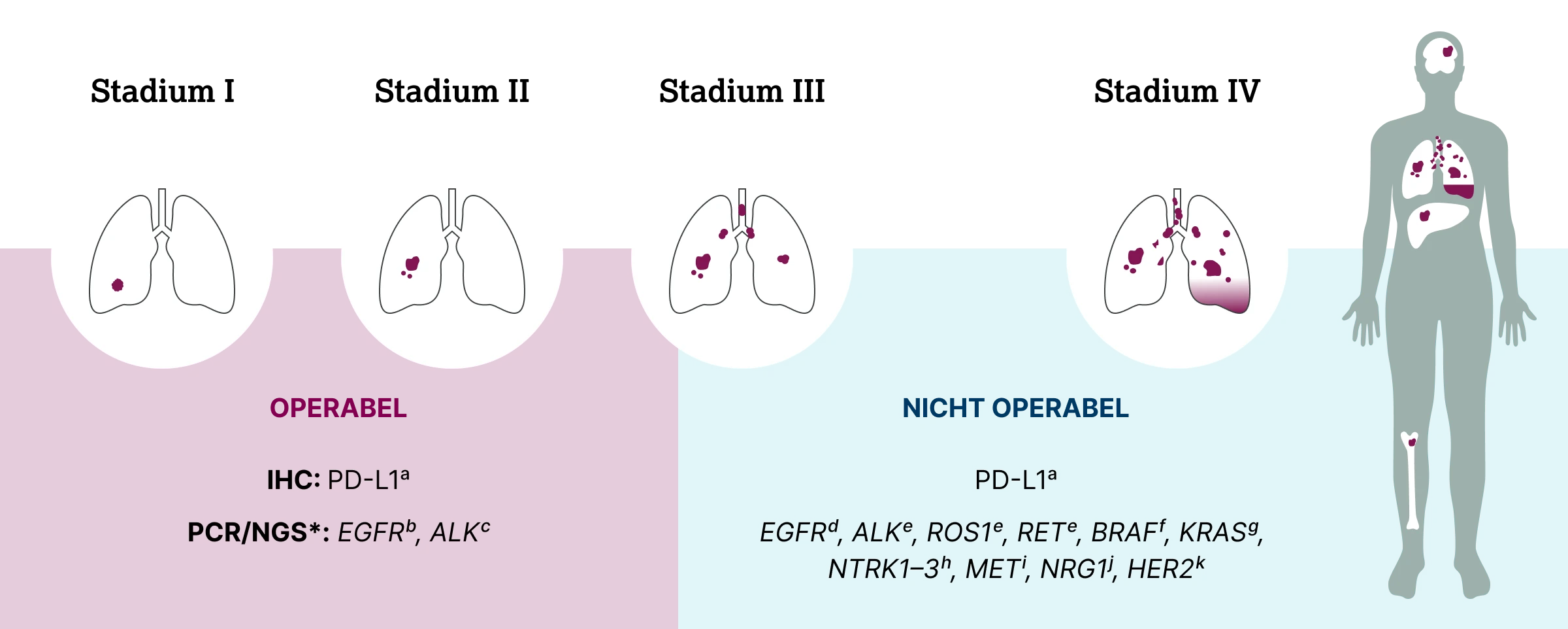
*Diskutiert wird eine umfassende molekulare Testung wie im Stadium IV
- Die PD-L1Testung wird von der S3- und der Onkopedia-Leitlinie in den Stadien IB–III empfohlen und im Stadium IV bei therapienaiven Patient:innen.
- Die EGFR-Testung wird von der S3-Leitlinie in den Stadien IB–IIIA für Exon 19 und 21 empfohlen, von der Onkopedia-Leitlinie in den Stadien IB–IIIC für del19 und L853 empfohlen.
- Die Testung auf ALK-Translokationen wird in der Onkopedia-Leitlinie in Stadien IB–IIIC und in der S3-Leitlinie in den Stadien IB–IIIA bei Tumoren ≥ 4 cm empfohlen.
- Die EGFR-Testung im Stadium IV wird von der S3-Leitlinie bei therapienaiven Patient:innen für Exon 18–21 und von der Onkopedia-Leitlinie für Exon 18–21 plus T790M empfohlen.
- In Stadium IV wird von beiden Leitlinien die Testung auf ALK-, ROS1- und RET-Fusionen vor Beginn der Erstlinientherapie empfohlen.
- In der S3-Leitlinie wird die Testung auf BRAF-V600-Mutationen empfohlen, in der Onkopedia-Leitlinie wird die Testung auf BRAF-V600E-Mutationen beschränkt.
- In der S3-Leitlinie wird die Testung auf KRAS-Mutationen (inkl. G12C) empfohlen, in der Onkopedia-Leitlinie wird die Testung auf KRAS G12C-Mutationen beschränkt.
- In der S3-Leitlinie wird die Testung auf NTRK1-3-Fusionen empfohlen, in der Onkopedia-Leitlinie auf NTRK-Translokationen (die Fusionsereignisse beinhalten).
- In der S3-Leitlinie wird die Testung auf MET-Amplifikation und MET Exon-14-Skipping-Mutationen empfohlen, in der Onkopedia-Leitlinie lediglich auf c-MET Exon-14-Skipping-Mutationen.
- Die NRG1-Testung wird in der S3-Leitlinie im Stadium IV empfohlen.
- In der S3-Leitlinie wird die Testung auf HER2 (ERBB2)-Mutationen in den Exons 8, 18, 19, 20 und 21 empfohlen, in der Onkopedia-Leitlinie wird generell die Testung auf HER2 (ERBB2)-Mutationen empfohlen.
Auch im Fall eines Rezidivs oder bei Progress unter EGFR-TKI ist die Wiederholung der EGFR-Testung essenziell, insbesondere zur Identifikation sekundärer Resistenzmechanismen. Ein prominentes Beispiel ist die T790M-Mutation, die häufige Ursache für Resistenzen gegenüber Erst- und Zweitgenerations-TKI ist.2
Zur Resistenzabklärung sollte eine Rebiopsie oder – für den Fall, dass keine Gewebeprobe entnommen werden kann – eine Liquid Biopsy erfolgen, idealerweise im Rahmen eines erweiterten molekularen Panels. Die Detektion von T790M erlaubt eine gezielte Umstellung auf einen Drittgenerations-TKI.2
Videotipp
Praxiserfahrungen zur EGFR-Testung in frühen Stadien des NSCLC ansehen
Empfehlungen zum optimalen Zeitpunkt für die EGFR-Testung beim NSCLC
Die molekulare Testung auf EGFR-Mutationen ist ein entscheidender Schritt in der Diagnostik und Therapieplanung des nicht-kleinzelligen Lungenkarzinoms (NSCLC). Sowohl die S3-Leitlinie11 als auch die Onkopedia-Leitlinie2 betonen die Bedeutung einer frühzeitigen und umfassenden molekularpathologischen Analyse.
Frühzeitige Testung nach Diagnosesicherung
Gemäß den aktuellen Empfehlungen sollte die EGFR-Mutationsanalyse unmittelbar nach der histologischen Sicherung der Diagnose erfolgen, idealerweise vor Beginn einer systemischen Therapie. Dies gilt für alle NSCLC-Stadien ab IB aufwärts, einschließlich operabler Stadien. Eine frühzeitige Testung ermöglicht eine gezielte Therapieplanung und vermeidet Verzögerungen im Behandlungsverlauf.2,11
Testung in frühen, operablen Stadien (IB–IIIA)
In den frühen Stadien des NSCLC (IB–IIIA) ist die EGFR-Testung besonders relevant, da sie die Auswahl geeigneter oder den Ausschluss ungeeigneter adjuvanter oder neoadjuvanter Therapien beeinflusst. In der S3-Leitlinie wird die Testung auf die häufigen EGFR-Mutationen in den Ex19del und L858R empfohlen.11
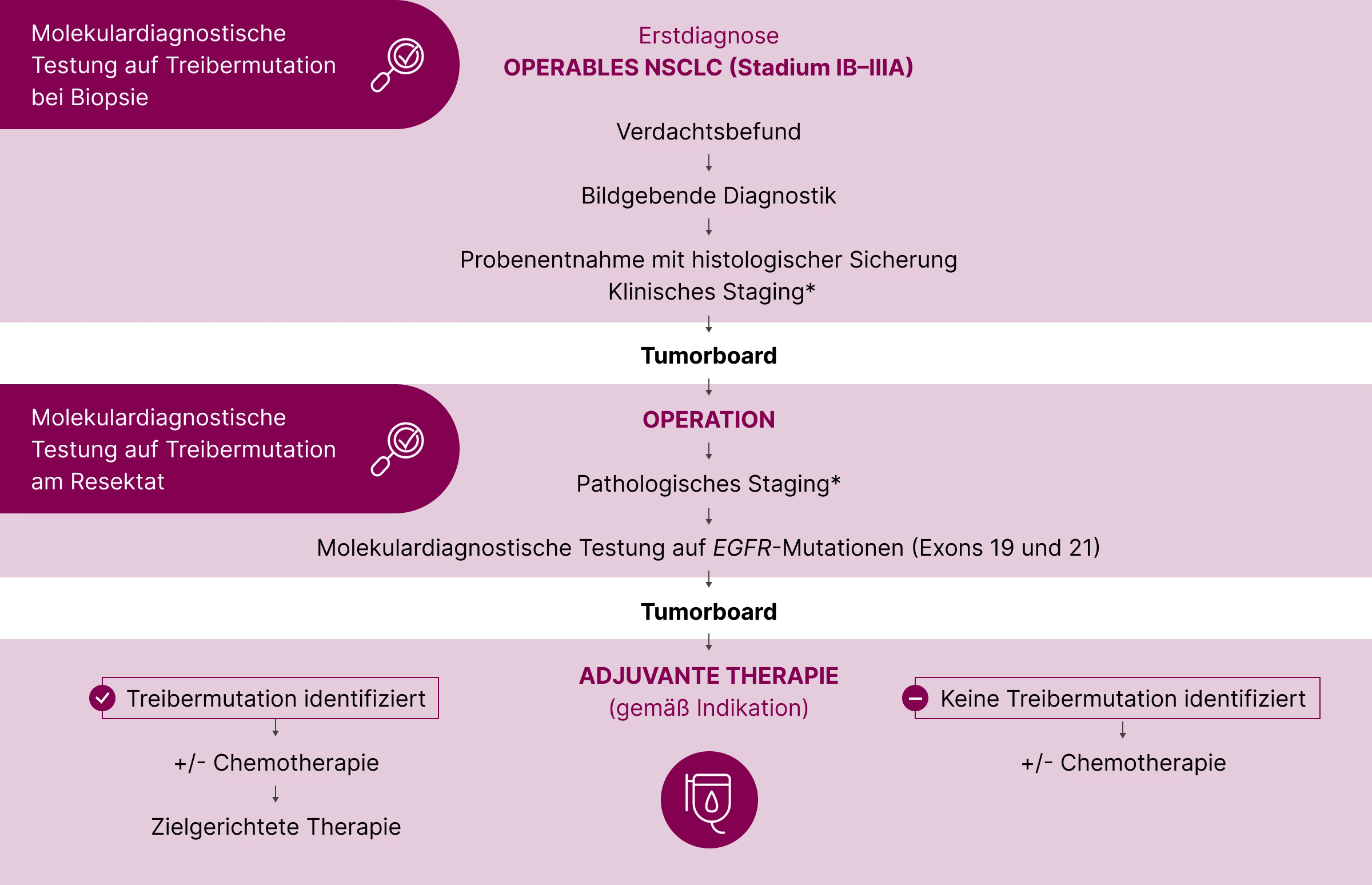
* Klinisches Staging vor der Operation nach IASLC/UICC9. Pathologisches Staging nach Resektion; Schnittränder (R0, R1, R2); Tumorgröße; befallene Lymphknoten.

Expert:innenmeinungen zur Bedeutung der molekularpathologischen Testung in den frühen Stadien.
Testung in fortgeschrittenen, nicht operablen Stadien (IIIB–IV)
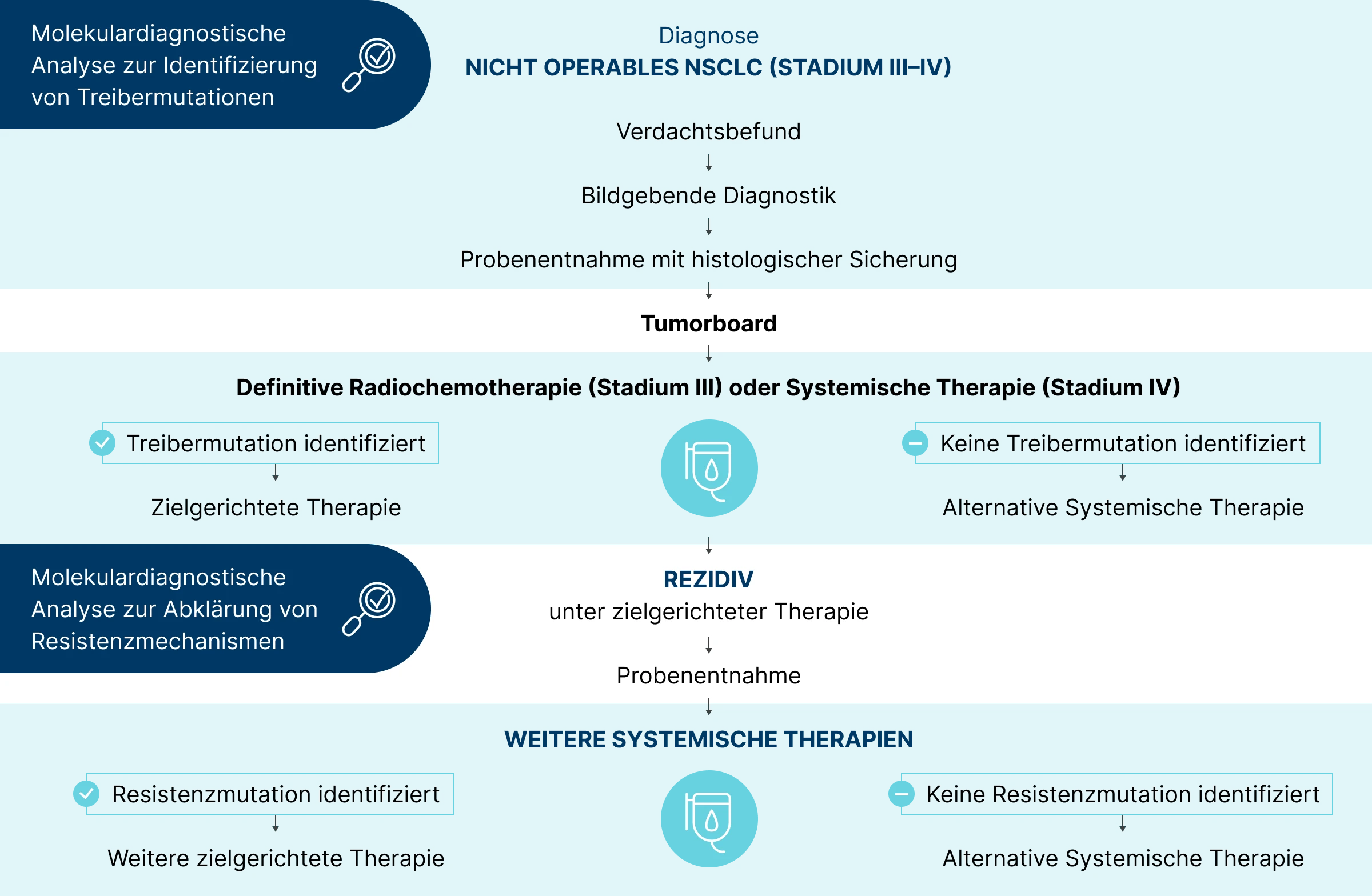
Bei fortgeschrittenem NSCLC ist die EGFR-Mutationsanalyse vor Beginn der Erstlinientherapie unerlässlich. In der Onkopedia-Leitlinie wird bei nicht operablem Tumor im Stadium III mindestens eine Testung auf EGFR (del19/L858R) empfohlen, in Stadium IV eine umfassende molekulare Diagnostik, einschließlich der Testung auf EGFR-Mutationen in den Exons 18–21.2 Diese Analyse bildet die Grundlage für den Einsatz von EGFR-TKI und ist entscheidend für die Wahl der optimalen Therapie.
Anforderungen an Probenmaterial und Testmethoden zur EGFR-Mutationsanalyse
Für die EGFR-Mutationsdiagnostik sollte möglichst frisches Tumorgewebe eingesetzt werden, vorzugsweise aus Biopsien oder chirurgischen Resektaten. Steht kein ausreichend qualitatives oder quantitatives Gewebematerial zur Verfügung, stellt die Liquid Biopsy eine sinnvolle Alternative dar. Sie ermöglicht den Nachweis von EGFR-Mutationen in der zirkulierenden Tumor-DNA (ctDNA) und ist insbesondere bei nicht biopsierbaren Läsionen von diagnostischem Nutzen.
Die aktuellen Leitlinien empfehlen ausdrücklich den Einsatz moderner molekularpathologischer Methoden. Im Vordergrund steht das Next-Generation-Sequencing (NGS), da es eine umfassende Analyse aller klinisch relevanten genomischen Alterationen – einschließlich seltener EGFR-Mutationen – in einem einzigen Testdurchlauf ermöglicht.
Ergänzend können in bestimmten Situationen auch klassische PCR-basierte Verfahren angewendet werden, insbesondere bei fokussierter Fragestellung oder limitiertem Probenmaterial.2,11
Abkürzungen
ALK: Anaplastische Lymphomkinase; BRAF: Serin/Threonin-Protein-Kinase B-Raf (Gen); ctDNA: zirkulierende Tumor-DNA; DNA: Desoxyribonukleinsäure; EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); ERBB2: v-erb-b2 erythroblastic leukemia viral oncogene homolog; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2 (Gen); IASLC: International Association for the Study of Lung Cancer; KRAS: Kirsten Rat Sarkoma (Gen); MET: Mesenchymal-epithelialer Transitionsfaktor (Gen); NGS: Next-Generation-Sequencing; NSCLC: nicht-kleinzelliges Lungenkarzinom; NTRK: Neurotrophe Tyrosinrezeptor-Kinasen (Gen); PCR: Polymerase-Kettenreaktion; PD-L1: Programmed cell death ligand-1; PIK3CA: Phosphoinositid-3-Kinase katalytische Untereinheit alpha; R0: kein Residualtumor; R1: mikroskopischer Residualtumor; R2: makroskopischer Residualtumor; RET: Rearranged during Transfection (Gen); ROS1: ROS-Protoonkogen 1 (Gen); TKI: Tyrosinkinase-Inhibitoren; UICC9: 9. Auflage der TNM-Klassifikation, herausgegeben von der Union Internationale Contre le Cancer
- Zhang YL, et al. Oncotarget 2016;7(48):78985–93.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig (NSCLC); April 2025. Verfügbar unter www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: Februar 2026.
- Tan AC, et al. J Clin Oncol 2022;40(6):611–25.
- Penault-Llorca F, et al. Oncologist 2025;30(3):oyae357.
- Chevallier M, et al. World J Clin Oncol 2021;12(4):217–37.
- Tsao AS, et al. J Thorac Oncol 2016;11(5):613–38.
- Harrison PT, et al. Semin Cancer Biol 2020;61:167–79.
- Masood A, et al. Semin Oncol 2019;46(3):271–83.
- Yang JC, et al. Lancet Oncol 2015;16(7):830–8.
- Stephan-Falkenau S, et al. Int J Mol Sci 2022;23(20):12511.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter register.awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: Februar 2026.
- Tsuboi M, et al. N Engl J Med 2023;389(2):137–47.
- Lee CK, et al. J Thorac Oncol 2017;12(2):403–7.
- Mok TS, et al. N Engl J Med 2009;361(10):947–57.
- Maemondo M, et al. N Engl J Med 2010;362(25):2380–8.
- Sequist LV, et al. J Clin Oncol 2013;31(27):3327–34.
- Paz-Ares L, et al. Ann Oncol 2017;28(2):270–7.
- Mok TS, et al. J Clin Oncol 2018;36(22):2244–50.
- Soria JC, et al. N Engl J Med 2018;378(2):113–25.
- Planchard D, et al. N Engl J Med 2023;389(21):1935-1948 (inkl. Supplements).


