KRAS, STK11, KEAP1 beim Lungenkarzinom
Die präzise Identifikation von KRAS-, STK11- und KEAP1-Mutationen ist ein zentrales Element der modernen Pathologie beim NSCLC. Die Wahl und Kombination diagnostischer Methoden beeinflusst die Detektionsrate, die Aussagekraft und die klinische Nutzbarkeit der Ergebnisse maßgeblich.1-3 Klinisch validierte NGS-Panels, wie FoundationOne oder MSK-IMPACT, beinhalten diese Gene routinemäßig und werden meist an formalinfixiertem, paraffineingebettetem Tumorgewebe (FFPE) durchgeführt.4-6
Molekulare Testung mittels Next-Generation-Sequencing (NGS)
Die breite molekulare Testung auf alle therapeutisch relevanten Biomarker mittels Next-Generation-Sequencing (NGS) wird von nationalen und internationalen Leitlinien möglichst früh, bereits zum Zeitpunkt der Diagnose eines NSCLC in Stadium IV empfohlen.7-11 Um sicherzustellen, dass Patient:innen, die am besten für sie geeignete Behandlung erhalten, sollten umfassende molekulare Tests sowohl etablierte als auch neue, therapeutisch nutzbare Mutationen beinhalten („Emerging Biomarkers“).12
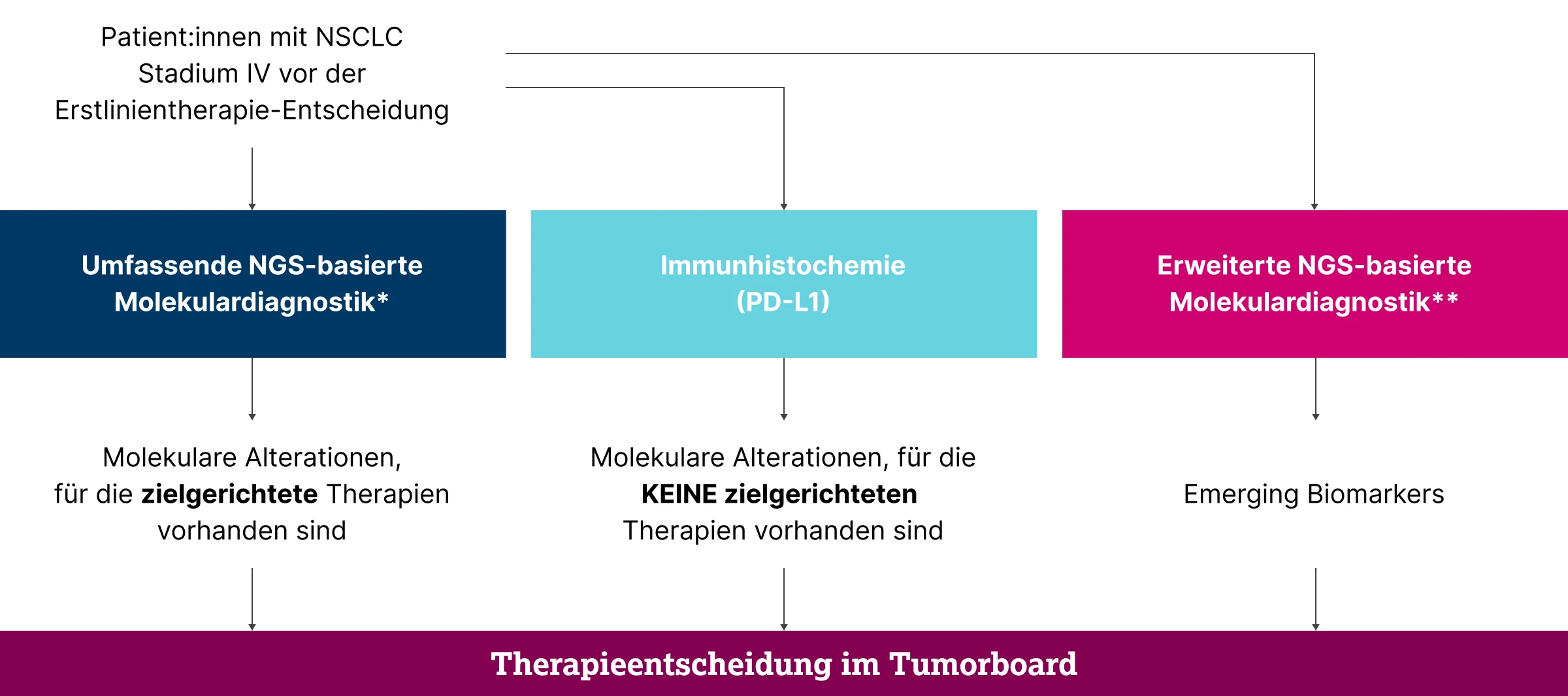
* In Anbetracht der Dynamik der Entwicklung neuer personalisierter Therapieansätze sollte angestrebt werden, dass jeder Patient/jede Patientin mit NSCLC Stadium IV vor der Erstlinientherapieentscheidung eine umfassende NGS-basierte Molekulardiagnostik erhält.7
** Bei Patient:innen mit Wildtypkonfiguration für EGFR, ALK, ROS1, BRAF V600, NTRK, RET, METex14, KRAS, HER2 (ERBB2) sollte eine umfassende Genotypisierung auf weitere bekannte Treibermutationen stattfinden, um bei dem Nachweis einer solchen eine zielgerichtete Therapie im Rahmen der Zulassung (ggf. für weitere Mutationen mit zugelassenen Medikamenten), einer Studie oder im Off-Label-Use zu ermöglichen.7
NGS ermöglicht die gleichzeitige Analyse zahlreicher Gene und Mutationen in einer einzigen Probe und deckt dabei Punktmutationen, kleine Insertionen/Deletionen sowie Kopienzahlveränderungen zuverlässig ab.2,13 Auch für die Detektion von KRAS-, STK11- und KEAP1-Mutationen gilt NGS als der Goldstandard.3 Die drei Biomarker sind bereits in zahlreichen kommerziell erhältlichen NGS Lung Cancer Panels enthalten.
Die molekulare Analyse kann schnell und zuverlässig an formalinfixiertem, paraffineingebettetem Tumorgewebe (FFPE), aber auch per Liquid Biopsy (sofern kein Gewebe zugänglich/vorhanden) durchgeführt werden.3,12
Die Liquid Biopsy, also die Analyse zirkulierender Tumor-DNA (ctDNA) aus Blutplasma, gewinnt insbesondere bei fortgeschrittener Erkrankung oder unzureichendem Tumormaterial zunehmend an Bedeutung.4,14 Auch hier kommt NGS zum Einsatz, wobei die Methode nicht-invasiv ist und eine schnelle Verfügbarkeit der Ergebnisse ermöglicht. Die Liquid Biopsy eignet sich besonders zur Detektion von KRAS-, STK11- und KEAP1-Mutationen, wenn eine Gewebebiopsie nicht möglich ist, oder wenn eine Verlaufskontrolle unter Therapie erforderlich ist.4,14 Die Sensitivität der Methode eingeschränkt, sodass ein negatives Ergebnis eine Mutation nicht sicher ausschließt.4,14 Dennoch liefert die Liquid Biopsy wertvolle Informationen zur Tumorbiologie und kann mehrfach im Krankheitsverlauf eingesetzt werden, um molekulare Veränderungen zu überwachen.14
Neben der molekularen Diagnostik werden zumindest für STK11 auch immunhistochemische Testmethoden diskutiert.15 Ein Verlust der STK11-Expression im Tumorgewebe kann auf eine inaktivierende Mutation oder Deletion hindeuten und ist mit einer aggressiveren Tumorbiologie sowie einer schlechteren Prognose assoziiert.15,16 Die IHC ermöglicht eine schnelle und kostengünstige Beurteilung des Proteinstatus, ersetzt jedoch nicht die molekulare Analyse, da nicht alle Mutationen zu einem vollständigen Proteinverlust führen. Für KRAS und KEAP1 ist die IHC derzeit nicht etabliert.15,16
Praktische Empfehlungen und Workflow
In der klinischen Praxis empfiehlt sich die umfassende molekulare Testung mittels NGS an Tumorgewebe bei allen Patient:innen mit fortgeschrittenem NSCLC, um eine optimale Therapieplanung und Prognoseabschätzung zu ermöglichen. Bei limitierter Gewebemenge oder fortgeschrittener Erkrankung sollte die Liquid Biopsy als ergänzende oder alternative Methode in Betracht gezogen werden. Die IHC für STK11 kann zusätzliche Informationen liefern, sollte jedoch nicht als alleinige Methode zur Mutationsdetektion verwendet werden. Die Ergebnisse der molekularen Diagnostik sollten im interdisziplinären Tumorboard diskutiert und in die individuelle Therapieentscheidung einbezogen werden, um die bestmögliche Versorgung der Patienten zu gewährleisten.2,4
Abkürzungen
APC: Antigenpräsentierende Zellen; CD4: Cluster of Differentiation 4; CD80/86: Cluster of Differentiation 80/86, auch bekannt als B7-1/B7-2; ctDNA: zirkulierende Tumor-DNA; CTLA-4: T-Lymphozyten-assoziiertes Protein 4; FFPE: formalinfixiertes paraffingebettetes Tumorgewebe; ICI: Immuncheckpoint-Inhibitoren; IHC: Immunohistochemie; KEAP1: Kelch-like ECH-associated protein 1; KRAS: Kirsten-Ratten-Sarkom-Virus-Onkogen; MDSC: Myeloide Supressorzelle; MHC: Histokompatibilitätskomplex; NGS: Next-Generation-Sequencing; NSCLC: nicht-kleinzelliges Lungenkarzinom; PD-1: Programmed cell death-1; PD-L1: Programmed cell death ligand-1; STK11: Serin/Threonin-Kinase-11-Gen; TCR: T-Zellrezeptor; TME: Tumormikroumgebung; Tregs: regulatorische T-Zellen
- Pavan A, et al. Transl Lung Cancer Res 2021;10(1):202–20.
- Knetki-Wróblewska M, et al. Transl Lung Cancer Res 2024;13(12):3718–30.
- Shiller M, et al. Front Oncol 2024;14:1459737.
- Sposito M, et al. Front Oncol 2024;14:1436588.
- Cheng DT, et al. J Mol Diagn . 2015 May;17(3):251-64.
- Rizvi H, et al. J Clin Oncol. 2018 Mar 1;36(7):633-641.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms - Living Guideline; 2025. Verfügbar unter register.awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: Februar 2026.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig; 2025. Verfügbar unter www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: Februar 2026.
- Hendriks LE, et al. (2025). ESMO Oncogene-Addicted Non-Small Cell Lung Cancer Living Guideline v1.2. Verfügbar unter www.esmo.org/living-guidelines/esmo-oncogene-addicted-metastatic-non-small-cell-lung-cancer-living-guideline. Letzter Zugriff: Februar 2026.
- NCCN Clinical Practice Guidelines in Oncology. Version 4.2025. Verfügbar unter www.nccn.org/guidelines/guidelines-detail?category=1&id=1450. Letzter Zugriff: Februar 2026.
- Owen DH, et al. (2025). ASCO Living Guideline, Version 2024.3. Therapy for Stage IV Non-Small Cell Lung Cancer With Driver Alterations. Verfügbar unter ascopubs.org/doi/pdf/10.1200/JCO-24-02785. Letzter Zugriff: Januar 2026.
- Ionescu DN, et al. Kompass Pneumol 2022;10(6):275–87.
- Smolle E, et al. Transl Lung Cancer Res 2021;10(5):2237–51.
- Ding H, et al. NPJ Precis Oncol 2025;9(1):5.
- Mitchell KG, et al. Ann Thorac Surg 2020;110(4):1131–8.
- Pons-Tostivint E, et al. Cells 2021;10(11):3129.

