EGFR-Diagnostik beim Lungenkarzinom
Der epidermale Wachstumsfaktor-Rezeptor (EGFR) stellt einen zentralen Biomarker in der molekularen Diagnostik des nicht-kleinzelligen Lungenkarzinoms (NSCLC) dar. Etwa ein Drittel aller Patient:innen mit NSCLC weist eine Mutation im EGFR-Gen auf.1 Die häufigsten Veränderungen betreffen Deletionen in Exon 19 (del19) sowie die Punktmutation L858R in Exon 21.2
Aufgrund verfügbarer zielgerichteter Therapien besitzen EGFR-Mutationen eine hohe klinische Relevanz und sollten gemäß der aktuellen Leitlinien bestimmt werden.1
EGFR-Testablauf
Die Analyse des EGFR-Mutationsstatus ist ein essenzieller Bestandteil der molekularen Routinediagnostik beim NSCLC und erfolgt in einem standardisierten mehrstufigen Verfahren. Ausgangsmaterial ist in der Regel Tumorgewebe aus histologischen Biopsien, zytologischen Präparaten oder – in geeigneten Fällen – zirkulierender Tumor-DNA aus dem peripheren Blut.3,4
Laut Leitlinie soll eine EGFR-Testung auch bei NSCLC im Frühstadium (IB–IIIA) am verfügbaren Tumorgewebe/Tumorzelle erfolgen. Im besten Fall erfolgt die Testung am Biopsat, andernfalls kann ein Resektat verwendet werden.3
Zur Detektion EGFR-relevanter Mutationen kommen verschiedene molekularbiologische Verfahren zum Einsatz, darunter:5
Real-time PCR
(RT-PCR)
Digital PCR
(dPCR)
Next-Generation-Sequencing
(NGS)
NGS gilt als derzeit bevorzugte Methode aufgrund seiner hohen Sensitivität und breiten Mutationsabdeckung, da auch nach anderen Mutationen gesucht wird.3–5

Informationen zu den Studien- und Leitlinienempfehlungen zur EGFR-Testung beim Mammakarzinom.
Probenmaterial zur EGFR-Testung
Die Genomanalyse kann an verschiedenen Ausgangsmaterialien durchgeführt werden.3,4,6
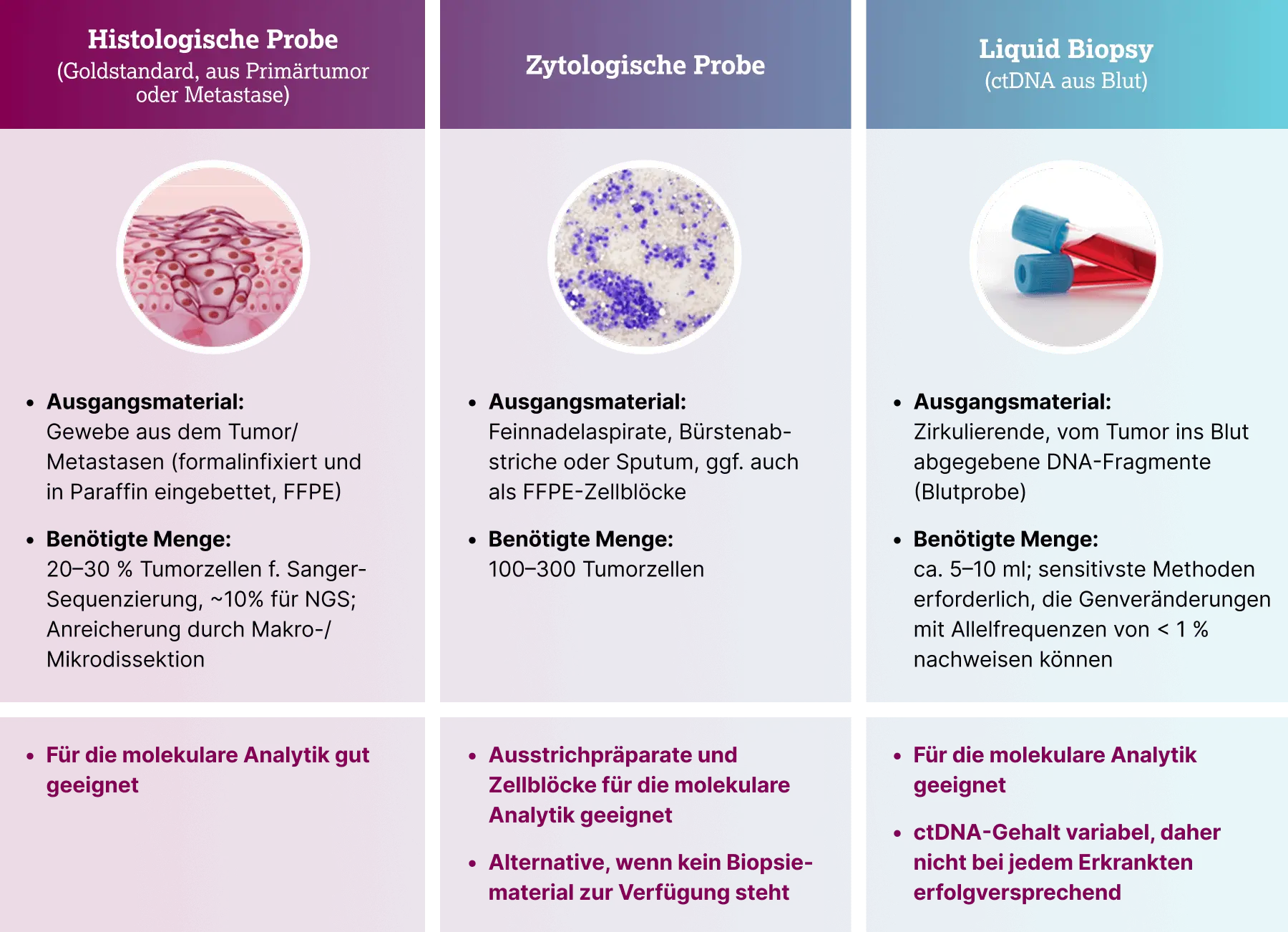
- Histologische Probe
Ausgangsmaterial: Gewebe aus Tumor oder Metastase (formalinfixiert und in Paraffin eingebettet (FFPE))
- Zytologische Probe
Ausgangsmaterial: Feinnadelaspirate, Bürstenabstriche oder Sputum, ggf. FFPE-Zellblöcke
- Liquid Biopsy (ctDNA aus Blut)
Ausgangsmaterial: Zirkulierende, vom Tumor ins Blut abgegebene DNA-Fragmente
Probenentnahmetechniken für die Zytologie
Zytologische Materialien eignen sich in der Regel sehr gut für die molekularpathologische Mutationsanalyse, sowohl aus Primärtumoren als auch aus Metastasen. Alle etablierten zytologischen Entnahmetechniken können genutzt werden. Feinnadelaspirate liefern qualitativ geeignetes Zellmaterial, allerdings oft nur in begrenzter Menge.7 Auch Bürstenabstriche sind – abhängig von Tumorlokalisation und klinischer Situation – eine valide Option.8,9


Liquid Biopsy zur EGFR-Testung beim NSCLC
Die Liquid Biopsy stellt eine etablierte, minimalinvasive Methode zur Analyse des EGFR-Mutationsstatus beim NSCLC dar. Grundlage ist die Untersuchung zirkulierender Tumor-DNA (ctDNA) im peripheren Blut.
Frühe Tumorstadien sind häufig mit einer höheren ctDNA-Konzentration assoziiert, was die Detektion genomischer Alterationen erleichtert.12 Für die Verwendung von Blut als Probenmaterial wird auch unter Einschränkungen von den Leitlinien empfohlen:
Technische Aspekte und Anforderungen
Die Analyse zirkulierender Tumor-DNA war lange mit logistischen Herausforderungen verbunden: Vollblutproben mussten innerhalb von 4 Stunden nach Entnahme zu Plasma verarbeitet werden, da andernfalls Zelllyse das Ergebnis verfälschen konnte.
Heute stehen spezielle Blutabnahmeröhrchen für ctDNA-Analysen zur Verfügung. Diese enthalten Stabilisatoren, die eine Konservierung der Blutprobe über mehrere Tage ermöglichen und so flexiblere Transport- und Verarbeitungszeiten erlauben.13–16
Analytische Qualität und Testauswahl
Für die EGFR-Testung mittels Liquid Biopsy sollten ausschließlich validierte, robuste und hochsensitive Testverfahren eingesetzt werden. Nur so lässt sich die diagnostische Aussagekraft maximieren und das Risiko falsch-negativer Ergebnisse – insbesondere bei niedriger ctDNA-Konzentration – minimieren. Die Spezifität der ctDNA-Analytik liegt maximal bei nahezu 100 %, weshalb falsch-positive Befunde praktisch ausgeschlossen werden können. Die Sensitivität hingegen beträgt im Mittel etwa 60 %, sodass ein negatives Ergebnis das Vorliegen einer Mutation nicht mit Sicherheit ausschließt. Entsprechend sollte die Liquid Biopsy im klinischen Kontext stets mit Bedacht interpretiert werden.17,18

Informationsvideos zum Thema Liquid Biopsy beim NSCLC.
EGFR-Testverfahren: Prinzip der komplementären Testung
Eine Metaanalyse19 bestätigt die diagnostische Relevanz der Liquid Biopsy bei der Testung von EGFR-Mutationen beim NSCLC, betont jedoch zugleich die Bedeutung einer ergänzenden Testung. Die Autoren unterstreichen die Vorteile der Liquid Biopsy in Bezug auf die Patientensicherheit, da sie eine weniger invasive Methode darstellt. Zudem ermöglicht die Liquid Biopsy die Detektion einer Vielzahl von Mutationen, die für die Therapieentscheidung von Bedeutung sind. Insbesondere die Analyse der EGFR-Mutationen ist entscheidend, um die Wirksamkeit der Behandlung mit Tyrosinkinase-Inhibitoren (TKIs) zu bewerten.

Klinisch relevante Alterationen, wie die häufig vorkommende Punktmutation L858R in Exon 21 als auch Deletionen in Exon 19, sowie die seltener vorkommende T790M Mutation auf Exon 20 des EGFR-Gens können durch Liquid Biopsy nachgewiesen werden. Dennoch empfehlen die Leitlinien für die Testung der Mutationen in den Exonen 19-21 zunächst eine Gewebeanalyse, da hier die Sensitivität der Methode höher ist. 3,6
Der gezielte Einsatz beider Methoden – Gewebediagnostik und Liquid Biopsy – stellt somit einen komplementären Ansatz dar, um sowohl diagnostische Sicherheit als auch Patientenkomfort zu maximieren.
Die S3-Leitlinie unterstützt diesen Ansatz, da sie empfiehlt „bei nicht ausreichendem Gewebe für die molekulare Diagnostik, und wenn eine erneute Biopsie nicht mit vertretbarem Risiko durchgeführt werden kann, soll eine Liquid Biopsy durchgeführt werden, vorausgesetzt eine histologische/zytologische Diagnosesicherung ist gegeben“.3
Abkürzungen
CT: Computertomografie; ctDNA: zirkulierende Tumor-DNA; ddPCR: droplet-digitale Polymerase-Kettenreaktion; EBUS-FNA: endobronchial-ultraschallgestützte Feinnadelaspiration; EGFR: epidermaler Wachstumsfaktor-Rezeptor (Protein); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); EUS-FNA: endoskopische ultraschallgestützte Feinnadelaspiration; FFPE: formalinfixiertes paraffineingebettetes Tumorgewebe; FNA: Feinnadelaspirate; NGS: Next-Generation-Sequencing; NSCLC: nicht-kleinzelliges Lungenkarzinom; PCR: Polymerase-Kettenreaktion; ROSE: Rapid Onsite Evaluation; RT-PCR: Real-time Polymerase-Kettenreaktion; TKI: Tyrosinkinase-Inhibitor
- Pasello G, et al. Front Oncol 2022;12:909064.
- Batra U, et al. BMJ Open Respir Res 2023;10(1):e001492.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: September 2025.
- Mirikar D, et al. Sci Rep 2025;15(1):1252.
- Hofman P, et al. ESMO Open 2023;8(5):101628.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig (NSCLC); April 2025. Verfügbar unter onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: September 2025.
- Dupain C, et al. Mol Oncol 2020;15(1):104–115.
- Jain D, et al. Arch Pathol Lab Med 2018; 142 (9): 1127–1133.
- Theegarten D, et al. Radiologe 2016;56(9):777–85.
- Scarpino S, et al. Lung Cancer 2015;87(1):8–13.
- Yan S, et al. Front Oncol 2025;15:1566666.
- Ma L, et al. Signal Transduct Target Ther. 2024;9(1):336.
- ROCHE. Cell-Free DNA Collection Tube, 2022. Verfügbar unter: https://elabdoc-prod.roche.com/eLD/api/downloads/32b4ee93-f590-ed11-1a91-005056a772fd?countryIsoCode=XG. Letzter Zugriff: September 2025.
- QIAGEN. PAXgene Blood ccfDNA Tube, 2019. Verfügbar unter: https://www.preanalytix.com/storage/download/_ProductResources_/TechnicalNotes/PROM-13914-001_TN_Blood_ccfDNA_TubeCEIVD_TubeTransport_0319_EU-lay11.pdf. Letzter Zugriff: September 2025.
- MAGBIO. Blood STASIS™ 21-ccfDNA, 2025. Verfügbar unter: https://www.magbiogenomics.com/pub/media/productattach/b/l/blood_stasis_21-ccfdna_handbook.pdf?srsltid=AfmBOooTuEZl3VmLUH581bg5Uax2ANPRyqk82hIlGhhfeH_ox5HSo8uj. Letzter Zugriff: September 2025.
- Streck. Cell-Free DNA BCT, 2025. Verfügbar unter: https://www.streck.com/wp-content/uploads/2025/03/03_Cell-Free_DNA_BCT_RUO_IFU.pdf. Letzter Zugriff unter: September 2025.
- Samaha R, et al. Curr Oncol 2025;32(2):57.
- Jha P, et al. J Liq Biopsy 2025;8:100300.
- Cai J, et al. Transl Oncol 2024;47:102022.
