Therapiemöglichkeiten bei einem veränderten HER2-Status
Zielgerichtete HER2-Inhibition
Therapeutische Antikörper und niedermolekulare Inhibitoren, die an die extrazelluläre bzw. intrazelluläre Domäne des HER2-Rezeptors binden, blockieren nachgeschaltete Signalwege und können den Zellzyklus der Tumorzellen zum Stillstand bringen.1 Mehrere HER2-gerichtete Therapien sind derzeit zugelassen, darunter monoklonale Antikörper, Antikörper-Wirkstoff-Konjugate (ADCs) und Tyrosinkinase-Inhibitoren (TKIs).
Monoklonale Anti-HER2-Antikörper
Der erste gegen HER2 gerichtete, humanisierte monoklonale Antikörper wurde bereits in den 1980er-Jahren entwickelt2 und ist heute fester Bestandteil der Standardtherapie bei bestimmten Brust- und Lungenkarzinomen. Dieser Antikörper bindet an die extrazelluläre Domäne von HER2 (Subdomäne IV), hemmt die Homodimerisierung und unterbricht die nachgeschaltete Signalkaskade.3,4 Allerdings kann er die ligandenvermittelte Heterodimerisierung von HER2 mit HER3 oder HER1 offenbar nicht vollständig verhindern – ein potenzieller Resistenzmechanismus.5
Ein zweiter, ebenfalls humanisierter monoklonaler Antikörper, der seit 2013 in Europa zugelassen ist, bindet an eine andere Stelle der extrazellulären HER2-Domäne (Subdomäne II)4 und unterbindet die Dimerisierung mit anderen HER-Rezeptoren, insbesondere HER3.4,5
Die Kombination beider Antikörper zeigt aufgrund ihrer komplementären Wirkmechanismen eine stärkere Hemmung der HER2-vermittelten Signalwege.4 Darüber hinaus fördern monoklonale Anti-HER2-Antikörper die Endozytose des HER2-Rezeptors, hemmen die Angiogenese und können über antikörperabhängige zellvermittelte Zytotoxizität die Tumorzelllyse induzieren.4
Antikörper-Wirkstoff-Konjugate (ADCs)
ADCs sind eine neuartige Klasse onkologischer Wirkstoffe, die die zielgerichtete Bindung von Antikörpern mit der Wirksamkeit von Chemotherapeutika kombinieren. Aufgrund ihres Wirkprinzips – dem gezielten Einschleusen zytotoxischer Substanzen in Tumorzellen – werden sie auch als „trojanische Pferde“ bezeichnet.
Nach Bindung an den HER2-Rezeptor wird das ADC von der Tumorzelle aufgenommen. Der Linker, der zytostatischen Wirkstoff und Antikörper verbindet, wird gespalten und das Zytostatikum ins Zytoplasma freigesetzt, was zur Apoptose führt. Zusätzlich kann ein sogenannter Bystander-Effekt auftreten, wenn die freigesetzten Wirkstoffmoleküle in benachbarte Zellen diffundieren und dort ebenfalls den Zelltod auslösen.6
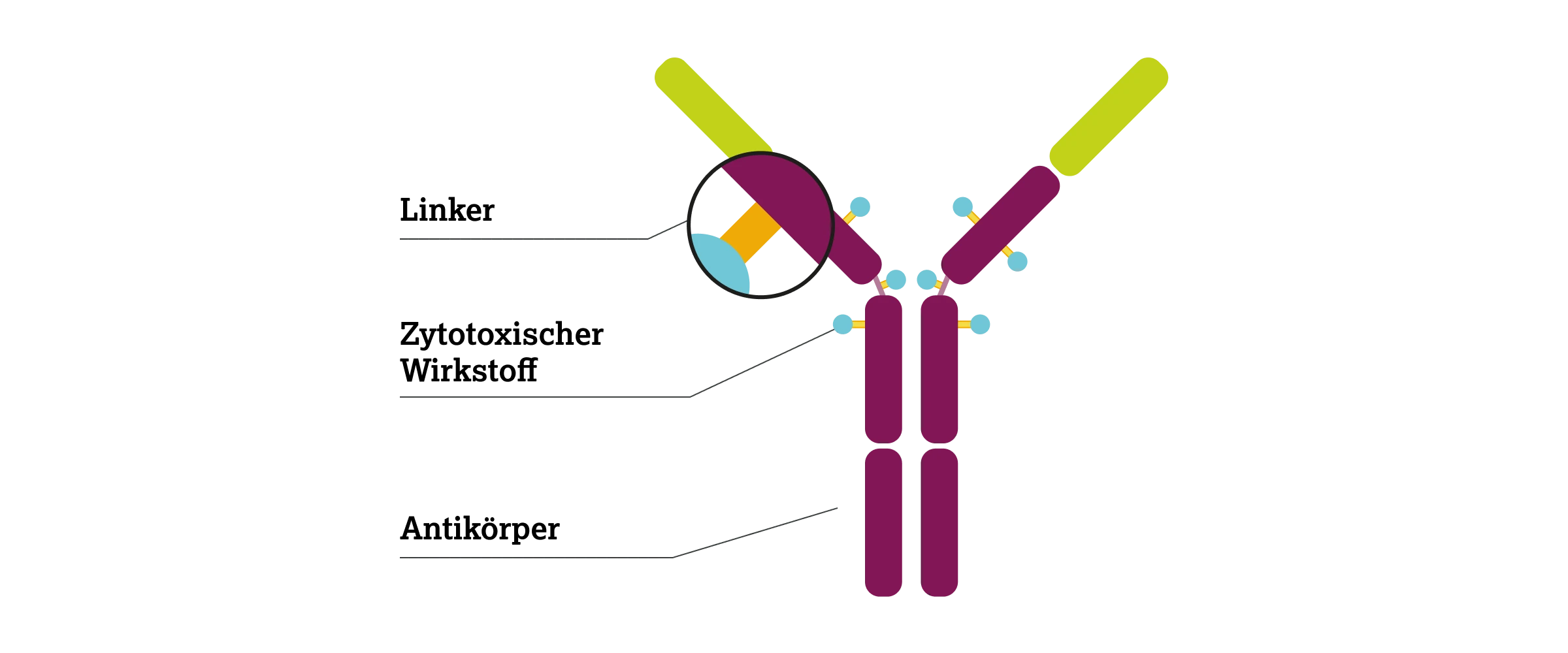
Ein Antikörper-Wirkstoff-Konjugat (ADC) besteht aus drei Komponenten: dem gegen ein spezifisches Tumorantigen (z. B. HER2) gerichteten Antikörper, dem zytotoxischen Wirkstoff und einem Linker, der diesen Wirkstoff mit dem Antikörper verbindet.7
Tyrosinkinase-Inhibitoren (TKIs)
TKIs sind kleine Moleküle, die intrazellulär wirken und Tyrosinkinasen blockieren – Enzyme, die wichtige Signalwege in Tumorzellen aktivieren. Seit 2008 ist ein TKI zur Behandlung von fortgeschrittenem HER2-positivem Brustkrebs zugelassen. Dieser hemmt die Tyrosinkinase-Domänen von HER1 und HER2 und unterbricht so die Tumorproliferation.3
Auch beim Lungenkarzinom werden TKIs erfolgreich eingesetzt, etwa zur Therapie HER1-(EGFR)-mutierter Tumoren – was die Prognose signifikant verbessern kann.8 Gegen HER2 gerichtete TKIs beim nicht-kleinzelligen Lungenkarzinom (NSCLC) befinden sich derzeit in der klinischen Entwicklung.
Abkürzungen
ADC: Antibody-Drug Conjugate; EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); HER1: humaner epidermaler Wachstumsfaktor-Rezeptor 1 (Protein); HER1: humaner epidermaler Wachstumsfaktor-Rezeptor 1 (Gen); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HER3: humaner epidermaler Wachstumsfaktor-Rezeptor 3; NSCLC: nicht-kleinzelliges Lungenkarzinom; TKI: Tyrosinkinase-Inhibitor
- Hart V, et al. Oncotarget 2020;11(46):4338–57.
- Slamon DJ, et al. N Engl J Med 2001;344(11):783–92.
- Albagoush SA, et al. (2025). Tissue Evaluation for HER2 Tumor Marker. Verfügbar unter ncbi.nlm.nih.gov/books/NBK537134/. Update 07.01.2024; Letzter Zugriff November 2025.
- Yu S, et al. Exp Hematol Oncol 2017;6:31.
- Harbeck N, et al. Breast Care (Basel) 2013;8(1):49–55.
- Aoki M, et al. Gastric Cancer 2021;24(3):567–76.
- Criscitiello C, et al. J Hematol Oncol 2021;14(1):20.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter register.awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: November 2025.


