PIK3CA/AKT1/PTEN-Diagnostik beim Mammakarzinom
Probenmaterial und Testablauf
Die molekulargenetische Analyse von PIK3CA-, AKT1- oder PTEN sollte an formalinfixierten, paraffineingebetteten (FFPE)-Gewebeproben – einschließlich Feinnadelaspiraten und zytologischen Präparaten –von HR-positivem, HER2-negativem, metastasiertem Mammakarzinom (mBC) durchgeführt werden, sofern eine ausreichende Zellzahl vorliegt. Alternativ kann unfixiertes (frisches oder gefrorenes) Gewebe aus dem Primärtumor oder aus Metastasen verwendet werden.1-3 Wenn eine erste Testung an Plasma (Liquid Biopsy) durchgeführt wurde und ein negatives Ergebnis für den gesuchten Biomarker zeigt, wird dringend empfohlen, eine Folgetestung am Tumormaterial vorzunehmen.2,3

Informationen zur Liquid Biopsy.
Die molekulargenetische Analyse von PIK3CA, AKT1 und PTEN erfolgt aus FFPE Material nach gezielter Tumorarealmarkierung durch den Pathologen. Bei niedriger Tumorzellfraktion wird eine Mikrodissektion durchgeführt. Die isolierte DNA dient als Ausgangsmaterial für ein NGS-basiertes Multigen-Panel, das Mutationen in den genannten Genen mit hoher Sensitivität detektiert. Die bioinformatische Auswertung erfolgt nach standardisierten Qualitätskriterien; klinisch relevante Varianten werden kontextbezogen interpretiert.4
Ob im Verlauf der Behandlung weitere Biopsien für NGS-Tests notwendig sind, sollte in Absprache mit den behandelnden Onkolog:innen und im Rahmen eines interdisziplinären Tumorboards entschieden werden. Eine Erstattung der NGS-Panel-Analysen hängt vom Ausgangsmaterial (Gewebetest oder Liquid Biopsy) ab und sollte vor der Testung mit den gesetzlichen Krankenkassen abgeklärt werden.5
Testung an Gewebe und Plasma (Liquid Biopsy)
Wird im Rahmen einer Liquid Biopsy eine pathogene PIK3CA-Alteration nachgewiesen, kann eine zielgerichtete Therapie eingeleitet werden. Zeigt eine initiale Liquid Biopsy keine PIK3CA-Alteration, sollte eine Nachtestung am Gewebe mittels NGS-Panels erfolgen, welche zusätzlich auch AKT1 und PTEN erfasst.3 Da die Nachforderung von Gewebeproben zeitliche Verzögerungen verursacht, wird bei HR-positivem, HER2-negativem mBC eine frühzeitige molekulargenetische Testung direkt am Gewebe mittels multigenem NGS-Panel empfohlen, um therapeutisch relevante Alterationen rechtzeitig zu identifizieren.
Für die Liquid-Biopsy-Diagnostik ist zusätzlich zu berücksichtigen, dass im Einheitlichen Bewertungsmaßstab (EBM) derzeit ausschließlich ESR1- und PIK3CA-Analysen für das Hormonrezeptor-positive, HER2-negative mBC erstattungsfähig sind.5 Patient:innen mit AKT1- oder PTEN-Alterationen könnten somit durch diese Teststrategie nicht erfasst werden.
Mehrere Studien bestätigen die Gewebetestung als diagnostischen Goldstandard für die Analyse von PIK3CA-, AKT1- und PTEN-Genveränderungen.3,6,7
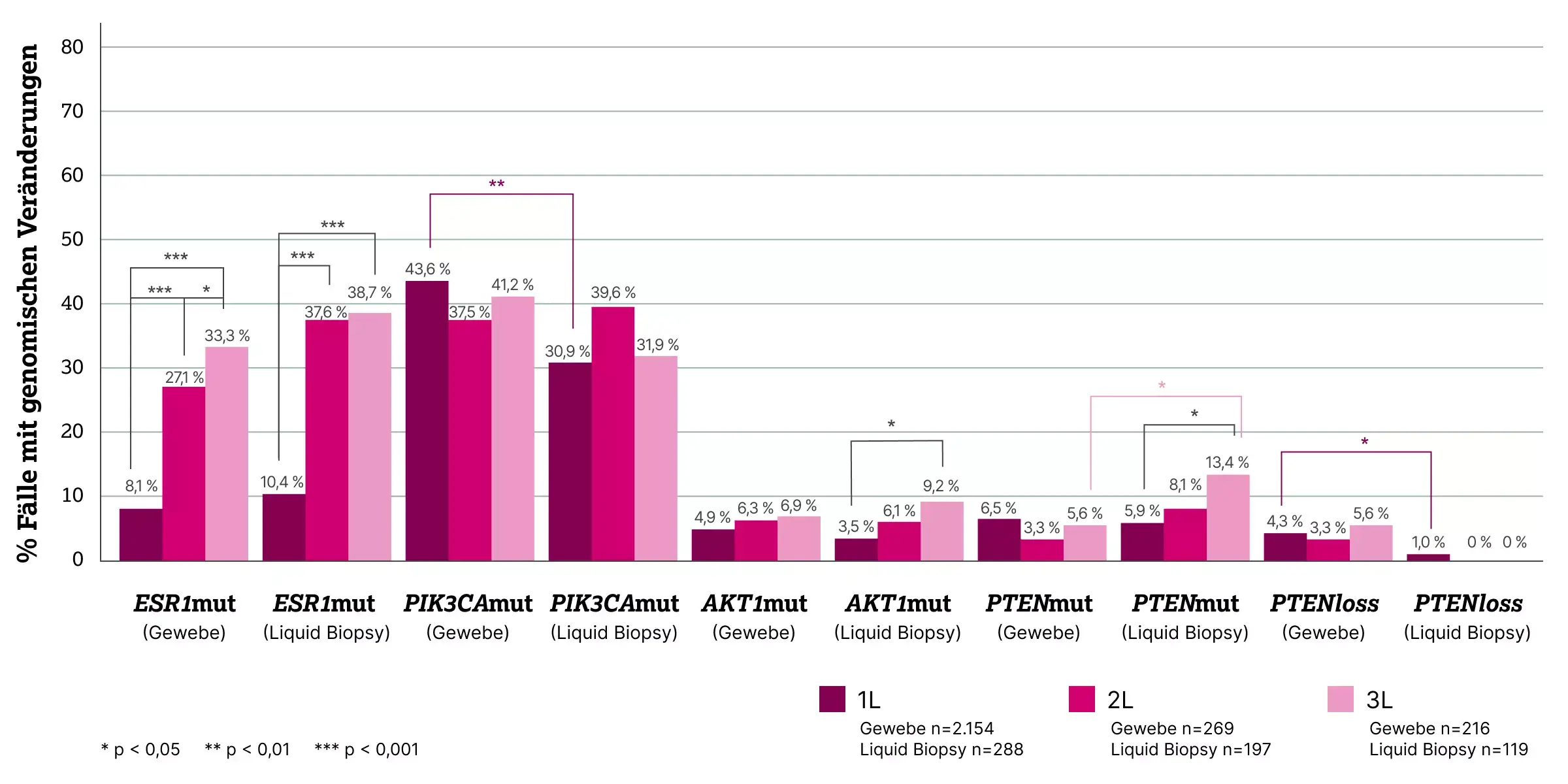
In einer umfangreichen Kohorte wurden NGS-Daten aus Liquid Biopsy und korrespondierenden Gewebeproben systematisch miteinander verglichen (vgl. Abbildung). Weitere Untersuchungen verdeutlichen die Limitationen der Liquid Biopsy für diese Gene, insbesondere durch unzureichende Mengen an zirkulierender Tumor-DNA (ctDNA) oder geringem Tumoranteil. Besonders herausfordernd ist die Detektion von PTEN-Veränderungen: Neben Punktmutationen sind auch größere Umlagerungen und Deletionen therapeutisch relevant. Komplexe Alterationen wie PTENloss (homozygoter Verlust) sowie Copy-Number-Varianten (CNVs) lassen sich in Liquid Biopsy nur eingeschränkt erfassen, während sie in Gewebeproben deutlich zuverlässiger nachweisbar sind.
Die zentralen Erkenntnisse der Analyse:3
- Die Sensitivität der Liquid Biopsy für PIK3CA/AKT1/PTEN war der Gewebetestung deutlich unterlegen, insbesondere bei geringem Tumoranteil oder heterogener klonaler Verteilung.
- PIK3CA-Mutationen wurden im Gewebe signifikant häufiger nachgewiesen als in ctDNA.
- PTEN-Verluste (homozygote Deletionen) und komplexe CNVs wurden in Gewebeproben deutlich häufiger detektiert als in Liquid Biopsy.
- Für klinisch relevante Therapieentscheidungen erwies sich die Gewebetestung als konsistenter und verlässlicher.
Daher sollte im Rahmen der molekularen Testung von HR-positivem, HER2-negativem Mammakarzinom eine primäre Gewebetestung bevorzugt eingesetzt werden.

Informationen zur Kostenerstattung bei PIK3CA/AKT1/PTEN-Mutationen.
Abkürzungen
AKT: Serin/Threonin-Kinase AKT (Protein); AKT1: Serin/Threonin-Kinase AKT1 (Gen); ctDNA: zirkulierende Tumor-DNA; EBM: Einheitlicher Bewertungsmaßstab; ER: Östrogenrezeptor; ESR1: Östrogenrezeptor 1; FFPE: formalinfixiert, paraffineingebettet; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HR: Hormonrezeptor; loss: Verlust der homozygoten Kopie; mBC: metastasiertes Mammakarzinom; mut: Mutation; NGS: Next-Generation-Sequencing; PI3K: Phosphoinositid-3-Kinase (Protein); PIK3CA: Phosphoinositid-3-Kinase katalytische Untereinheit alpha (Gen); PTEN: Phosphatase- und Tensin- Homolog (Gen); PTEN: Phosphatase- und Tensin- Homolog (Protein); 1L: Erstlinie, 2L: Zweitlinie: 3L: Drittlinie
- Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.V. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlungen 2025.1D. Pathologie.
- Cerma K, et al. Biomedicines 2023;11(1):109.
- Bhave MA, et al. Breast Cancer Res Treat 2024;207(3):599–609.
- Papa A, et al. Biomolecules 2019;9(1):29.
- Kassenärztliche Bundesvereinigung (KBV). Online-Version des EBM (Stand 2025/Q3). Erhältlich unter: https://ebm.kbv.de. Letzter Zugriff: August 2025
- Chaki M, et al. Breast Cancer Res 2025;27(1):122.
- Galvano A, et al. Ther Adv Med Oncol 2022;14:17588359221110162.


