PI3K/AKT/PTEN Signalweg-Alterationen
Etwa 40 % aller soliden Tumoren weisen genomische Veränderungen in den Genen PIK3CA, AKT1 oder PTEN auf, die zu einer Hyperaktivierung des Signalweges führen können. Dies trifft besonders auf Tumoren des Endometriums und der Brust zu, ist aber auch in anderen Entitäten als Biomarker relevant.1,2
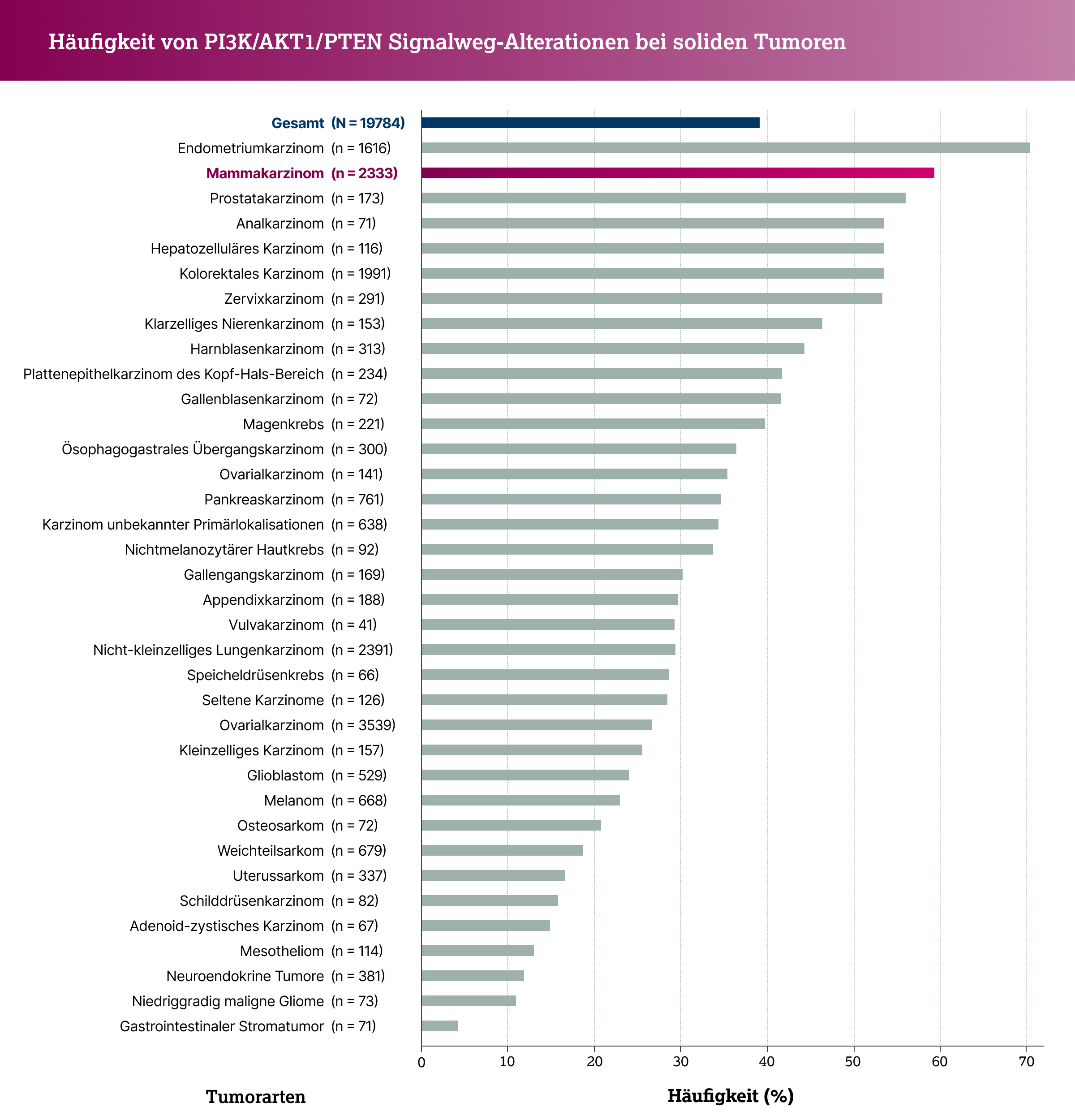
Im HR-positiven, HER2-negativen Mammakarzinom ergibt sich eine Gesamtprävalenz von ca. 50 % an Alterationen in PIK3CA (ca. 40 %), AKT1 (ca. 5 %) und PTEN (ca. 5 %).2,3 Durch gain-of-function-Mutationen in PIK3CA und AKT1 bzw. loss-of-function-Alterationen in PTEN sind Hyperaktivierungen des Signalwegs die Folge. Die Hyperaktivierung ist im Mammakarzinom mit einer Resistenz gegenüber endokrinen Therapien assoziiert und beschleunigt die Progression sowie die Entwicklung von Chemotherapie-Resistenzen.4,5

Durch die Alterationen werden die Proteine PI3K und AKT in ihrer Funktion verstärkt oder dauerhaft (konstitutiv) aktiviert. Die meisten PIK3CA-Mutationen kommen in der Helix- und Kinase-Domäne vor. Hier liegen vier Hotspot-Mutationen vor, die bis zu 80 % der PIK3CA-Mutationen ausmachen.6,7
Alterationen im AKT1-Gen sind in der Regel im Exon 2 lokalisiert. Am häufigsten ist mit ca. 40–75 % aller AKT1-Alterationen die E17K-Mutation. Diese Mutation beeinflusst die PH-Domäne, welche wesentlich für die Proteinaktivität ist.8–11
Die Funktion des Tumorsuppressorproteins PTEN wird durch Alterationen im PTEN-Gen in der Regel inaktiviert.12 Es können multiple genomische Alterationen, einschließlich Frameshift-Mutationen und Deletionen, auftreten. Diese inhibieren die katalytische Phosphatase-Domäne oder resultieren in einer stark verkürzten Aminosäureabfolge und folglich einem Protein mit reduzierter oder keiner Aktivität (loss-of-function).8,13 Die Folge ist die verringerte Umwandlung von PIP3 zu PIP2, was die Balance in Richtung Hyperaktivität des Signalwegs verschiebt.12,13
Dynamik molekularer Alterationen im Krankheitsverlauf des Mammakarzinoms: Stabilität von PIK3CA/AKT1/PTEN vs. Zunahme von ESR1-Mutationen
Nur wenige Studien untersuchen PIK3CA-, AKT1- bzw. PTEN-Alterationen systematisch vom frühen bis zum fortgeschrittenen Stadium des Mammakarzinoms. Die Angaben zu Prävalenzen der verschiedenen Alterationen in Primärtumoren bzw. Metastasen variieren je nach Datensatz.11,14–16 Basierend auf der Datenlage ist davon auszugehen, dass PIK3CA-, AKT1- und PTEN-Alterationen zwischen der primären und der metastasierten Erkrankung weitgehend stabil sind.
Neben Alterationen von PIK3CA, AKT1 und PTEN sind Mutationen im ESR1-Gen ebenfalls relevant und wurden als ein Hauptmechanismus für die erworbene Resistenz gegen endokrine Therapien identifiziert. ESR1 kodiert für das Östrogenrezeptor-Alpha-Protein. Mutationen im ESR1-Gen können zu einer konstitutiven Aktivierung des ER-Signalwegs führen. Die Aktivierung ist wiederum unbeeinflusst von einer durch Aromatasehemmer-bedingten Östrogenreduktion.9,17,18
Während Alterationen im PI3K/AKT/PTEN-Signalweg über den Krankheitsverlauf hinweg eine vergleichsweise konstante Prävalenz von etwa 50 % aufweisen, nimmt die Häufigkeit von ESR1-Mutationen im Verlauf der Erkrankung signifikant zu – insbesondere unter Selektionsdruck endokriner Therapien in späteren Therapielinien. Vor diesem Hintergrund empfehlen die ASCO (American Society for Clinical Oncology) und das NCCN (National Comprehensive Cancer Network) den Einsatz der Liquid Biopsy zur Detektion von ESR1-Mutationen ab der zweiten Therapielinie.19,20
Abkürzungen
AKT: AKT Serin/Threonin-Kinase (Protein); AKT1: AKT Serin/Threonin-Kinase 1 (Gen); ASCO: American Society of Clinical Oncology; ER: Östrogenrezeptor; ESR1: Östrogenrezeptor-1 (Gen); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HR+: Hormonrezeptor-positiv; NCCN: National Comprehensive Cancer Network; NSCLC: nicht-kleinzelliges Lungenkarzinom; PI3K: Phosphoinositid-3-Kinase (Protein); PIK3CA: Phosphoinositid-3-Kinase katalytische Untereinheit alpha (Gen); PTEN: Phosphatase- und Tensin- Homolog (Gen); PTEN: Phosphatase- und Tensin- Homolog (Protein); SCLC: kleinzelliges Lungenkarzinom
- Rodon J, et al. Nat Rev Clin Oncol. 2013;10(3):143-53.
- Millis SZ, et al. JAMA Oncol. 2016;2(12):1565-1573.
- Cancer Genome Atlas Network Nature. 2012;490(7418):61-70.
- Martorana F, et al. Front Pharmacol. 2021:12:662232
- Paplomata E, et al. Ther Adv Med Oncol. 2014;6(4):154-66.
- Ellis H, et al. Curr Oncol Rep. 2019;21(12):110.
- Keraite I, et al. Sci Rep 2020;10:17082.
- Miricescu D, et al. Int J Mol Sci. 2020;22(1):173.
- Alves S, et al. Int. J. Mol. Sci. 2023; 24(5):4522.
- Yi KH, et al. Oncotarget. 2016;7(4):4241-51.
- AKT1 E17K - My Cancer Genome, 2025. (https://www.mycancergenome.org/content/alteration/akt1-e17k/). Letzter Zugriff: Dezember 2025.
- Wang X, et al. Cell Research. 2008 ;18:807–816.
- Criscitiello C, et al. J. Mol. Pathol. 2021;2(1):42-54.
- Lefebvre C, et al. PLoS Med 2016;13:e1002201.
- Fumagalli D, et al. Ann Oncol 2016;27:1860–6.
- Razavi P, et al. Cancer Cell 2018;34:427-438.e6.
- Hanker AB, et al. Cancer Cell 2020;37:496–513.
- Osborne CK, et al. Annu Rev Med 2011;62:233–47.
- Bhave MA, et al. Breast Cancer Res Treat 2024;207:599–609.
- Bidard F-C, et al. J Clin Oncol 2022;40:3246–56.

