Therapiemöglichkeiten bei einem „kalten“ NSCLC-Tumor
Patient:innen mit fortgeschrittenem NSCLC und Co-Mutationen in KRAS und STK11 oder KEAP1 haben eine besonders ungünstige Prognose.1–3 Wie in verschiedenen Studien gezeigt werden konnte, sind Mutationen in STK11 und KEAP1 mit einer deutlich verringerten Wirksamkeit von PD-(L)1 Inhibitoren assoziiert.4–9
Ein wesentlicher Grund hierfür ist die Ausbildung einer sogenannten „kalten“ Tumormikroumgebung (tumor microenvironment, TME). Diese erlaubt es den Tumorzellen, der Immunüberwachung zu entgehen und reduziert die Effektivität immuntherapeutischer Ansätze.5,10,11 Charakteristisch für diese immunsuppressive Mikroumgebung sind
- eine geringe oder fehlende Expression von PD-(L)1
- eine niedrige Dichte infiltrierender zytotoxischer CD8+ T-Lymphozyten
- sowie eine Anreicherung neutrophiler Granulozyten.3,12
Umwandlung „kalter“ in „heiße“ Tumoren durch duale Immuncheckpoint-Blockade
Präklinische und klinische Daten legen nahe, dass Kombinationstherapien mit ICIs eine Reprogrammierung „kalter“ Tumoren in immunaktive („heiße“) Tumoren ermöglichen können.13,14
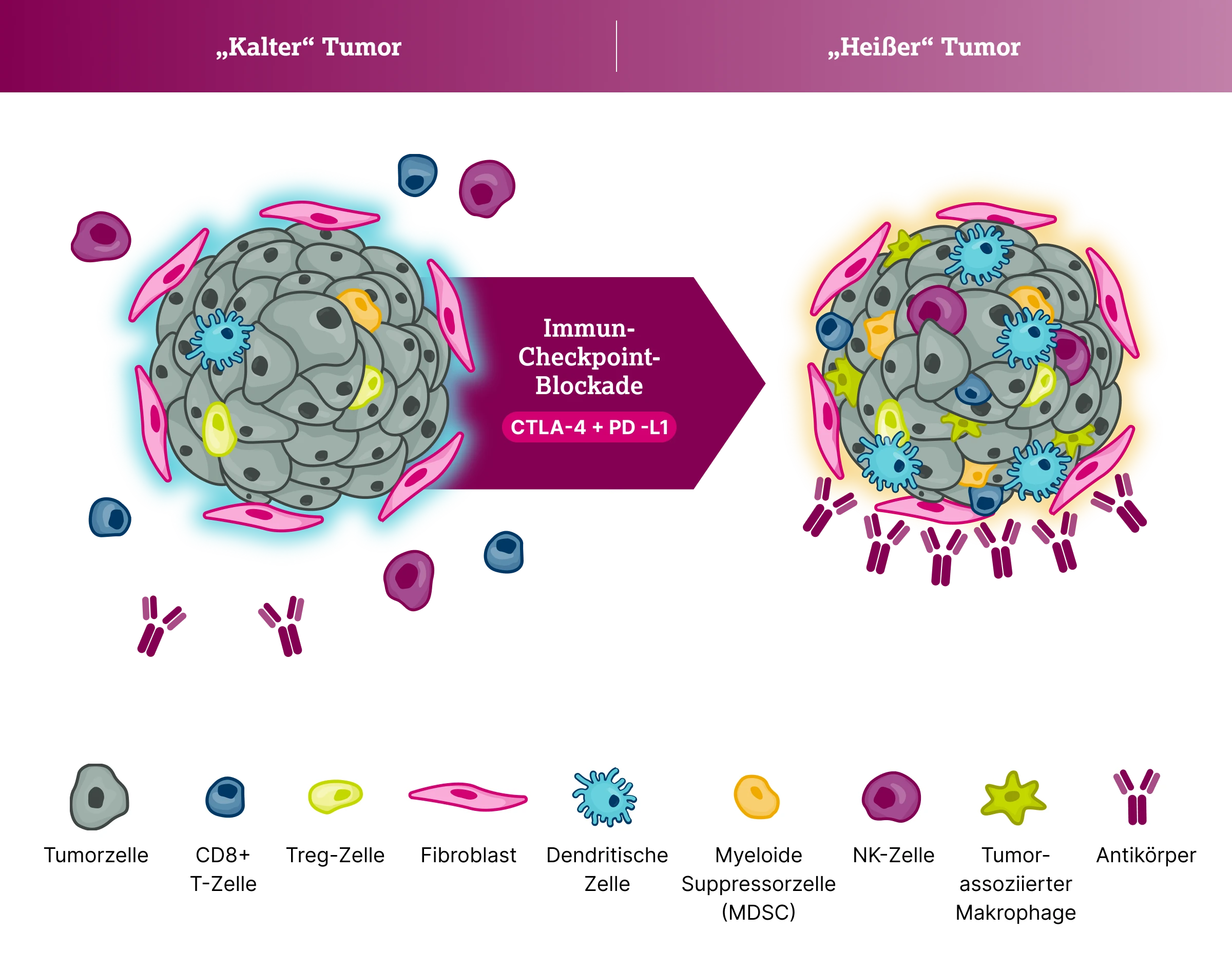
Tumoren versuchen den Angriffen des Immunsystems zu entkommen, indem sie ihre Mikroumgebung modulieren: Die erhöhte Präsenz von immunsuppressiver Zellen lässt sie zu einem "kalten" Tumor werden, der schlechter auf eine Immuntherapie anspricht.10 Eine doppelte Immun-Checkpoint-Blockade kann diesen Zustand möglicherweise ändern und die Immunantwort durch die Rekrutierung zytotoxischer T-Lymphozyten verstärken, so dass ein "heißer" Tumor" entsteht.12 "Heiße" Tumoren sprechen besser auf eine Immuntherapie an.
Beispielhaft zeigte die Hinzunahme eines CTLA-4 Inhibitors zur Kombination aus PD-L1 Inhibitor und Chemotherapie bei Patient:innen mit fortgeschrittenem NSCLC eine nahezu Verdopplung des medianen Gesamtüberlebens.12,13
Diese dreifache Kombinationstherapie stellt somit eine vielversprechende Erstlinienoption für Patient:innen mit molekular komplexem, immunresistentem mNSCLC dar.13,16
Immuncheckpoint-Inhibition: Mechanismen und Synergieeffekte
Aktuell zugelassene ICIs zielen auf unterschiedliche Immuncheckpoints, darunter
- CTLA-4, das zytotoxische T-Lymphozyten-assoziierte Protein 4,
- PD-1, den Rezeptor für den programmierten Zelltod 1 und
- PD-L1, den Liganden 1 für den programmierten Zelltod.16
Diese Moleküle fungieren als negativ regulatorische Signale der T-Zell-Aktivierung, unterscheiden sich jedoch in ihrer Funktion:17
- CTLA-4 wirkt primär in der Frühphase der Immunantwort – insbesondere in Lymphknoten –, indem es die Proliferation von T-Zellen hemmt.
- PD-(L)1 greift vorrangig in der Spätphase der Immunantwort ein, vor allem im peripheren Gewebe.
Das synergistische Potenzial der gleichzeitigen Blockade von PD-(L)1 und CTLA-4 zielt darauf ab, eine effektive antitumorale T-Zell-Antwort zu induzieren und das immunologische Gleichgewicht zugunsten einer tumorgerichteten Immunaktivierung zu verschieben.18

Informationen zum Immuncheckpoint PD-L1.
Deep Dive: Der CTLA-4 Checkpoint und seine Blockade
Das zytotoxische T-Lymphozyten-assoziierte Protein 4 (CTLA-4) ist ein Immun-Checkpoint-Molekül, das von T-Helferzellen, zytotoxischen T-Zellen, aber auch regulatorischen T-Zellen (Tregs) exprimiert wird. CTLA-4 (synonym CD152) ist ein Transmembranrezeptor an der Oberfläche von T-Lymphozyten, wo er einen Teil der sog. Immunsynapse bildet.19,20 Die Aktivierung der zytotoxischen T-Zellen erfolgt in zwei Phasen:
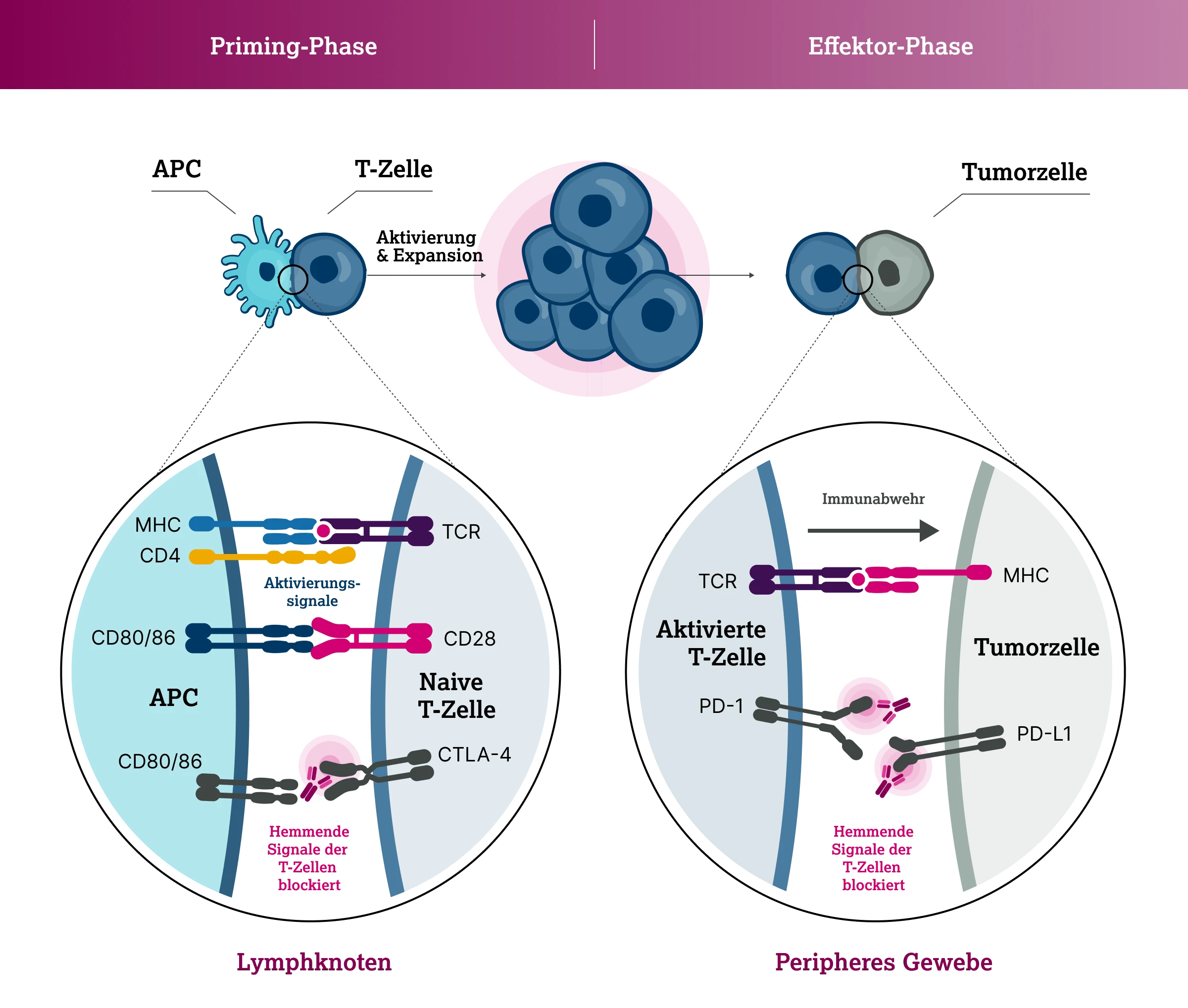
Priming-Phase
T-Zellen nutzen ihren T-Zell-Rezeptor (TCR), um Antigene aufzuspüren, die vom Haupthistokompatibilitätskomplex (MHC Klasse I oder II) auf der Oberfläche von antigenpräsentierenden Zellen (APC) bereitgestellt werden. Dieses erste Signal reicht jedoch nicht aus, um die T-Zellen zu aktivieren.
Effektor-Phase:
Das zweite Signal, das für die Synapsenbildung notwendig ist, ist die Interaktion der co-stimulierenden CD80/CD86-Moleküle auf der Oberfläche von APC mit CD28 auf der Oberfläche der T-Zellen. Dies führt schließlich zur T-Zell-Aktivierung und -Expansion.19,20 Die CTLA-4 Expression wird kurz nach der T-Zell-Aktivierung hochreguliert.
Unter normalen physiologischen Bedingungen binden die CTLA-4 Rezeptoren auf aktivierten T-Zellen mit höherer Affinität und Avidität an beide Liganden (CD80 und CD86) und senden im Gegensatz zu CD28 ein hemmendes Signal an die T-Zellen. Dies führt zur Verringerung der Proliferation von T-Zellen, Hemmung der Aktivität regulatorischer Tregs und Verringerung der Zytokinsekretion und damit zur Immunsuppression.20
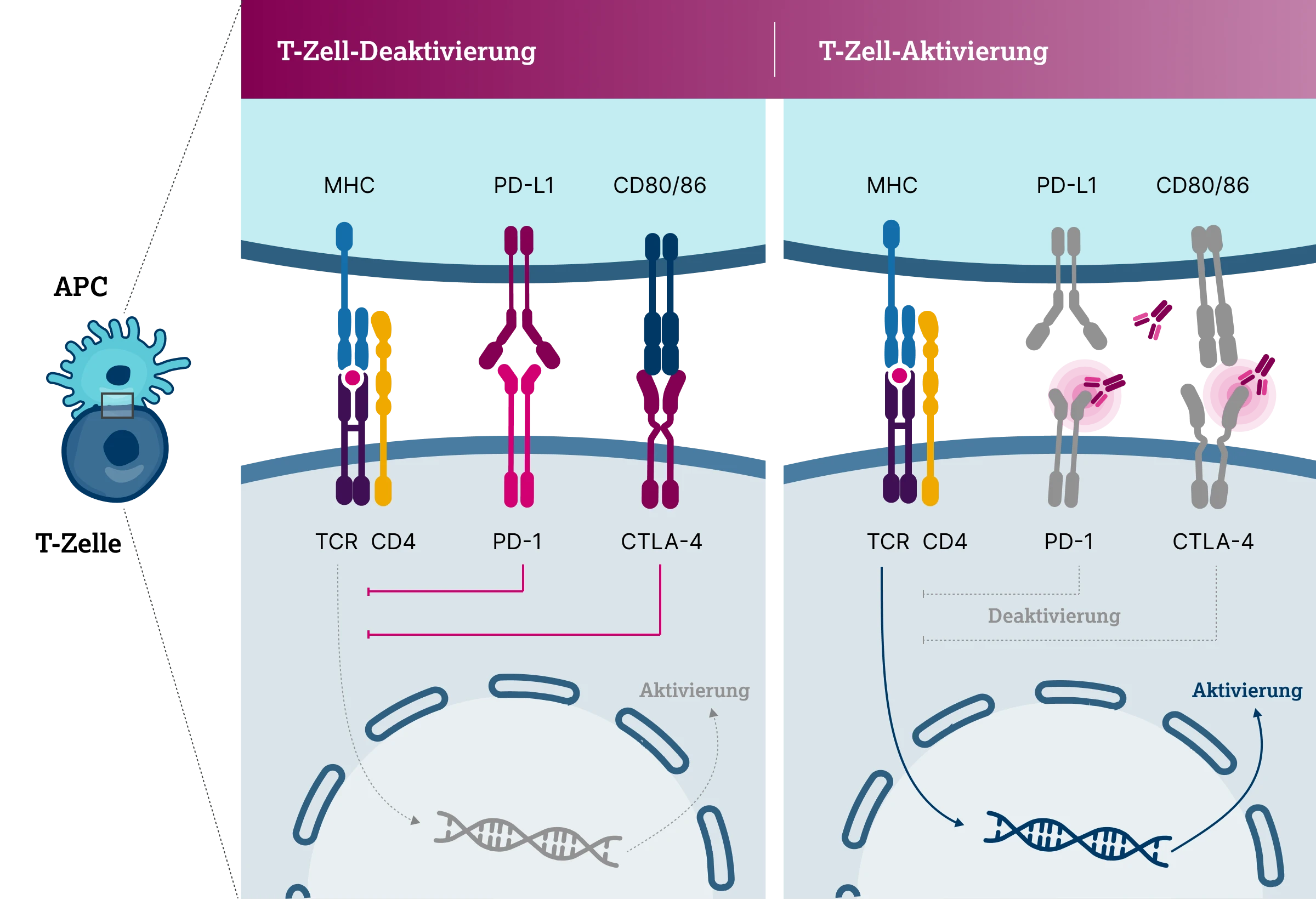
Umprogrammierung von T-Helferzellen
Außerdem führt eine hohe Expression von CTLA-4 zu einer funktionellen Umprogrammierung von T-Helferzellen in Tregs, die starke immunsuppressive Eigenschaften aufweisen.19 Tumoren rekrutieren häufig Tregs in die TME und nutzen ihre immunsuppressiven Funktionen, um die Anti-Tumor-Immunreaktionen des Wirts zu umgehen.23 Die Treg-Spiegel im TME und im peripheren Blut von Krebspatienten sind häufig höher als bei gesunden Kontrollpersonen und korrelieren mit einem ungünstigen klinischen Verlauf und einem niedrigeren Gesamtüberleben.23 Aufgrund seiner konstitutiven Expression auf Tregs ist CTLA-4 ein ideales Ziel, um die suppressiven Funktionen von Tregs im TME selektiv zu verringern oder zu hemmen.
Mithilfe von Anti-CTLA-4 Inhibitoren kann der CTLA-4 Signalweg gehemmt und tumorspezifische T-Zellen gefördert und reaktiviert werden. So wirken Anti-CTLA-4 Inhibitoren der Fähigkeit von Tumorzellen, sich der Immunüberwachung des Wirts zu entziehen, entgegen.22 Bereits in der frühen Phase der T-Zell -Aktivierung werden antitumorale Effekte ausgelöst und die Bekämpfung der Tumorzellen durch das eigene Immunsystem verstärkt. Die genauen Mechanismen von Anti-CTLA-4 Inhibitoren sind nach wie vor nicht eindeutig geklärt. Präklinische Hinweise deuten jedoch darauf hin, dass die Verarmung der Tregs oder die Aufhebung ihrer Funktion der Hauptfaktor für die Anti-Tumor-Aktivität der CTLA-4 Blockade sein könnte.23
Rationale für eine kombinierte PD-L1 und CTLA-4 Blockade
Eine kombinierte Blockade von PD-(L)1 und CTLA-4 kann gegenüber der alleinigen Blockade des PD-(L)1 Signalwegs zu synergistischen Effekten führen:22,24
Die Blockade von PD-(L)1 ist mit einer Hochregulierung von CTLA-4 verbunden, so dass eine direkte zusätzliche Blockade eine weitere Immunflucht verhindern kann.
Myeloide Suppressorzellen (MDSC) können die T-Zell-Aktivität innerhalb der TME stark einschränken, aber eine kombinierte Blockade kann den Anteil der CD8+ Effektor-T-Zellen im Verhältnis zu den MDSC synergistisch erhöhen.
Die kombinierte Checkpoint-Blockade erhöht die Produktion von Entzündungszytokinen wie TNF-alpha und IFN-gamma und verringert die T-Zell-Anergie.
Schließlich kann die kombinierte Blockade zur Vermehrung von Gedächtnis-T-Zellen führen, die im Vergleich zu Effektor-T-Zellen eine längerfristige Anti-Tumor-Immunität verleihen können.
Insgesamt kann eine duale Immun-Checkpoint-Blockade die Chance erhöhen, in einer "immunkalten" Tumormikroumgebung eine Immunantwort auszulösen.
Abkürzungen
APC: Antigenpräsentierende Zellen; CD: Cluster of Differentiation; CD8+: zytotoxische T-Zelle; ctDNA: zirkulierende Tumor-DNA; CTLA-4: T-Lymphozyten-assoziiertes Protein 4; FFPE: formalinfixiert, paraffineingebettet; ICI: Immuncheckpoint-Inhibitor; IFN: Interferon; IHC: Immunohistochemie; KEAP1: Kelch-like ECH-associated protein 1 (Gen); KRAS: Kirsten Rat Sarkoma (Gen); MDSC: Myeloide Suppressorzelle; MHC: Haupthistokompatibilitätskomplex; NGS: Next-Generation-Sequencing; NK: Natural Killer; NSCLC: nicht-kleinzelliges Lungenkarzinom; PD-1: Programmed cell death-1; PD-L1: Programmed cell death ligand-1; STK11: Serin/Threonin-Kinase 11 (Gen); TCR: T-Zell-Rezeptor; TME: Tumormikroumgebung; TNF: Tumornekrosefaktor; Tregs: regulatorische T-Zellen
- Cekani E, et al. Cancers (Basel) 2022;14(17):4103.
- Riely GJ, et al. J Clin Oncol 2016;34(15_suppl):9019.
- Shire NJ, et al. PLoS ONE 2020;15(9):e0238358.
- Papillon-Cavanagh S, et al. ESMO Open 2020;5(2):e000706.
- Skoulidis F, et al. Cancer Discov 2018;8(7):822–35.
- Di Federico A, et al. Eur J Cancer 2021;157:108–13.
- Di Federico A, et al. J Natl Cancer Inst 2023;115(1):29–42.
- Marinelli D, et al. Ann Oncol 2020;31(12):1746–54.
- Ricciuti B, et al. J Thorac Oncol 2022;17(3):399–410.
- Appleton E, et al. Front Immunol 2021;12:754436.
- Wang M, et al. Clin Transl Immunology 2020;9(12):e1226.
- Pons-Tostivint E, et al. Cells 2021;10(11):3129.
- Cheng L, et al. Cancer Immunol Immunother 2022;71(5):1167–81.
- Skoulidis F, et al. Nature 2024;635(8038):462–71.
- Llinàs-Arias P, et al. Cancers (Basel) 2021;13(16):4139.
- Perrier A, et al. Biomolecules 2020;10(7):1061.
- Buchbinder EI, et al. Am J Clin Oncol 2016;39(1):98–106.
- Wei SC, et al. Cancer Discov 2018;8(9):1069–86.
- Wojtukiewicz MZ, et al. Cancer Metastasis Rev 2021;40(3):949–82.
- Poto R, et al. Front Immunol 2022;13:804597.
- Awadasseid A, et al. Biomed Pharmacother 2021;142:111957.
- Dong Y, et al. Cancers (Basel) 2021;13(8):1949.
- Hong MMY, et al. Cancers (Basel) 2022;14(6):1580.
- Rotte A. J Exp Clin Cancer Res 2019;38(1):255.