DNA-Reparaturdefekte in verschiedenen Tumorentitäten
Eine der grundlegenden Eigenschaften maligner Tumoren ist die genomische Instabilität. Sie entsteht, wenn Schäden am Erbgut nicht effizient behoben werden – etwa als Folge defekter DNA-Reparaturmechanismen.1 Solche Defekte können einen hereditären Ursprung haben (Keimbahnmutationen) oder im Laufe des Lebens durch somatische Mutationen entstehen, beispielsweise in den Genen Breast Cancer Associated Gene 1 (BRCA1) oder Breast Cancer Associated Gene 2 (BRCA2) oder in anderen für Reparaturproteine kodierenden Genen. Für zahlreiche Tumorentitäten sind inzwischen charakteristische Reparaturdefekte bekannt.2
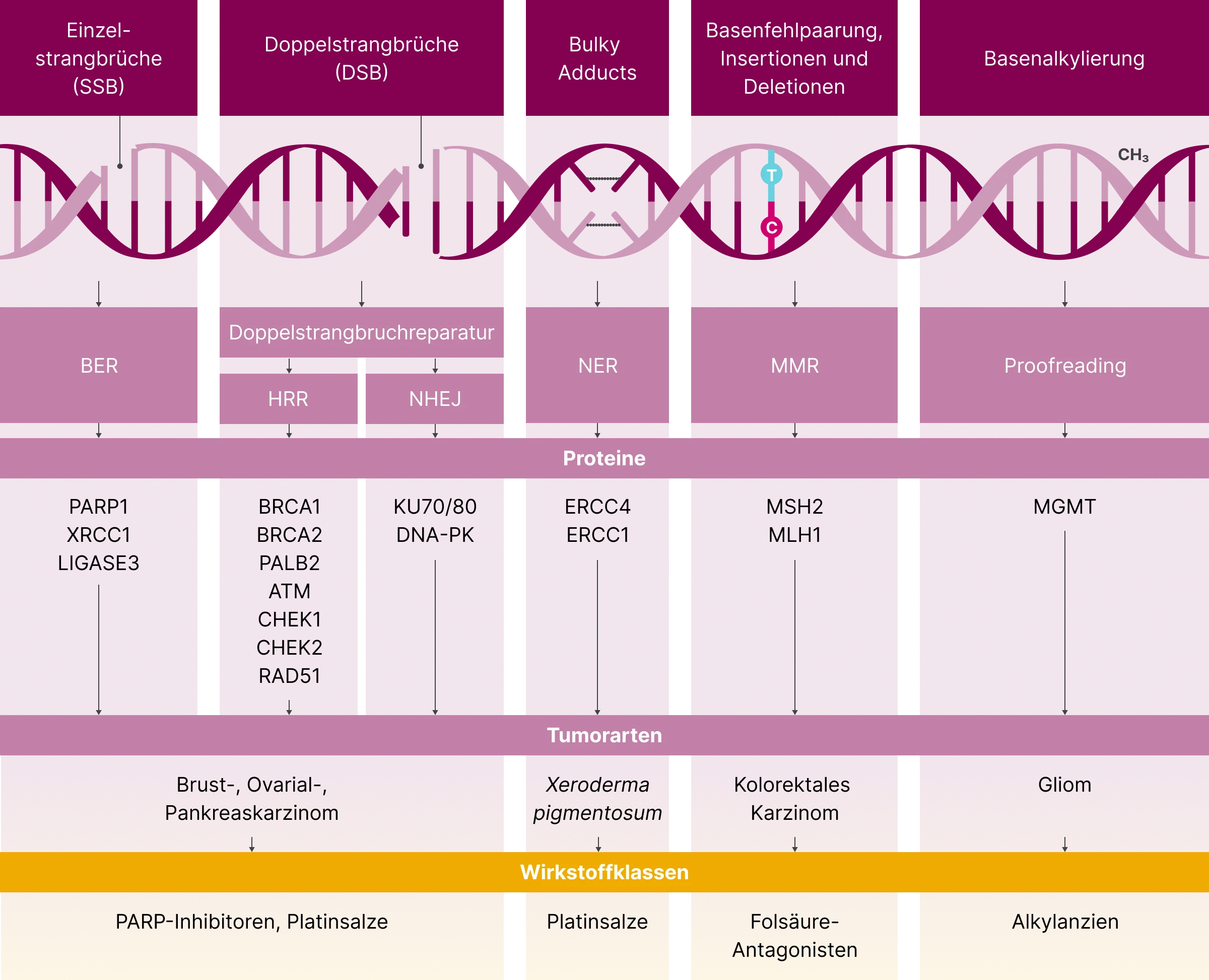
Die homologe Rekombinationsreparatur (HRR) ist beispielsweise vermehrt bei Mamma-, Ovarial-, Prostata- und Pankreaskarzinomen beeinträchtigt, während bei kolorektalen Karzinomen typischerweise Störungen in der DNA-Mismatch-Reparatur (MMR) vorliegen. Bei Gliomen ist hingegen häufig der einfache Mechanismus des Proofreading gestört.2 Die folgende Abbildung gibt einen Überblick über beispielhafte Defekte in DNA-Reparaturmechanismen bei verschiedenen Krebserkrankungen.

Informationen zu den Funktionen von HRD.
Mutationen in HRR-Genen bei unterschiedlichen Tumorentitäten
Homologe Rekombinationsdefizienz (HRD) beschreibt den Funktionsverlust der HRR. In einer groß angelegten Studie wurden die molekularen Profile von über 50.000 Tumoren unterschiedlicher Entitäten hinsichtlich Mutationen in HRR-Genen analysiert.3 Die Ergebnisse zeigten, dass die relative Häufigkeit von HRR-Genveränderungen je nach Tumorart deutlich variiert.
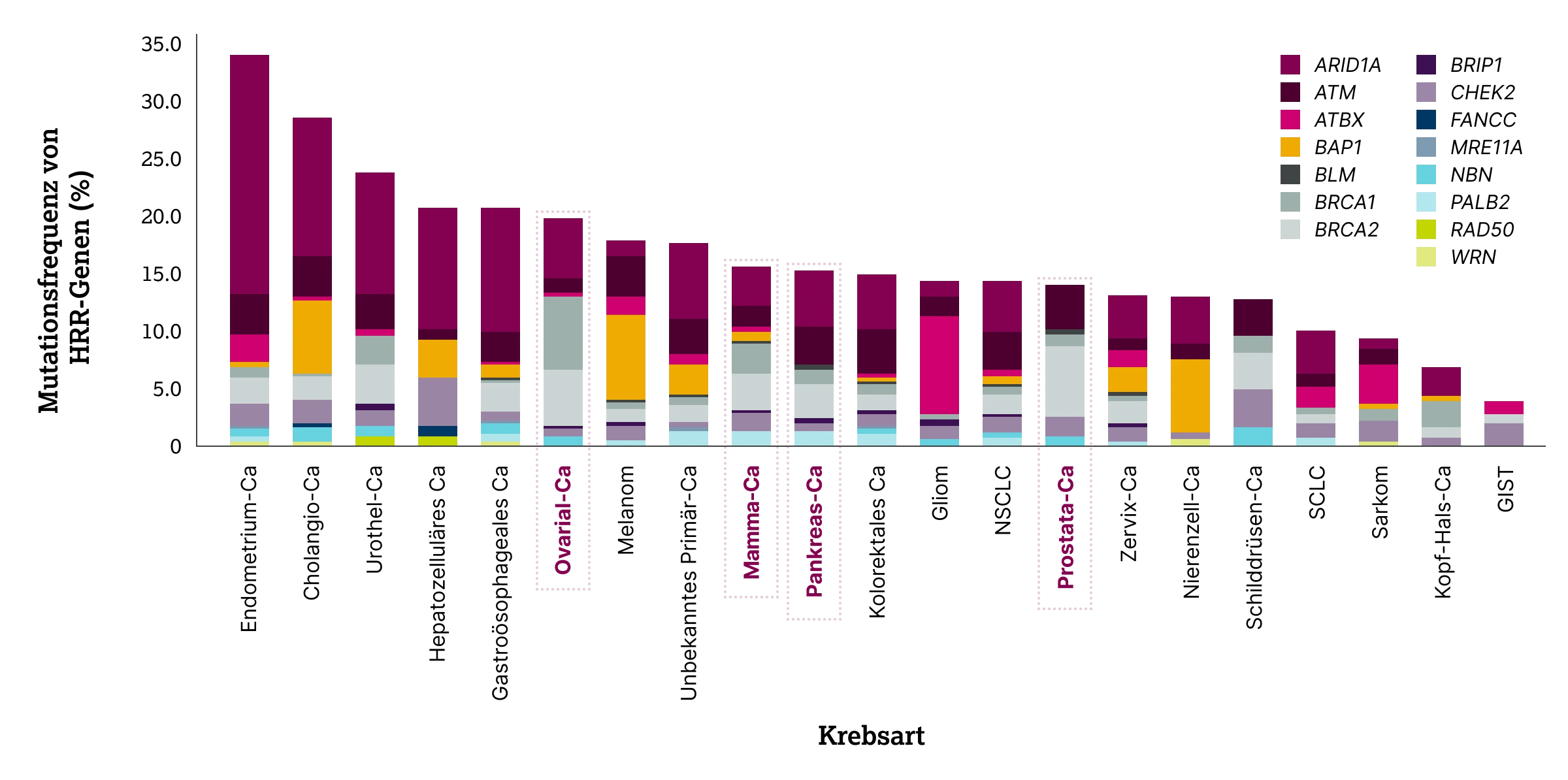
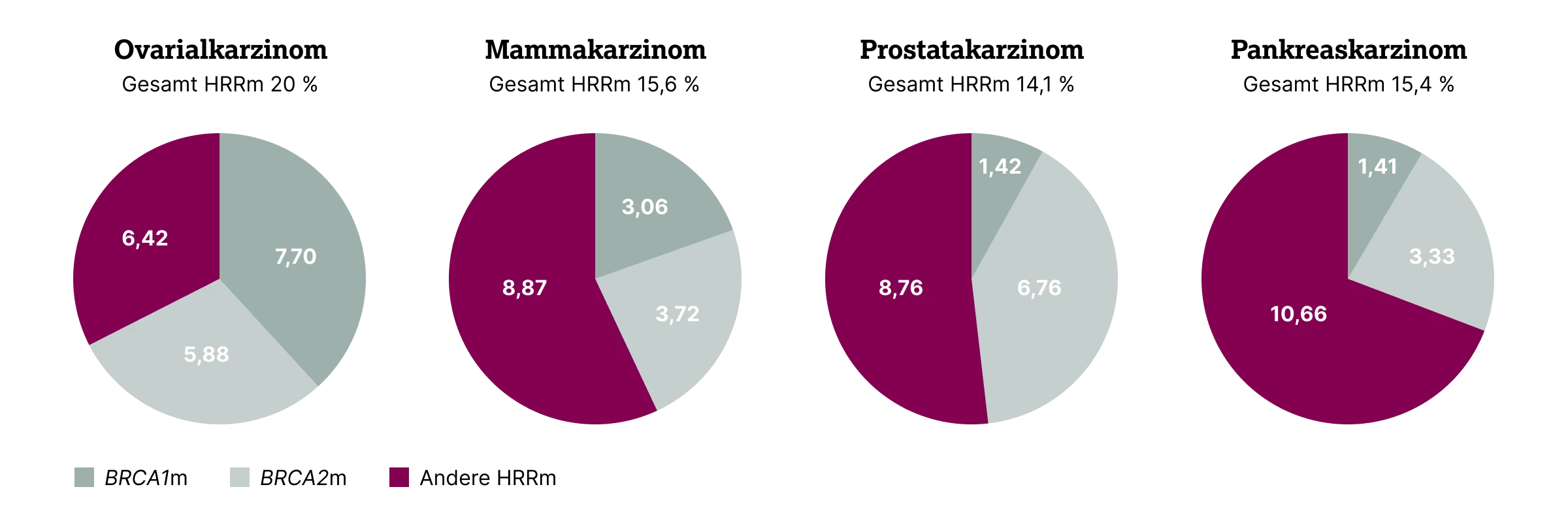
Beim HRD-assoziierten Ovarialkarzinom stellen Mutationen in BRCA1 gefolgt von BRCA2 die häufigsten Genveränderungen dar (insgesamt etwa 70 %). Beim Mamma-, Prostata- und insbesondere Pankreaskarzinom treten hingegen häufiger Mutationen in anderen HRR-Genen auf.
Eine weitere Studie mit 390 Patientinnen mit Ovarialkarzinom untersuchte Mutationen in BRCA1/2, RAD51C/D, PALB2, NBN, FAM175A, CHEK1/2, BRIP1 und BARD1 und zeigte, dass die Mutationsrate in HRR-Genen unter den Erkrankten bei insgesamt 31,3 % lag. Davon entfielen 22,6 % auf Keimbahnmutationen, 7,6 % auf somatische Mutationen und bei 1,1 % wurde sowohl eine Keimbahn- als auch eine somatische Mutation nachgewiesen. Übereinstimmend mit der oben beschriebenen Studie machten BRCA1- und BRCA2‑Mutationen dabei etwa 70 % der HRR‑Mutationen aus.4
In der AGO‑TR1‑Studie wurden bei 26,4 % der 523 inkludierten Patientinnen mit Ovarialkarzinom Keimbahnmutationen in HRR-Genen detektiert (untersucht wurden16 HRR-Gene: ATM, BRCA1, BRCA2, CDH1, CHEK2, MLH1, MSH2, MSH6, NBN, PMS2, PTEN, PALB2, RAD51C, RAD51D, STK11, TP53). BRCA1/2-Mutationen in der Keimbahn fanden sich bei 21 % der Erkrankten.5 Die Autor:innen schlossen daraus, dass die alleinige Analyse von BRCA-Mutationen mehr als 5 % der HRD‑Fälle nicht erfassen würde. Die obere Abbildung lässt vermuten, dass dieser Anteil bei Tumorentitäten wie Mamma-, Prostata- und Pankreaskarzinom noch weitaus höher ist.
Abkürzungen
AGO-TR1: Arbeitsgemeinschaft Gynäkologische Onkologie – Translational Research Studie 1; ARID1A: AT‑Rich Interaction Domain 1A (Gen); ATM: Ataxia Telangiectasia Mutated (Gen); BAP1: BRCA1 Associated Deubiquitinase 1 (Gen); BARD1: BRCA1 Associated Ring Domain 1 (Gen); BER: Basenexzisionsreparatur; BLM: BLM RecQ Like Helicase (Gen); BRCA1: Breast Cancer Associated Gene 1; BRCA2: Breast Cancer Associated Gene 2; BRIP1: BRCA1‑Interacting Protein 1 (Gen); Ca: Karzinom; CDH1: Cadherin 1 (Gen); CHEK1: Checkpoint Kinase 1 (Gen); CHEK2: Checkpoint Kinase 2 (Gen); DDR: DNA‑Damage‑Response; DNA: Desoxyribonukleinsäure; FAM175A: Abraxas 1, BRCA1 A Complex Subunit (Gen); FANCC: Fanconi Anemia Complementation Group C (Gen); GIST: Gastrointestinaler Stromatumor; HR: homologe Rekombination; HRD: homologe Rekombinationsdefizienz; HRR: homologe Rekombinationsreparatur; HRRm: HRR‑Mutation; MLH1: MutL Homolog 1; MLH1: MutL Homolog 1 (Gen); MMR: DNA-Mismatch-Reparatur; MRE11A: MRE11 Homolog, Double Strand Break Repair Nuclease A (Gen); MSH2: Mutator S Homolog 2; MSH2: Mutator S Homolog 2 (Gen); MSH6: Mutator S Homolog 6 (Gen); NBN: Nibrin (Gen); NER: Nukleotidexzisionsreparatur; NHEJ: nicht‑homologe Endverknüpfung; NSCLC: nicht‑kleinzelliges Lungenkarzinom; PALB2: Partner and Localizer of BRCA2 (Gen); PARP1: Poly(ADP‑ribose)‑Polymerase 1; PMS2:: Postmeiotic Segregation Increased 2 (Gen); PTEN: Phosphatase- und Tensin‑Homolog (Gen); RAD50: RAD50 Double Strand Break Repair Protein (Gen); RAD51C: RAD51 Paralog C (Gen); RAD51D: RAD51 Paralog D (Gen); SCLC: kleinzelliges Lungenkarzinom; STK11: Serin/Threonin‑Kinase‑11 (Gen); TP53: Tumorsuppressor‑Protein P53 (Gen); WRN: WRN RecQ Like Helicase (Gen)
- Hanahan D & Weinberg RA. Cell 2011;144(5):646–74.
- Lord CJ & Ashworth A. Nature 2012;481(7381):287–94.
- Heeke AL, et al. JCO Precis Oncol 2018;2018:PO.17.00286.
- Pennington KP, et al. Clin Cancer Res 2014;20(3):764–75.
- Harter P, et al. PLoS One 2017;12(10):e0186043.



