MMR und MSI beim Endometriumkarzinom
Rolle von MMR und MSI beim Endometriumkarzinom
Endometriumkarzinome entstehen überwiegend sporadisch als Folge von erworbenen somatischen Veränderungen – darunter Veränderungen in Genen der DNA-Reparatursysteme. In einem Teil der Fälle ist das DNA-Mismatch-Reparatur (MMR)-System betroffen.1,2
Etwa 70 % der Endometriumkarzinome weisen eine profiziente MMR (pMMR) auf, d. h. eine funktionell intakte DNA-Mismatch-Reparatur.3 Trotz intakter MMR können in diesen Tumoren weitere molekulare Veränderungen vorliegen, z. B. eine homologe Rekombinationsdefizienz (HRD) mit konsekutiver genomischer Instabilität.4
In etwa 20–30 % der Fälle zeigt sich eine defiziente MMR (dMMR).5 Diese Tumoren weisen häufig eine Mikrosatelliteninstabilität (MSI) auf, die mit einer erhöhten Mutationslast einhergeht und klinisch sowie therapeutisch besonders relevant ist.6 Obwohl dMMR und MSI eng korrelieren und eine hohe diagnostische Konkordanz aufweisen, handelt es sich um unterschiedliche molekulare Phänomene, die als eigenständige Biomarker bewertet werden.7 Die Prävalenz von dMMR und pMMR kann je nach Studienkollektiv und untersuchter Population variieren.8
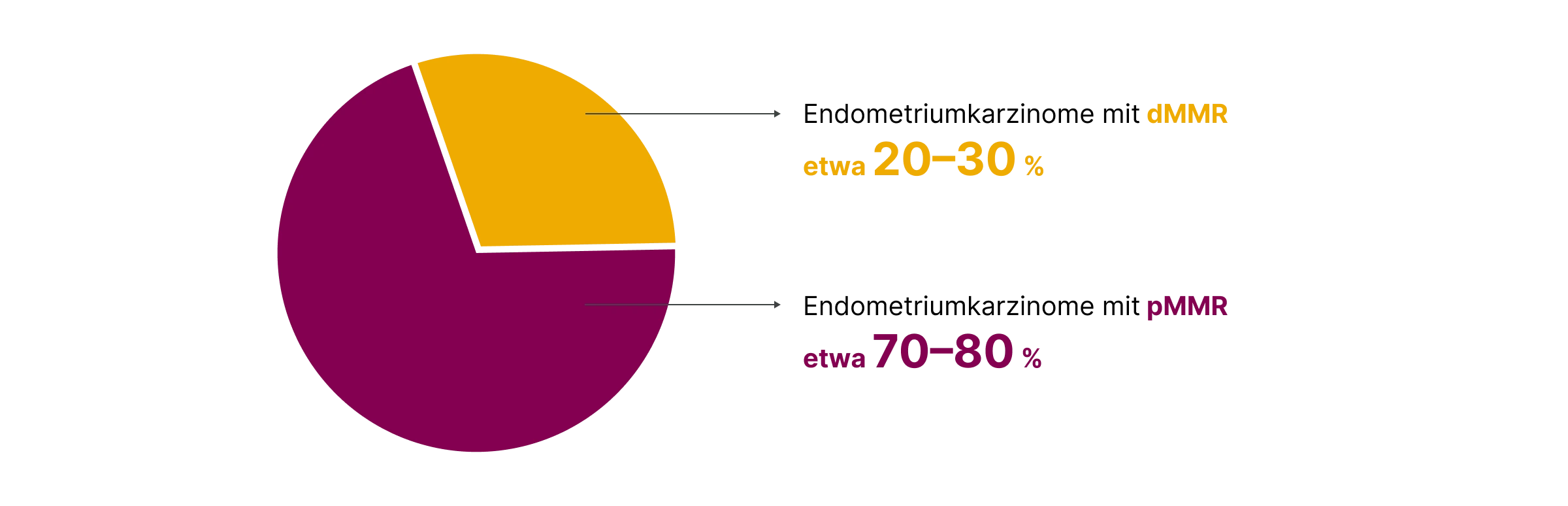
In der aktuellen S3-Leitlinie Endometriumkarzinom (2024) wird zwischen dMMR (defiziente MMR) und pMMR (profiziente MMR) unterschieden und empfohlen, bei allen neu diagnostizierten Fällen den MMR-Status immunhistochemisch zu bestimmen.8 Im Gegensatz dazu verwendet die neue ESGO–ESTRO–ESP-Leitlinie (2025) den Begriff non-MMRd anstelle von pMMR, da diese Gruppe keine molekular homogene Einheit darstellt.9 In der Praxis sollten daher beide Begrifflichkeiten bekannt sein, da sie je nach Leitlinie parallel in der Literatur und in Befundberichten auftreten.
MMR-Status: Diagnostik und klinische Relevanz
Die Bestimmung des MMR-Status erfolgt primär mittels Immunhistochemie (IHC) der vier zentralen DNA-Mismatch-Reparatur-Proteine (MLH1, PMS2, MSH2, MSH6). Das Fehlen der Expression eines oder mehrerer dieser Proteine weist auf eine dMMR hin.6 Empfohlen wird ein Zwei- oder Viermarker-Ansatz, wobei der Zwei-Antikörper-Ansatz (MSH6 und PMS2) dem klassischen Vier-Antikörper-Panel (MLH1, PMS2, MSH2, MSH6) gleichwertig ist.9 Bei Verlust von MLH1/PMS2 soll zusätzlich eine MLH1-Promotor-Methylierung bestimmt werden, um zwischen sporadischer Hypermethylierung und Lynch-assoziiertem Tumor zu unterscheiden.9 Nur wenn die IHC-Befunde uneindeutig oder heterogen sind, soll ergänzend eine MSI-Analyse mittels PCR durchgeführt werden.9
Der MMR-Status besitzt sowohl prognostische als auch prädiktive Bedeutung und ist entscheidend für die Therapieplanung.8,9
Bei fortgeschrittenen oder rezidivierten Endometriumkarzinomen mit dMMR wird heute eine Kombination aus platinhaltiger Chemotherapie und Immuncheckpoint-Inhibitor empfohlen, gefolgt von einer Erhaltungstherapie.8,9 Auch für pMMR/non-MMRd-Tumoren werden zunehmend innovative Therapiekonzepte, etwa Kombinationen von Immuncheckpoint-Inhibitoren mit Tyrosinkinase-Inhibitoren, erprobt. Darüber hinaus dient die MMR-Bestimmung als wichtiger Schritt in der Präselektion für das Lynch-Syndrom.8,9
Heterogenität pMMR-assozierter Endometriumkarzinome
Die Gruppe der pMMR/non-MMRd-Tumoren ist molekular heterogen und umfasst unterschiedliche Subtypen. Mit der Einführung der molekularen Klassifikation im Rahmen des TCGA-Projekts (The Cancer Genome Atlas)10 wurde die bisherige, rein histopathologische Einteilung zunehmend durch molekulare Methoden ergänzt.11 Dadurch verbessert sich die prognostische Einordnung erheblich.12
Nach TCGA werden vier molekulare Subtypen unterschieden:
dMMR/MSI
POLE-mutiert (POLEm)
p53-aberrant (p53abn)
NSMP (No Specific Molecular Profile)
Die Subgruppen unterscheiden sich in Mutationslast und Kopienzahlveränderungen. Während dMMR/MSI eine eigene Entität darstellt, fassen POLEm, p53abn und NSMP die heterogene Gruppe der pMMR-Tumoren zusammen. In dieser Gruppe können weitere relevante Biomarker (z. B. POLE, p53 oder HER2) von diagnostischer und therapeutischer Bedeutung sein.9,13,14
Die aktuelle ESGO-Guideline 2025 empfiehlt erstmals eine differenzierte Unterteilung der NSMP-Tumoren nach dem Östrogenrezeptor-Status (ER).9 NSMP-Karzinome werden seither als „NSMP, ER-positiv“ (≥ 10 % ER-Expression) und „NSMP, ER-negativ“ (< 10 % ER-Expression) klassifiziert, da diese Unterscheidung mit signifikanten Unterschieden im klinischen Verlauf und den Therapieempfehlungen einhergeht. Die Risikostratifizierung sowie Empfehlungen zu adjuvanten Therapien richten sich explizit nach dieser weiteren Subdifferenzierung.9
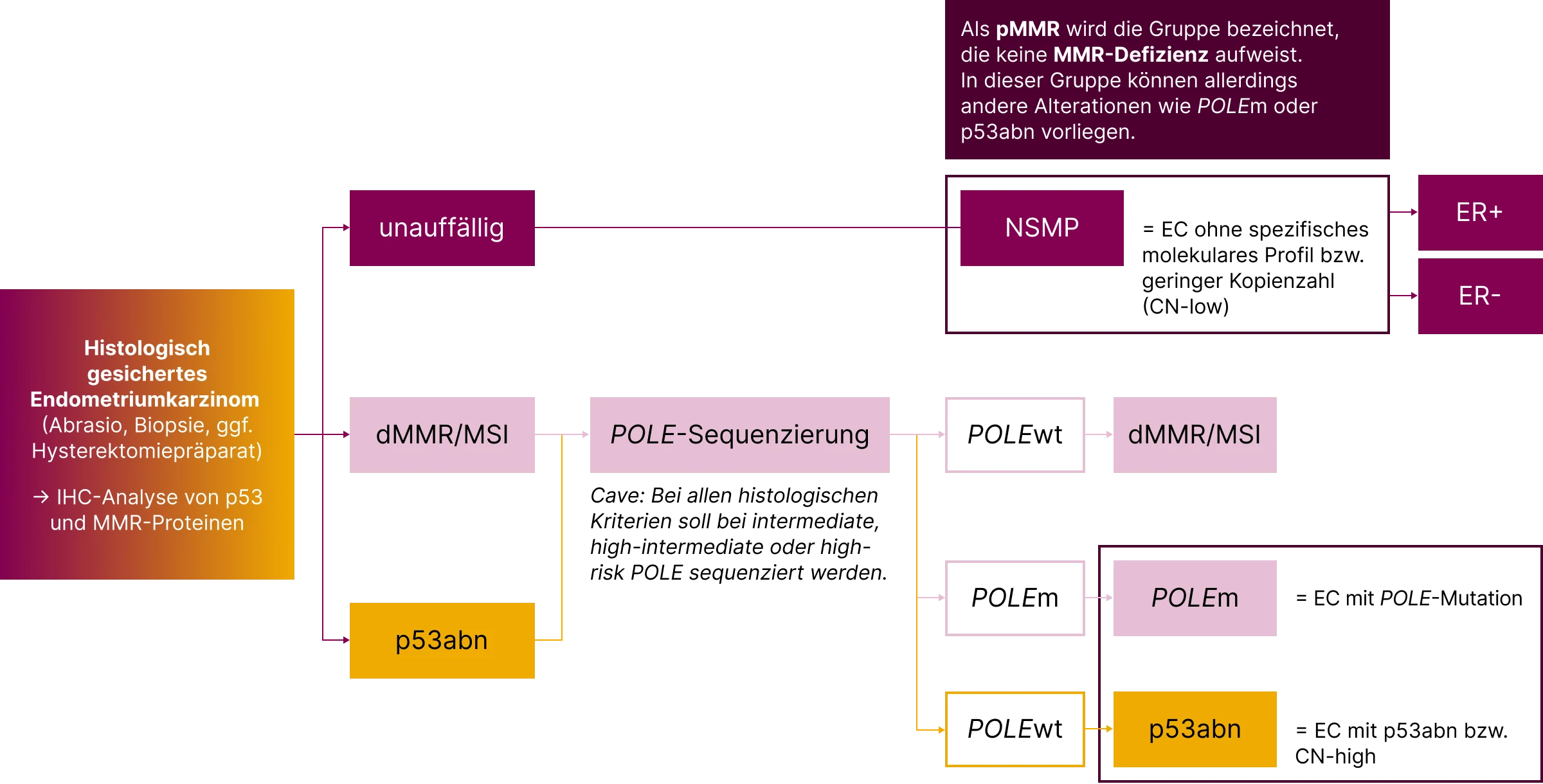
Diagnostischer Algorithmus und Anwendung in der Praxis
Die molekulare Typisierung wird aktuell standardmäßig beim endometrioiden Endometriumkarzinom eingesetzt. Für seltene histologische Subtypen ist die Datenlage eingeschränkt. Empfohlen wird jedoch in allen Fällen zumindest die immunhistochemische Analyse der MMR-Proteine und von p53. Für eine vollständige Klassifikation ist zusätzlich die POLE-Mutationsanalyse erforderlich. Deren Nutzen beim low-grade (G1–2), low-stage (Stadium I/pT1) ist allerdings weiterhin Gegenstand der Diskussion.8
Studien & Leitlinien-Empfehlungen zur MMR- und MSI-Testung beim Endometriumkarzinom

Die S3-Leitlinie betont die zentrale Rolle der MMR-Diagnostik beim Endometriumkarzinom – sowohl zur prognostischen Einschätzung als auch zur Erkennung eines möglichen Lynch-Syndroms und zur Therapieplanung.8,9
Die aktuelle S3-Leitlinie Endometriumkarzinom (2024) empfiehlt, bei allen neu diagnostizierten Endometriumkarzinomen eine immunhistochemische Bestimmung des MMR-Status durchzuführen.8
Dabei wird zwischen dMMR (defizient) und pMMR (profizient) unterschieden. Eine weiterführende MSI-Analyse soll nur erfolgen, wenn die IHC-Befunde unklar oder uneindeutig sind. Ergänzend wird eine POLE-Analyse bei höherem Risikoprofil sowie eine HER2-Testung beim serösen Karzinom empfohlen.8
Die ESGO–ESTRO–ESP-Leitlinie (2025) verwendet anstelle von pMMR den Begriff non-MMRd, um die Heterogenität dieser Gruppe zu verdeutlichen. Sie geht zudem über die S3-Empfehlungen hinaus und fordert eine vollständige molekulare Klassifikation für alle Endometriumkarzinome, unabhängig vom histologischen Subtyp.9
Diese umfasst:
- die immunhistochemische Analyse der MMR-Proteine (dMMR/pMMR),
- die Analyse der Exonuklease-Domäne von POLE (POLEmut),
- die immunhistochemische Analyse von p53 (p53abn),
- zusätzlich eine Bestimmung des Östrogenrezeptorstatus bei allen Subtypen (ER+/ER–)
- sowie die HER2-Analyse mittels IHC und In-situ-Hybridisierung, insbesondere bei p53-abrranten Tumoren, serösen Karzinomen und Karzinosarkomen.9
Für die IHC des MMR-Status empfehlen beide Leitlinien (S3 und ESGO) vorrangig ein Viermarker-Panel (MLH1, PMS2, MSH2, MSH6).

Alternativ ist auch ein Zweimarker-Panel (MSH6 und PMS2) möglich, das im Falle auffälliger oder unklarer Befunde durch die übrigen Marker ergänzt werden muss.8,9 Eine starke, homogene Kernfärbung aller getesteten Proteine gilt als Nachweis einer pMMR – in diesem Fall sind keine weiteren Analysen erforderlich. Laut S3 und ESGO soll eine MSI Analyse nach unklaren IHC-Ergebnissen folgen.8,9
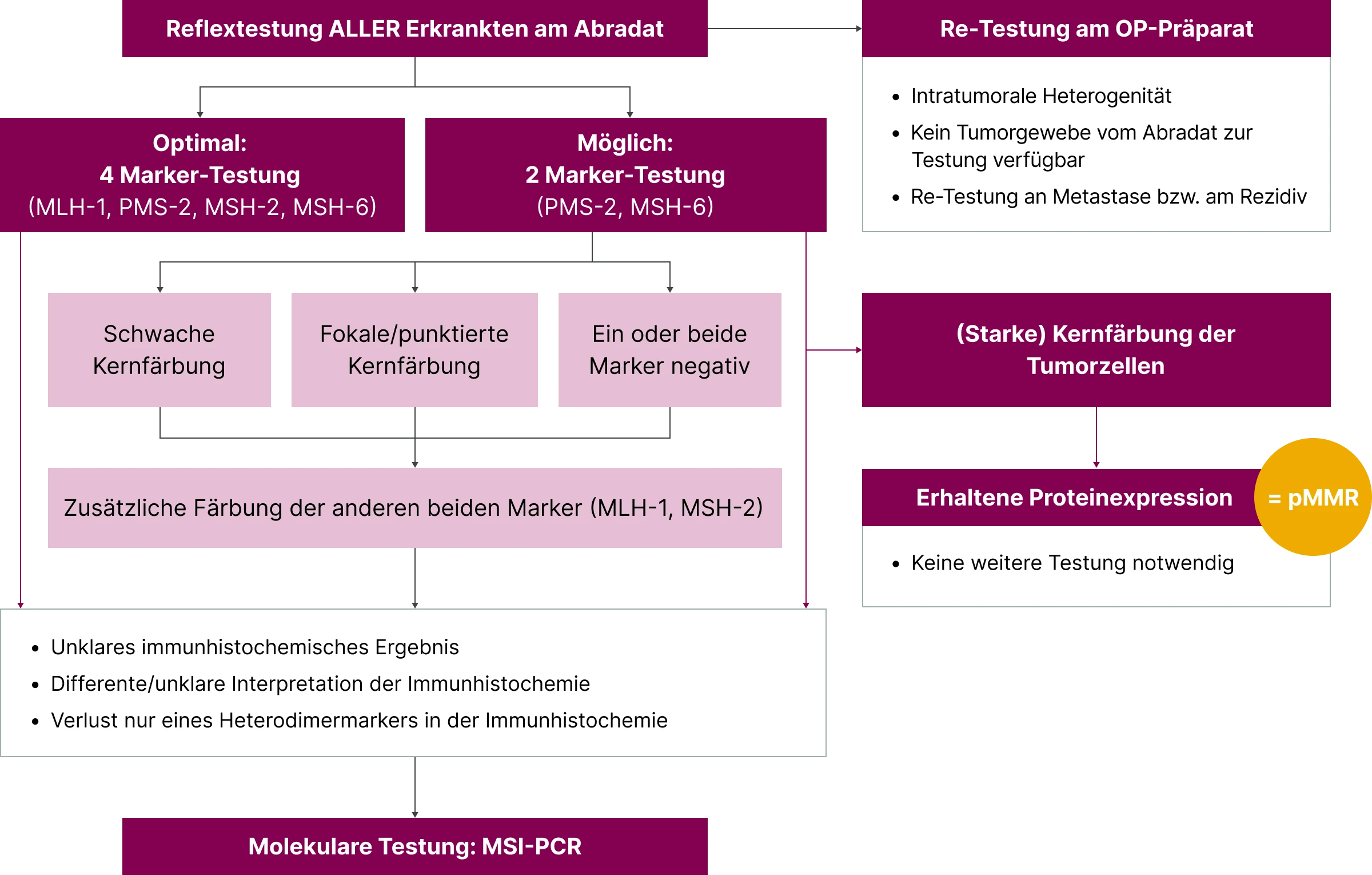
Empfehlungen zur MMR-/MSI-Diagnostik
Die Abbildung zeigt den empfohlenen Ablauf für die dMMR/pMMR-Analyse gemäß S3-Leitlinie.8 Für den MMR-Status wird präoperativ eine immunhistochemische Analyse am Abradat oder einer Endometriumbiopsie empfohlen, dabei wird die Verwendung des Abradats bevorzugt.8 Optimalerweise wird eine 4-Marker-Testung an MLH-1, PMS-2, MSH-2 und MSH-6 durchgeführt, die nur bei unklarem Befund durch eine nachgeschaltete MSI-Analyse ergänzt werden soll.8
Alternativ kann aber auch nur auf die beiden Marker PMS-2 und MSH-6 getestet werden – erst bei schwacher oder fokaler/punktierter Kernfärbung bzw. wenn einer der beiden Marker negativ ist, wird eine zusätzliche Färbung der anderen beiden Marker (MLH-1 und MSH-2) nachgeschaltet. Bei weiterhin unklarem Befund soll die Diagnostik durch eine MSI-Analyse mittels PCR ergänzt werden.8
Bei starker Kernfärbung liegt eine pMMR vor, in diesem Fall ist keine weitere Analyse notwendig.8 Laut ESMO-Empfehlungen soll jedoch an dieser Stelle zuerst eine PCR und alternativ eine NGS durchgeführt werden.6
Erweiterte Biomarkeranalysen gemäß Risikostratifizierung
Laut S3-Leitlinien wird die Analyse weiterer molekularer Marker, abhängig vom klinischen Risikoprofil, empfohlen:6
Bei low risk Endometriumkarzinomen kann eine IHC-Bestimmung von L1CAM durchgeführt werden.8
Bei G3 oder bei intermediate, high intermediate und high risk Endometriumkarzinomen soll eine Mutationsanalyse der Exonuklease-Domäne von POLE durchgeführt werden.8
Aufgrund einer möglichen therapeutischen Konsequenz sollte beim serösen Endometriumkarzinom eine Bestimmung des HER2-Status erfolgen.8
Abkürzungen
CN: Kopienzahl; dMMR: defiziente Mismatch-Reparatur; DNA: Desoxyribonukleinsäure; EC: Endometriumkarzinom; ER: Östrogenrezeptor; ESMO: European Society for Medical Oncology; G1-2: Grading Stufen 1 bis 2 (low grade); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HRD: homologe Rekombinationsdefizienz; IHC: Immunhistochemie; L1CAM: L1-Zelladhäsionsmolekül; MLH1: MutL Homolog 1; MMR: DNA-Mismatch-Reparatur; MSH2: Mutator S Homolog 2; MSH6: Mutator S Homolog 6; MSI: Mikrosatelliteninstabilität; MSS: Mikrosatellitenstabilität; NGS: Next-Generation-Sequencing; NSMP: Tumor ohne spezifisches molekulares Profil; p53abn: p53-aberrant; PCR: Polymerase-Kettenreaktion; pMMR: profiziente Mismatch-Reparatur; PMS2: Postmeiotic Segregation Increased 2; POLE: DNA-Polymerase Epsilon; POLEm: POLE-mutiert; POLEwt: POLE-Wildtyp; TCGA: The Cancer Genome Atlas Program
- Makker V, et al. Nat Rev Dis Primers 2021;7(1):88.
- Xu WH, et al. Int J Cancer 2004;108(4):613–9.
- Bonneville R, et al. JCO Precis Oncol 2017;1:PO.17.00073.
- Heeke AL, et al. JCO Precis Oncol 2018;2018:PO.17.00286.
- Corr B, et al. BMJ Med 2022;1(1):e000152.
- Luchini C, et al. Ann Oncol 2019;30(8):1232–43.
- Stelloo E, et al. Ann Oncol 2017;28(1):96–102.
- S3-Leitlinie Endometriumkarzinom. Version 3.0, Juni 2024. Verfügbar unter register.awmf.org/de/leitlinien/detail/032-034OL. Letzter Zugriff: Dezember 2025.
- ESGO–ESTRO–ESP guidelines for the management of patients with endometrial carcinoma: update 2025. Concin N, et al. Lancet Oncol 2025;26(8):e423-e435.
- Kandoth C, et al. Nature 2013;497(7447):67–73.
- Koskas M, et al. Int J Gynaecol Obstet 2021;155 Suppl 1(Suppl 1):45–60.
- Morice P, et al. Lancet 2016;387(10023):1094–108.
- Oaknin A, et al. Ann Oncol 2022;33(9):860–77.
- Santoro A, et al. Cancers (Basel) 2021;13(11):2623.

