BRCA1/2- und HRD-Diagnostik allgemein
Die Testung auf homologe Rekombinationsdefizienz (HRD) und Mutationen in den Genen Breast Cancer Associated 1 (BRCA1) und Breast Cancer Associated 2 (BRCA2) gewinnt zunehmend an klinischer Bedeutung. Die Gründe dafür sind vielfältig:
Prognostische Informationen
Einige BRCA1/2-mutierte Tumoren sprechen im Vergleich zu Tumoren ohne entsprechende Mutation besser auf bestimmte Chemotherapeutika an.1,2
Therapeutische Relevanz
Bei bestimmten Formen von Brust-, Ovarial-, Pankreas- oder Prostatakarzinomen kann der Nachweis einer BRCA1/2-Mutation bzw. einer HRD den Einsatz einer zielgerichteten Therapie ermöglichen – abhängig von Zulassung und individueller Situation.3-6
Konsequenzen für Familienangehörige
Wird eine BRCA1/2-Keimbahnmutation festgestellt, kann auch für Verwandte eine genetische Testung sinnvoll sein, um das Krebsrisiko frühzeitig zu identifizieren.3,6
Prävention und Früherkennung
Personen mit nachgewiesener Keimbahnmutation sollten ein intensiviertes Früherkennungsprogramm erhalten, um maligne Veränderungen rechtzeitig zu erkennen. In Einzelfällen kann auch eine prophylaktische Entfernung gefährdeter Organe erwogen werden.6
Im Überblick: Ansätze zum Nachweis von BRCA1/2- und HRD-Mutationen
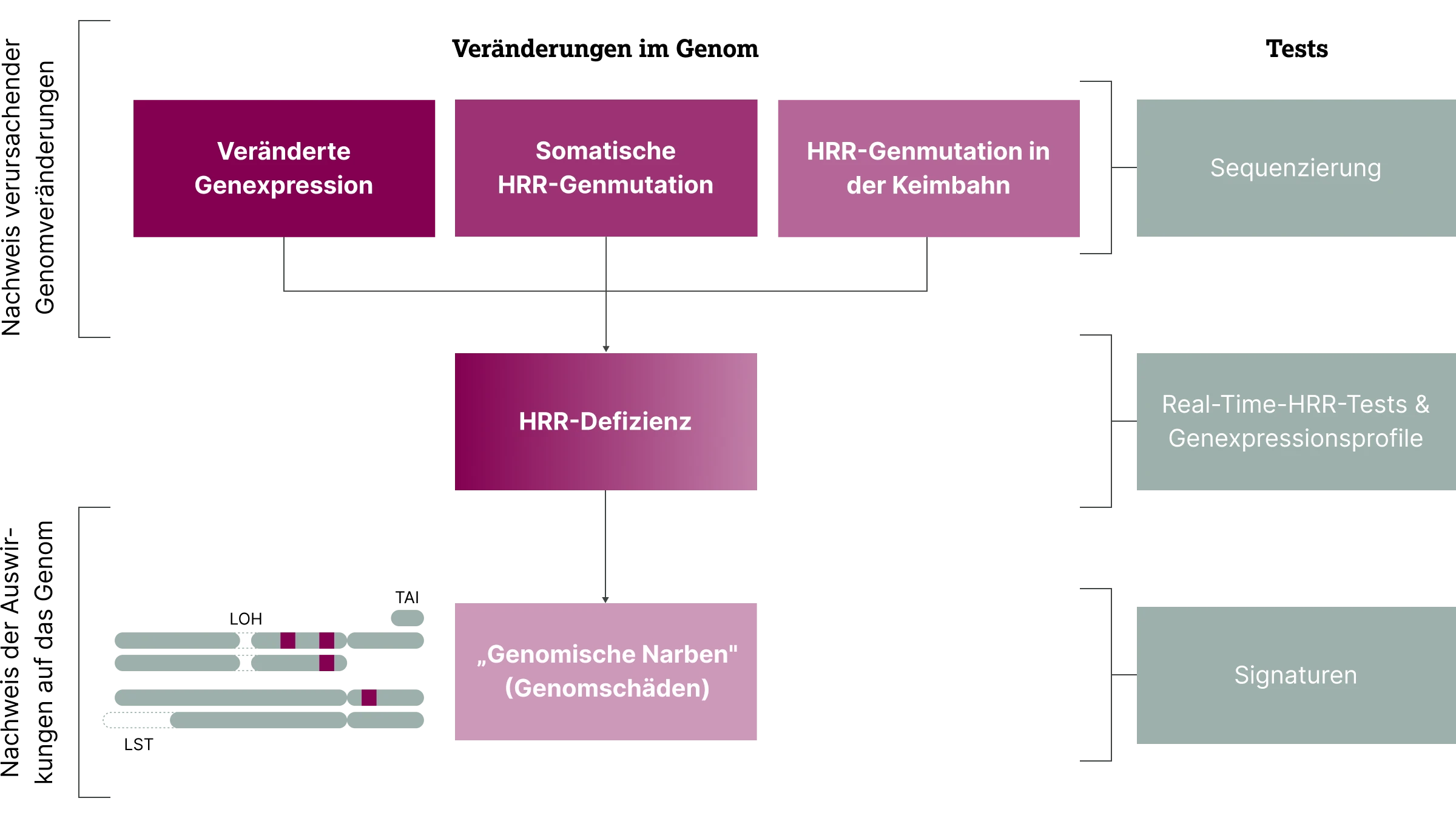
Es gibt verschiedene Ansatzpunkte, um Defekte der homologen Rekombinationsreparatur (HRR) nachzuweisen. Neben Mutationen und Expressionsveränderungen in HRR-assoziierten Genen wie BRCA1/2 zeigt sich eine HRD funktionell durch genomische Instabilität (GI). Diese lässt sich quantitativ mithilfe etablierter HRD-Scores messen, die drei Arten von „genomischen Narben“ erfassen: Verlust der Heterozygotie (LOH), telomerisches allelisches Ungleichgewicht (TAI) und Large ‑Scale State Transitions (LST).3.7
Für die therapeutisch relevante Diagnostik wird die HRD-Analyse in der Regel am Tumorgewebe durchgeführt, um charakteristische Muster der GI anhand von HRD-Scores nachzuweisen. Der BRCA1/2-Mutationsstatus wird hingegen – je nach Tumorentität und Zulassungskriterien – am Tumorgewebe und/oder im Blut bestimmt.3-6 Ein Nachweis von BRCA1/2 am Tumorgewebe (tBRCA1/2) allein erlaubt keine sichere Unterscheidung zwischen somatischer (sBRCA1/2) und hereditärer Mutation (gBRCA1/2). Zur Abklärung eines möglichen erblichen Risikos ist daher immer eine zusätzliche Keimbahntestung erforderlich.
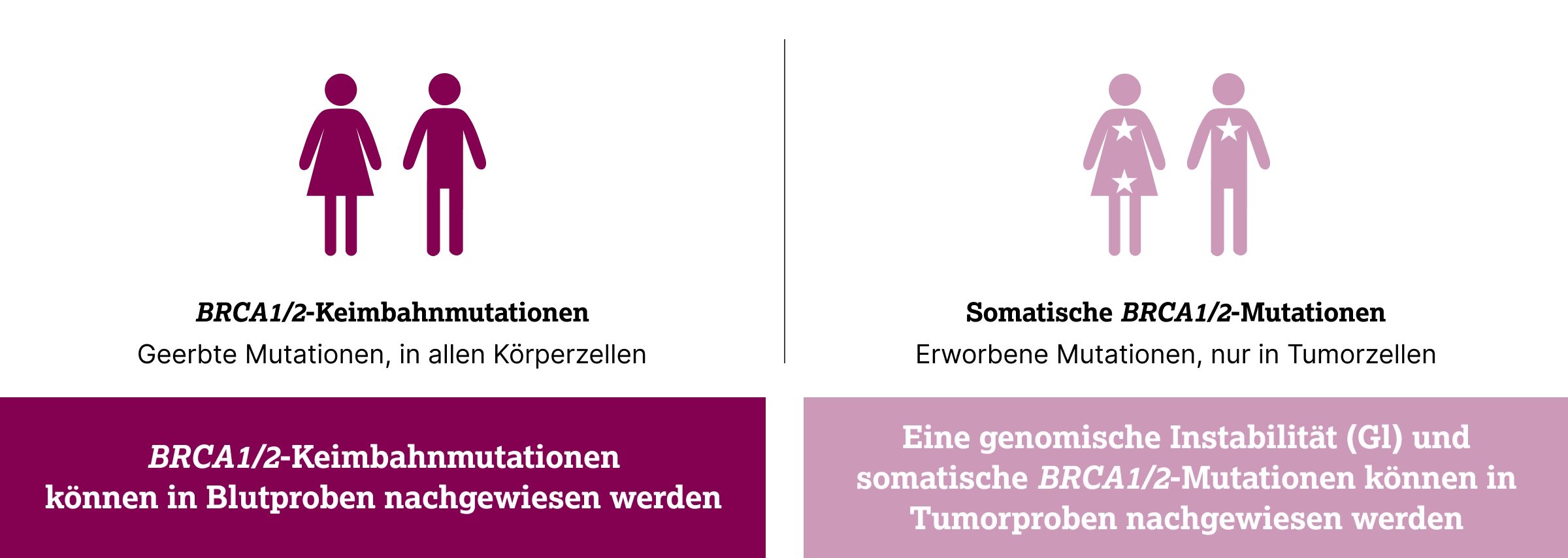
Definitionen: tBRCA1/2, sBRCA1/2 und gBRCA1/2
tBRCA1/2: Eine pathogene BRCA1- oder BRCA2-Mutation, die durch die Sequenzierung der DNA aus Tumorgewebe nachgewiesen wird. Es bleibt zunächst offen, ob diese Mutation somatisch (tumorspezifisch) oder ererbt (Keimbahn) ist.
sBRCA1/2: Eine somatische BRCA1/2-Mutation liegt vor, wenn diese ausschließlich im Tumorgewebe vorhanden und nicht in Normalgewebe (z. B. Blut, Sputum) feststellbar ist.
gBRCA1/2: Eine BRCA1/2-Mutation in der Keimbahn liegt vor, wenn diese im Normalgewebe (z. B. Blut, Sputum) gefunden wird, d. h. sie ist ererbt und betrifft alle Zellen des Körpers.

Informationen zum Biomarker HRD.
Optimaler Zeitpunkt für die BRCA1/2- bzw. HRD-Diagnostik
Für eine individualisierte Therapieplanung und die gezielte Abklärung familiärer Risiken für Brust-, Ovarial-, Pankreas- und Prostatakrebs ist die frühzeitige Bestimmung des BRCA1/2- und HRD-Status entscheidend. Die zeitnahe Testung ermöglicht die Auswahl geeigneter Therapieoptionen wie den Einsatz von Poly(ADP-ribose)-‑Polymerase (PARP)-Inhibitoren sowie eine gezielte genetische Beratung.8,9 Nationale und internationale Leitlinien empfehlen daher, die molekulargenetische Diagnostik möglichst bereits bei Diagnosestellung oder spätestens vor Einleitung einer medikamentösen Therapie durchzuführen.3-6,10,11
Die BRCA1/2-Diagnostik am Tumorgewebe unterliegt nicht dem Gendiagnostikgesetz (GenDG)12,13 und kann somit ohne Verzögerung erfolgen, sobald die betroffene Person eingewilligt hat. Wird eine Mutation im Tumorgewebe nachgewiesen, kann eine zusätzliche Keimbahntestung zur Abklärung eines erblichen Risikos erforderlich sein – hierfür gelten die Vorgaben des GenDG, inklusive genetischer Beratung.13

Informationen zum Gendiagnostikgesetz.
Diagnostisches vs. prädiktives Vorgehen bei der BRCA1/2-Testung
Die genetische Testung auf BRCA1/2-Mutationen kann zwei unterschiedliche Zielsetzungen verfolgen: Zum einen dient sie bei bereits erkrankten Personen der Therapieplanung (diagnostisches Vorgehen), zum anderen kann sie zur Einschätzung eines erblichen Krebsrisikos bei gesunden, aber familiär vorbelasteten Personen herangezogen werden (prädiktives Vorgehen). Je nach Zielstellung unterscheiden sich die rechtlichen Rahmenbedingungen, die zuständigen Einrichtungen und die Art der Probenentnahme.
Erfolgt die BRCA1/2-Analyse bei Personen mit nachgewiesener Krebserkrankung im Rahmen der Therapieplanung am Tumorgewebe, fällt diese Untersuchung nicht unter das GenDG. Sie wird üblicherweise in einem molekularpathologischen Labor durchgeführt und kann nach ärztlicher Aufklärung und Einwilligung der betroffenen Person veranlasst werden.12,13 Bei einem positiven Befund im Tumorgewebe sollte je nach Indikation und Zulassungskriterien eine ergänzende Keimbahntestung zur Abklärung des erblichen Risikos erfolgen.
Sofern eine Therapie nur bei Vorliegen einer BRCA1/2-Keimbahnmutation zugelassen ist, sollte die Testung anhand einer Blutprobe erfolgen. Diese Untersuchung unterliegt den Anforderungen des GenDG und muss in qualifizierten Zentren für Humangenetik oder in Einrichtungen des Deutschen Konsortiums Familiärer Brust- und Eierstockkrebs durchgeführt werden. Die betroffene Person muss vor der genetischen Analyse umfassend aufgeklärt werden und schriftlich einwilligen. Die genetische Beratung ist nach Abschluss der Untersuchung und im Fall des Nachweises einer pathogenen Variante verpflichtend anzubieten.
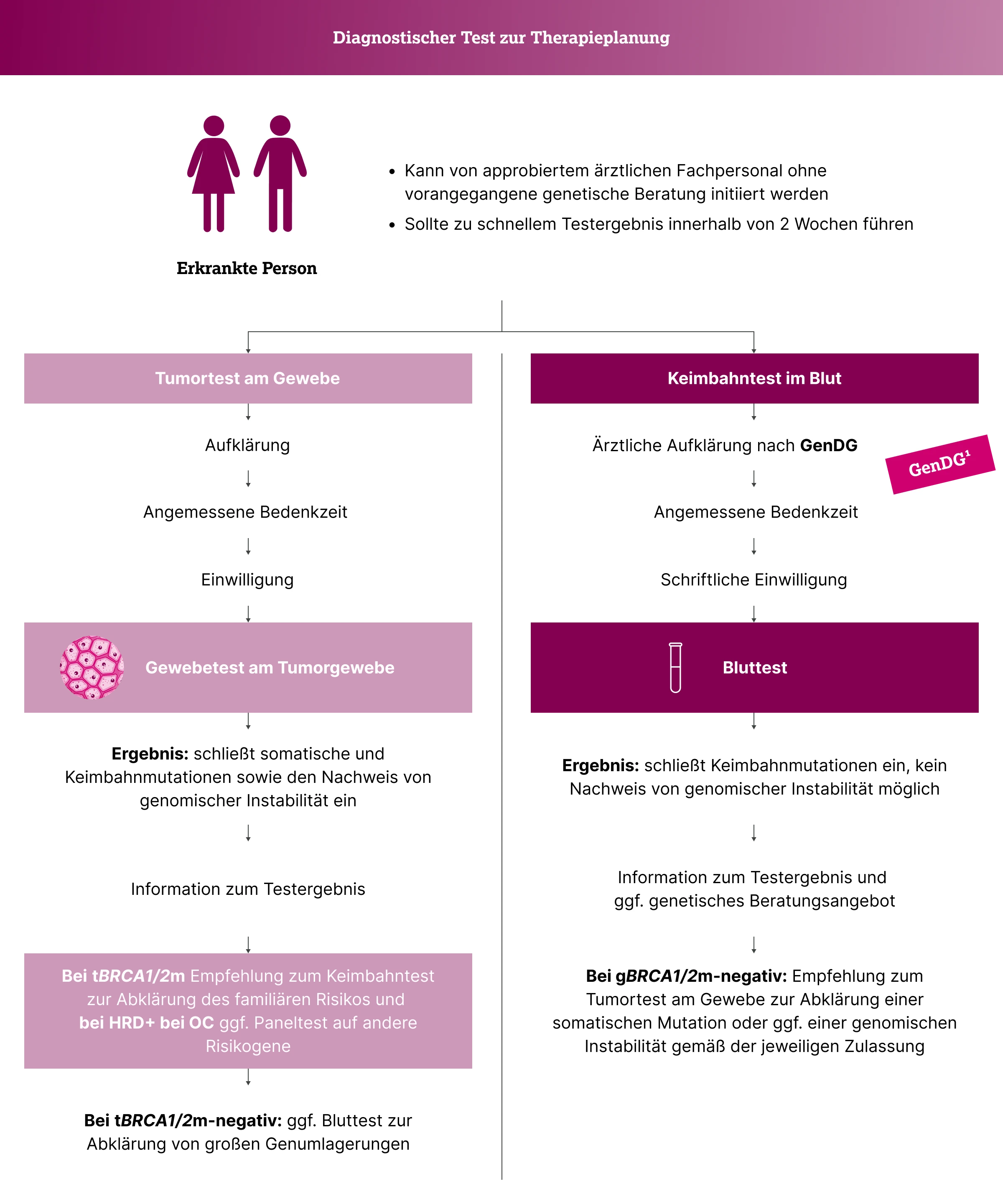
Wird der BRCA1/2-Test zur Therapieentscheidung durchgeführt, ist eine zügige Ergebnisübermittlung entscheidend für die Wahl der weiteren Therapiestrategie. Daher sollten für Patient:innen mit Ovarial-, Mamma-, Pankreas- oder Prostatakarzinom Fast-Track-Prozesse genutzt werden, sodass das Testergebnis zeitnah verfügbar ist.
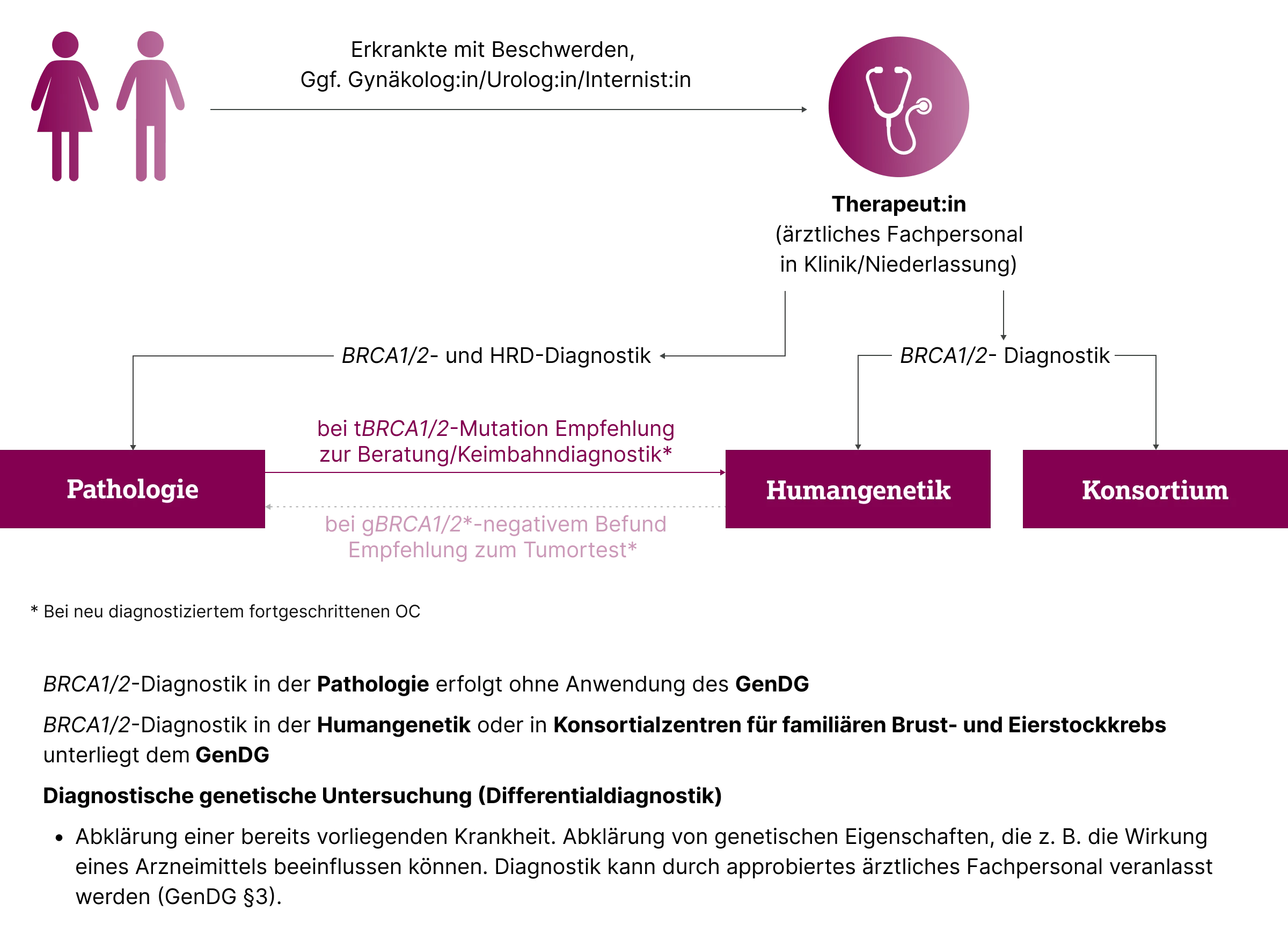
Besteht das Ziel der genetischen Diagnostik in der Einschätzung eines erblichen Krebsrisikos, etwa bei auffälliger Familienanamnese, erfolgt die genetische Beratung bzw. Testung immer über spezialisierte Einrichtungen wie das Deutsche Konsortium Familiärer Brust- und Eierstockkrebs, Fachärzt:innen für Humangenetik oder entsprechend qualifizierte humangenetische Labore. Bei vorliegender familiärer Risikokonstellation haben Betroffene Anspruch auf diese Untersuchung bzw. eine genetische Beratung.12,14 Bei einer prädiktiven genetischen Analyse erfolgt die Testung auf Keimbahnmutationen anhand einer Blutprobe. Gemäß GenDG ist die betroffene Person vor Durchführung eines solchen Tests sowie nach Vorliegen des Ergebnisses zwingend zu beraten.12,13


Informationen zur Qualitätssicherung in pathologischen Laboren.
Methoden zum Nachweis von BRCA1/2- und HRD-Mutationen
Nachweis von Genomschäden als Folge der HRD
Zellen mit einer HRD weisen charakteristische genomische Schäden auf – darunter Deletionen, Instabilitäten und chromosomale Strukturveränderungen. Diese entstehen etwa, weil bei defekter homologer Rekombination fehleranfällige Reparaturmechanismen wie die nicht-homologe Endverknüpfung (NHEJ) einspringen müssen.15
Im Gegensatz zum direkten Nachweis von Mutationen in HRR‑Genen wie BRCA1/2, der nicht zwangsläufig das Vorliegen eines HRD-Phänotyps belegt, erfassen HRD‑Tests die genomischen Folgen einer HRD („genomische Narben“) und ermöglichen so eine quantitative Bewertung der genomischen Instabilität.16 Hierzu werden drei komplementäre HRD-Scores herangezogen, die unterschiedliche Muster dieser „genomischen Narben“ abbilden: LOH, TAI und LST.15

Alle drei HRD-Scores zeigen eine nachgewiesene Korrelation mit Defekten in BRCA1/2 oder anderen HRR-Genen in Mamma- und Ovarialkarzinomen. Die kombinierte Analyse dieser Parameter verbessert die Unterscheidung zwischen HRD-positiven und -negativen Tumoren deutlich.17-19
Bestimmung des HRD-Status (bei Patientinnen mit Ovarialkarzinom)
Für die HRD-Diagnostik beim Ovarialkarzinom kommt in klinischen Studien und in der Routine derzeit überwiegend der myChoice® HRD-Test (Myriad Genetics) zum Einsatz. Dieser Assay kombiniert die Analyse genomischer Instabilitätsmuster (LOH, LST, TAI) mit einer Untersuchung des BRCA1/2-Mutationsstatus (Keimbahn oder somatisch).20
Es existieren bereits folgende Alternativen für die HRD-Diagnostik:
Single Nucleotide Polymorphisms (SNPs) gehören zu den häufigsten genetischen Veränderungen der DNA. Mittels SNP-‑Arrays lassen sich sowohl Kopienzahlveränderungen als auch kopienzahlneutrale Strukturveränderung wie LOH nachweisen.21,22 Die Detektionsdichte richtet sich nach der Anzahl der analysierten SNPs. Beispiele für SNP-Arrays sind der OncoScan FFPE Array (Affymetrix) oder der Infinium Cyto SNP Bead Chip (Illumina).23,24 Die Abdeckung und die erfassten Genombereiche variieren je nach Assay. Für die Analyse von BRCA1/2-Mutationen sind SNP-Arrays aufgrund der Größe der Gene und der erforderlichen Probenmenge jedoch nicht praktikabel.
Beim Shallow Whole Genome Sequencing (WGS), auch Low-Pass WGS oder Low-Coverage WGS genannt, wird das gesamte Genom mit einer geringen Sequenziertiefe von typischerweise 0,1–3x (statt 10–30x oder mehr) erfasst.25 Diese Methode ermöglicht eine kostengünstige, genomweite Detektion größerer Strukturveränderungen und eignet sich zur Berechnung von HRD-‑Scores. Für die Auswertung kombinierter GI-‑Scores sind spezielle bioinformatische Algorithmen erforderlich. Der Nachweis einzelner Mutationen, etwa in BRCA1/2, ist aufgrund der niedrigen Sequenziertiefe mit Shallow WGS nicht zuverlässig möglich und erfordert zusätzliche Analysen.26
Eine weitere Option ist die Panelsequenzierung mittels Next ‑Generation ‑Sequencing (NGS). Hierbei werden gezielt ausgewählte Genabschnitte analysiert, um Informationen zu SNPs, strukturellen Veränderungen und Mutationen in HRR-‑Genen, einschließlich BRCA1/2, zu gewinnen. Für die HRD-Testung stehen inzwischen kommerziell erhältliche Panels zur Verfügung. Diese müssen bioinformatisch angepasst und validiert werden, um eine zuverlässige Bestimmung des HRD-‑Status zu gewährleisten. Beispiele sind das AmoyDx® HRD Focus Panel (Amoy Diagnostics) und das Oncomine™ Comprehensive Assay Plus (Thermo Fisher). Beide kombinieren die Detektion von BRCA1/2-Mutationen mit einem genomischen Score, etwa einem LOH- oder Genomic Scar ‑Score.27,28
Nachweis von Mutationen in BRCA1/2 und anderen HRR-Genen
Mutationen in BRCA1/2 und weiteren Genen der HRR lassen sich zuverlässig mittels NGS nachweisen. Diese Gene sind mit etablierten NGS-Panels abgedeckt, die sowohl für die molekulare Tumorcharakterisierung als auch zur Risikoabschätzung erblicher Erkrankungen eingesetzt werden.
Probenmaterial für die BRCA1/2-Diagnostik
Der BRCA1/2-Mutationsstatus kann anhand des Tumorgewebes oder einer Blutprobe (Keimbahnanalyse) bestimmt werden:29,30
Die Analyse anhand der Tumorprobe kann somatische oder Keimbahnvarianten von BRCA1/2 detektieren. Tumorproben werden in der Regel im Rahmen eines invasiven Eingriffs gewonnen und liegen meist als formalinfixiertes, paraffineingebettetes (FFPE) Material oder schockgefrorenes Gewebe vor. Die Durchführbarkeit von BRCA1/2-Analysen an extrahierter DNA aus FFPE-Proben von Ovarial- und Mammakarzinomen ist etabliert, erfordert jedoch eine stringente Qualitätssicherung.29
Keimbahnmutationen werden üblicherweise anhand von Blutproben nachgewiesen (z. B. 10 ml in EDTA-Antikoagulans). Transport und Lagerung erfolgen gemäß den laborspezifischen SOPs.30
BRCA1/2-Keimbahn- und Tumortest: Warum sind beide Verfahren sinnvoll?
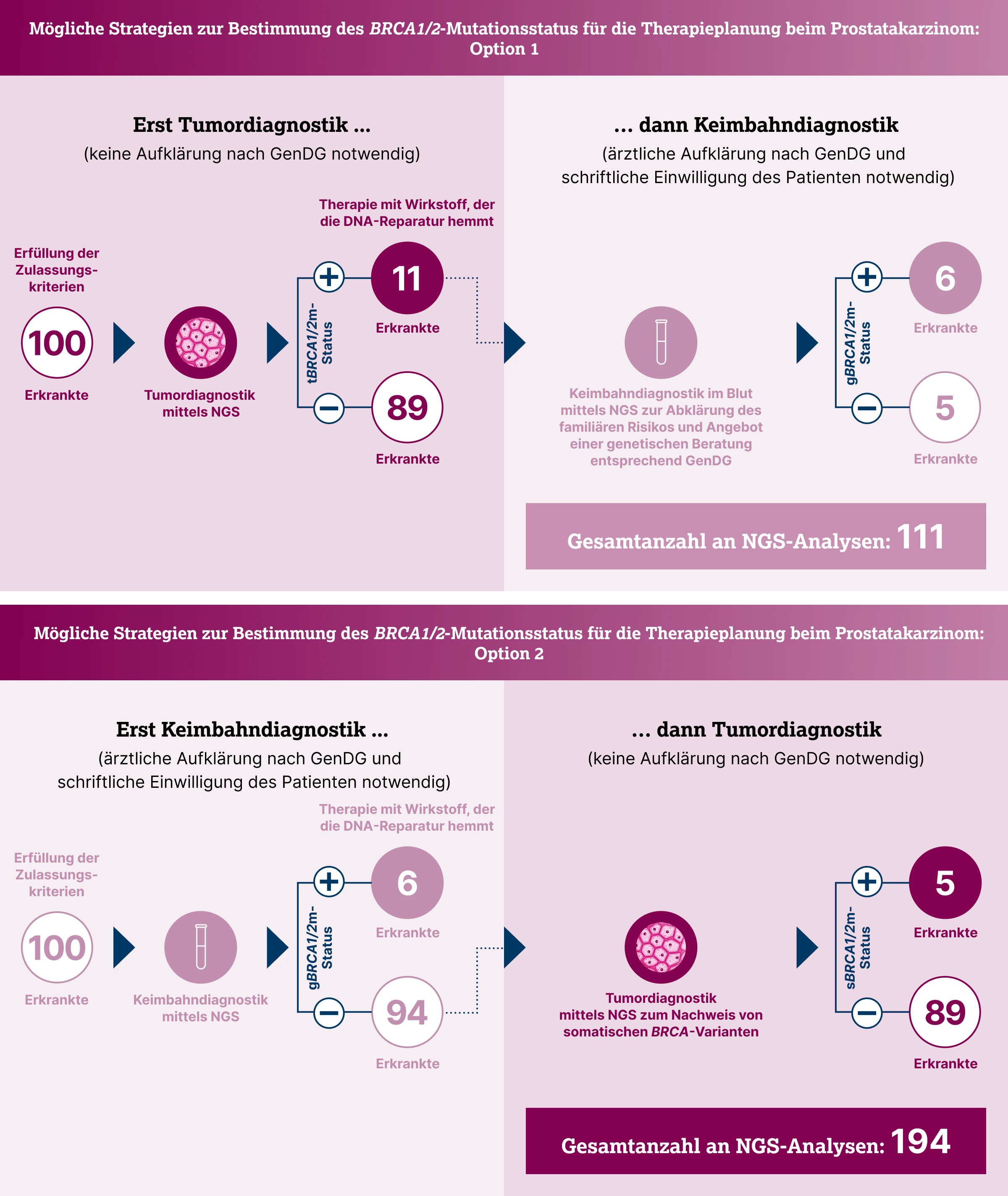
Beide Testverfahren bieten jeweils Vor- und Nachteile, sollten aber als komplementäre Verfahren gesehen werden. Der Keimbahntest anhand einer Blutprobe erfasst alle erblichen pathogenen BRCA1/2-Varianten, übersieht jedoch rein somatische Mutationen, die für die Therapiewahl relevant sein könnten. Der Test anhand des Tumorgewebes kann sowohl somatische als auch Keimbahnvarianten nachweisen, erlaubt aber ohne zusätzliche Analyse keine sichere Unterscheidung zwischen den beiden. Für eine optimale Therapieplanung und Abklärung familiärer Risiken ist daher oft eine Kombination beider Tests erforderlich. Dies setzt eine enge Zusammenarbeit zwischen Pathologie und Humangenetik bzw. spezialisierten Konsortialzentren Familiärer Brust- und Eierstockkrebs voraus.31,32
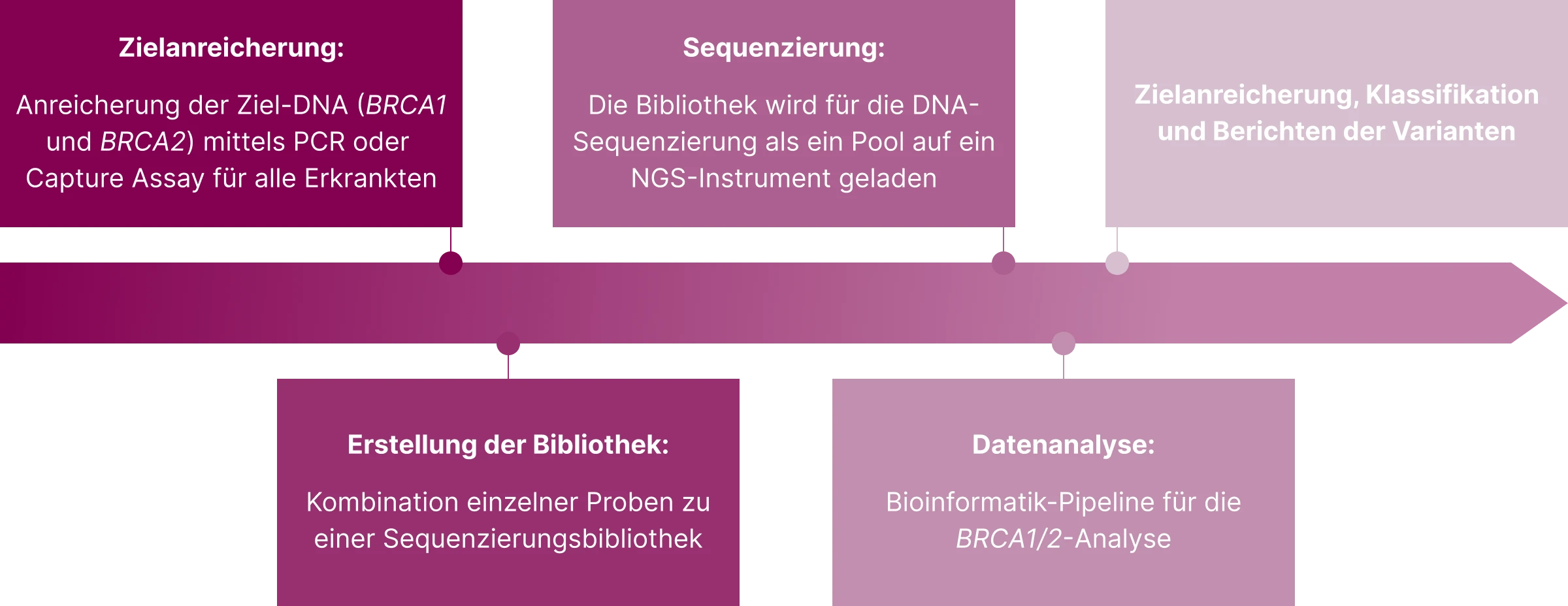
Ablauf der Genanalyse mittels NGS
Die NGS-Analyse ermöglicht eine Hochdurchsatz-‑Sequenzierung aller relevanten HRR-‑Genvarianten und erfordert DNA von ausreichend hoher Qualität. Bei Verwendung von FFPE-Gewebeproben ist eine schonende Fixierung in gepuffertem Formalin und eine kontrollierte Fixierdauer entscheidend. Bei niedriger Tumorzellfraktion kann eine Makro- oder Mikrodissektion zur Anreicherung des Tumormaterials erforderlich sein.35
Bei der BRCA1/2-Diagnostik ist es entscheidend, dass neben Single-Nukleotid-Varianten (SNVs) und Insertionen/Deletionen auch große genomische Umlagerungen zuverlässig erfasst werden. Ist dies mit der eingesetzten NGS-Technologie nicht gewährleistet, sollte eine ergänzende PCR-‑basierte Methode wie die Multiplex Ligation-dependent Probe Amplification (MLPA) angewendet werden.35 Mutationen in nicht‑kodierenden Genomregionen (z. B. intronische Spleißstellen, Promotoren, Enhancer) werden in der Routinediagnostik derzeit meist nicht systematisch erfasst, könnten jedoch für einen Teil bislang ungeklärter familiärer Fälle ursächlich sein.
Neu detektierte BRCA1/2-Varianten sind nach aktuellen Klassifikationsstandards (z. B. ACMG/AMP) einzuordnen, um pathogene, wahrscheinlich pathogene und nicht pathogene Varianten differenzieren zu können.36,37 Bei unklaren oder komplexen Befunden kann eine Validierung beispielsweise mittels Sanger-Sequenzierung sinnvoll sein.35
Alle Arbeitsschritte der NGS-Diagnostik müssen nach validierten Methoden unter strikter Qualitätskontrolle erfolgen. Dazu gehören:35
- DNA-Extraktion, DNA-Prozessierung und Library-Präparation
- Generierung von Sequenzier-Reads
- Base-Calling und Sequenz-Mapping
- Annotation, Filterung, Klassifizierung und Interpretation der Varianten
Die Abdeckung der zu analysierenden DNA-Sequenz muss ausreichend sein, um einen technischen prädiktiven Wert von 99,9 % zu erreichen. Für Keimbahnvarianten sollte eine 30-‑fache Abdeckung angestrebt werden. Bei niedriger Allelfrequenz, beispielsweise von somatischen Mutationen im Tumorgewebe, kann eine wesentlich höhere Sequenziertiefe (ca. 1.000-fach) erforderlich sein, um auch niedrigfrequente Varianten detektieren zu können.35
Die Analyse komplexer, GC-reicher DNA-Bereiche gelingt mit hochqualitativer DNA aus Frischmaterial wie Blut in der Regel zuverlässiger als aus FFPE-Gewebe. Hier sollten optimierte Anreicherungs- und Sequenzierstrategien eingesetzt werden, um Artefakte durch DNA-Fragmentierung oder chemische Modifikationen zu minimieren.35
Interpretation der BRCA1/2- und HRD-Testergebnisse
BRCA1/2-Testergebnisse und Interpretation
Da Mutationen in unterschiedlichen Abschnitten von BRCA1 und BRCA2 vorkommen können, müssen beide Gene für die Diagnostik vollständig analysiert werden. Dies umfasst alle kodierenden Exons mit angrenzenden intronischen Spleißstellen sowie SNVs und große genomische Umlagerungen.38 Eine Beschränkung auf bekannte Hot-Spot-Mutationen ist diagnostisch unzureichend.
Die Interpretation erfolgt in der Regel nach den internationalen ACMG/AMP-‑Kriterien unter Berücksichtigung der ClinGen ENIGMA-Spezifikationen für BRCA1/2.37 Hierbei fließen neben Datenbank- und Literaturquellen auch populationsgenetische, segregationsanalytische, prädiktive und funktionelle Daten ein.37 Zur standardisierten Bewertung der klinischen Signifikanz wird häufig die 5-Klassen-Einteilung verwendet:36

Ein kleiner, aber relevanter Anteil der Befunde (bei BRCA1/2 typischerweise 5–6 %) fällt trotz umfassender Analyse in die Kategorie 3 und wird als „Variante unklarer Signifikanz“ (Variant of Uncertain Significance, VUS) eingeordnet. Diese Varianten haben zunächst keine unmittelbare klinische Konsequenz, sollten jedoch regelmäßig im Hinblick auf neue wissenschaftliche Erkenntnisse überprüft werden.6
Das molekulargenetische Gutachten
Das molekulargenetische Gutachten sollte die eingesetzte Methodik klar und reproduzierbar dokumentieren, einschließlich Sequenzierplattform, Anreicherungsverfahren und den erfassten Zielregionen. Dies gilt für die Analyse von BRCA1/2 ebenso wie für andere HRR-Gene im Rahmen humangenetischer Untersuchungen. Der Laborbericht muss mindestens folgende Angaben enthalten:35,39
- Bezeichnung des untersuchten Gens bzw. der untersuchten Gene
- Auflistung der identifizierten genetischen Varianten in einer anerkannten Nomenklatur
- Interpretation und Klassifikation der Varianten gemäß etablierten Standards (z. B. ACMG/AMP)
Für die Auswertung sollten validierte bioinformatische Abläufe sowie sorgfältig kuratierte Datenbanken genutzt werden. Berichtet werden sollten bevorzugt Varianten mit belegter oder wahrscheinlicher klinischer Relevanz. VUS sollten klar als solche gekennzeichnet und nicht für direkte Therapieentscheidungen herangezogen werden.
HRD-Testergebnisse und Interpretation

HRD-Tests analysieren sowohl die GI als auch den BRCA1/2-Mutationsstatus. Für die Beurteilung einer HRD wird ein zusammengesetzter genomischer Score bzw. Algorithmus verwendet. Ein Ergebnis wird als HRD-positiv eingestuft, wenn der jeweilige testspezifische HRD-Score den definierten Schwellenwert erreicht oder überschreitet und/oder eine pathogene bzw. wahrscheinlich pathogene BRCA1/2-Mutation (Klassifikation der Variante: Klasse 4 oder 5) nachgewiesen wird. Ein Ergebnis wird als HRD-negativ eingestuft, wenn der jeweilige HRD-Score unter dem festgelegten Schwellenwert liegt und keine pathogene bzw. wahrscheinlich pathogene BRCA1/2-Variante vorliegt.
Der konkrete Schwellenwert für den HRD-Score sowie die Zusammensetzung des Scores sind testspezifisch und müssen gemäß Validierung des jeweils eingesetzten Verfahrens angegeben werden. Der HRD-Score ergibt sich anhand genomischer Instabilitätsmetriken wie LOH (Loss of Heterozygosity), TAI (Telomeric Allelic Imbalance) und LST (Large-Scale State Transitions). Diese erfassen komplementäre Aspekte HRR-typischer Schäden. Je nach Anbieter werden diese Marker einzeln oder kombiniert zu einem Score aggregiert (wie z. B. beim etablierten Myriad myChoice® HRD-Test20), der zusammen mit dem BRCA1/2-Mutationsstatus die HRD-Einstufung unterstützt. Schwellenwerte, Berechnungsweise und Gewichtung der Metriken sind test- bzw. plattformspezifisch und müssen im jeweiligen Verfahren ausgewiesen werden.
Abkürzungen
ACMG: American College of Medical Genetics and Genomics; AMP: Association for Molecular Pathology; BRCA1: Breast Cancer Associated Gene 1; BRCA2: Breast Cancer Associated Gene 2; BRCA1/2m: BRCA1/2-‑mutiert; CNV: Kopienzahlvariante; DNA: Desoxyribonukleinsäure; EDTA: Ethylendiamintetraacetat; ENIGMA: Evidence-based Network for the Interpretation of Germline Mutant Alleles; FFPE: formalinfixiert, paraffineingebettet; gBRCA1/2: BRCA1/2-‑Keimbahnmutation; GC: Guanin-Cytosin; GenDG: Gendiagnostikgesetz; GI: genomische Instabilität; GIS: genomischer Instabilitätsscore; GSS: Genomic Scar Score; HR: Hazard Ratio; HRD: homologe Rekombinationsdefizienz; HRD+: homologe Rekombinationsdefizienz-positiv; HRR: homologe Rekombinationsreparatur; LOH: Verlust der Heterozygotie; LST: Large ‑Scale State Transitions; MB: Megabyte; MLPA: Multiplex Ligation-dependent Probe Amplification; NGS: Next-Generation-Sequencing; NHEJ: nichthomologe Endverknüpfung‑; NOGGO: Nord-Ostdeutsche Gesellschaft für Gynäkologische Onkologie; OC: Ovarialkarzinom; PARP: Poly(ADPRibose‑)-Polymerase; PCR: Polymerase-Kettenreaktion; PFS: progressionsfreies Überleben; sBRCA1/2: somatische BRCA1/2-Mutation; SNP: Single Nucleotide Polymorphism; SNV: Single-Nukleotid-Variante; SOP: Standard Operating Procedure; TAI: telomerisches allelisches Ungleichgewicht; tBRCA1/2: BRCA1/2-Mutation im Tumor; VUS: Variant of Uncertain Significance; WGS: Whole Genome Sequencing
- Kowalewski A, et al. J Cancer Res Clin Oncol 2018;144(8):1503–07.
- Wattenberg MM, et al. Br J Cancer 2020;122(3):333–39.
- S3-Leitlinie Diagnostik, Therapie und Nachsorge maligner Ovarialtumoren. Version 6.1, Januar 2026. Verfügbar unter https://register.awmf.org/assets/guidelines/032-035OLl_S3_Ovarialkarzinom_2024-10.pdf. Letzter Zugriff: März 2026.
- S3-Leitlinie Prostatakarzinom. Version 8.0, Juli 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/leitlinien/prostatakarzinom/. Letzter Zugriff: März 2026.
- S3-Leitlinie Exokrines Pankreaskarzinom. Version 3.1, September 2024. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Pankreaskarzinom/Version_3/LL_Pankreaskarzinom_Langversion_3.1.pdf. Letzter Zugriff: März 2026.
- S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 5.0, Dezember 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mammakarzinom_4_0/Version_5/LL_Mammakarzinom_Langversion_5.0.pdf. Letzter Zugriff März 2026.
- Hoppe MM, et al. J Natl Cancer Inst 2018;110(7):704-13.
- Ledermann JA, et al. Ann Oncol 2024;35(3):248–66.
- González-Martín A, et al. Ann Oncol 2023;34(10):833–48.
- NCCN Clinical Practice Guidelines in Oncology. Pancreatic Adenocarcinoma. Version 2.2025. Verfügbar unter https://www.nccn.org/login?ReturnURL=https://www.nccn.org/professionals/physician_gls/pdf/pancreatic.pdf. Letzter Zugriff: Oktober 2025.
- Fizazi K & Gillessen S. Annals of Oncology 2023;34(6):557-63.
- Bundesministerium für Gesundheit. Begriffe A–Z. Verfügbar unter https://www.bundesgesundheitsministerium.de/service/begriffe-von-a-z/g/gendiagnostikgesetz.html. Letzter Zugriff: März 2026.
- Gesetz über genetische Untersuchungen bei Menschen (Gendiagnostikgesetz – GenDG) vom 31. Juli 2009. Bundesgesetzblatt 50:2529–2538. Letzte Änderung: 04. Mai 2021. Verfügbar unter https://www.gesetze-im-internet.de/gendg/BJNR252900009.html. Letzter Zugriff: März 2026.
- Deutsches Konsortium Familiärer Brust- und Eierstockkrebs. Verfügbar unter https://www.konsortium-familiaerer-brustkrebs.de. Letzter Zugriff: März 2026.
- Lord CJ & Ashworth A. Nat Rev Cancer 2016;16(2):110–20.
- Watkins JA, et al. Breast Cancer Res 2014;16(3):211.
- Abkevich V, et al. Br J Cancer 2012;107(10):1776–82.
- Popova T, et al. Cancer Res 2012;72(21):5454–62.
- Birkbak NJ, et al. Cancer Discov 2012;2(4):366–75.
- Myriad Genetic Laboratories. myChoice® HRD Technical Information. Verfügbar unter https://s3.amazonaws.com/myriad-library/technical-specifications/myChoice-HRD-Tech-Specs.pdf. Letzter Zugriff: März 2026.
- LaFramboise T. Nucleic Acids Res 2009;37(13):4181–93.
- Telli ML, et al. Clin Cancer Res 2016;22(15):3764–73.
- https://www.thermofisher.com/order/catalog/product/902293.
- https://emea.illumina.com/products/by-type/clinical-research-products/infinium-cytosnp-850k.html.
- https://www.cancer.gov/about-nci/organization/ccg/blog/2019/low-coverage-seq.
- Eeckhoutte A, et al. Bioinformatics 2020;36(12):3888–89.
- https://www.amoydiagnostics.com/products/amoydx-hrd-focus-panel.
- https://www.thermofisher.com/de/de/home/clinical/preclinical-companion-diagnostic-development/oncomine-oncology/oncomine-cancer-research-panel-workflow/oncomine-comprehensive-assay-plus.html.
- S1-Leitlinie: Tumorgenetik – Diagnostik im Kontext maligner Erkrankungen. Version 1.0, Dezember 2021. Verfügbar unter https://register.awmf.org/de/leitlinien/detail/078-017. Letzter Zugriff: März 2026.
- Blum HE, Müller-Wieland D (Hrsg.). Klinische Pathophysiologie. 11. Auflage, Stuttgart: Georg Thieme Verlag; 2020. DOI: 10.1055/b-0041-180116.
- Hahnen E et al. Dtsch Arztebl 2016;113(45):A-2028/B-1700/C-1682.
- Loser H, et al. Pathologe 2017;38(2):117–26.
- Hussain M, et al. Clin Cancer Res 2022;28(8):1518-30.
- Lang SH, et al. Int J Oncol 2019;55(3):597–616.
- European Medicines Agency (EMA). Guideline on good pharmacogenomic practice - First version. September 2018. Verfügbar unter https://www.ema.europa.eu/en/good-pharmacogenomic-practice. Letzter Zugriff: März 2026.
- Plon SE, et al. Hum Mutat 2008;29(11):1282–91.
- Parsons MT, et al. Am J Hum Genet 2024;111(9):2044–58.
- Palma M, et al. Crit Rev Oncol Hematol 2006;57(1):1–23.
- den Dunnen JT, et al. Hum Mutat 2016;37(6):564–9.-30.




