PIK3CA/AKT1/PTEN beim Mammakarzinom
Bedeutung und Prävalenz von PIK3CA/AKT1/PTEN
Die PIK3CA/AKT1/PTEN-Diagnostik ist im HR-positiven, HER2-negativen Mammakarzinom von zentraler Bedeutung. Mutationen in diesen Genen können zu einer Hyperaktivierung des PI3K/AKT/PTEN-Signalwegs führen, der mit Resistenzen gegenüber endokrinen Therapien und beschleunigter Tumorprogression verbunden ist.1–3 Die molekulare Analyse dieser Alterationen kann Hinweise auf die Prognose liefern und ermöglicht prädiktive personalisierte Therapieentscheidungen.4–8
Die Gene PIK3CA, AKT1 und PTEN kodieren Schlüsselproteine des PI3K/AKT/PTEN-Signalwegs, der essenzielle zelluläre Prozesse wie Wachstum, Proliferation, Überleben und Stoffwechsel steuert.
Genetische Alterationen in diesem Signalweg gehören zu den häufigsten molekularen Veränderungen bei soliden Tumoren, insbesondere beim Mammakarzinom.1–3 Aktivierende Mutationen in PIK3CA und AKT1 sowie ein Funktionsverlust von PTEN führen zu einer konstitutiven Aktivierung des Signalwegs. Beim metastasierten Mammakarzinom lassen sich PIK3CA-Mutationen in etwa 40 % der Fälle nachweisen, PTEN-Alterationen in etwa 5 % und AKT1-Mutationen in bis zu 5 % der Fälle.9–11

Biomarker PIK3CA, AKT1 und PTEN
PI3K/AKT/PTEN- und der ER-Signalweg
Im HR-positiven, HER2-negativen Mammakarzinom können sich der PI3K/AKT/PTEN- und der Östrogenrezeptor-(ER)-Signalweg durch wechselseitige Interaktionen beeinflussen.
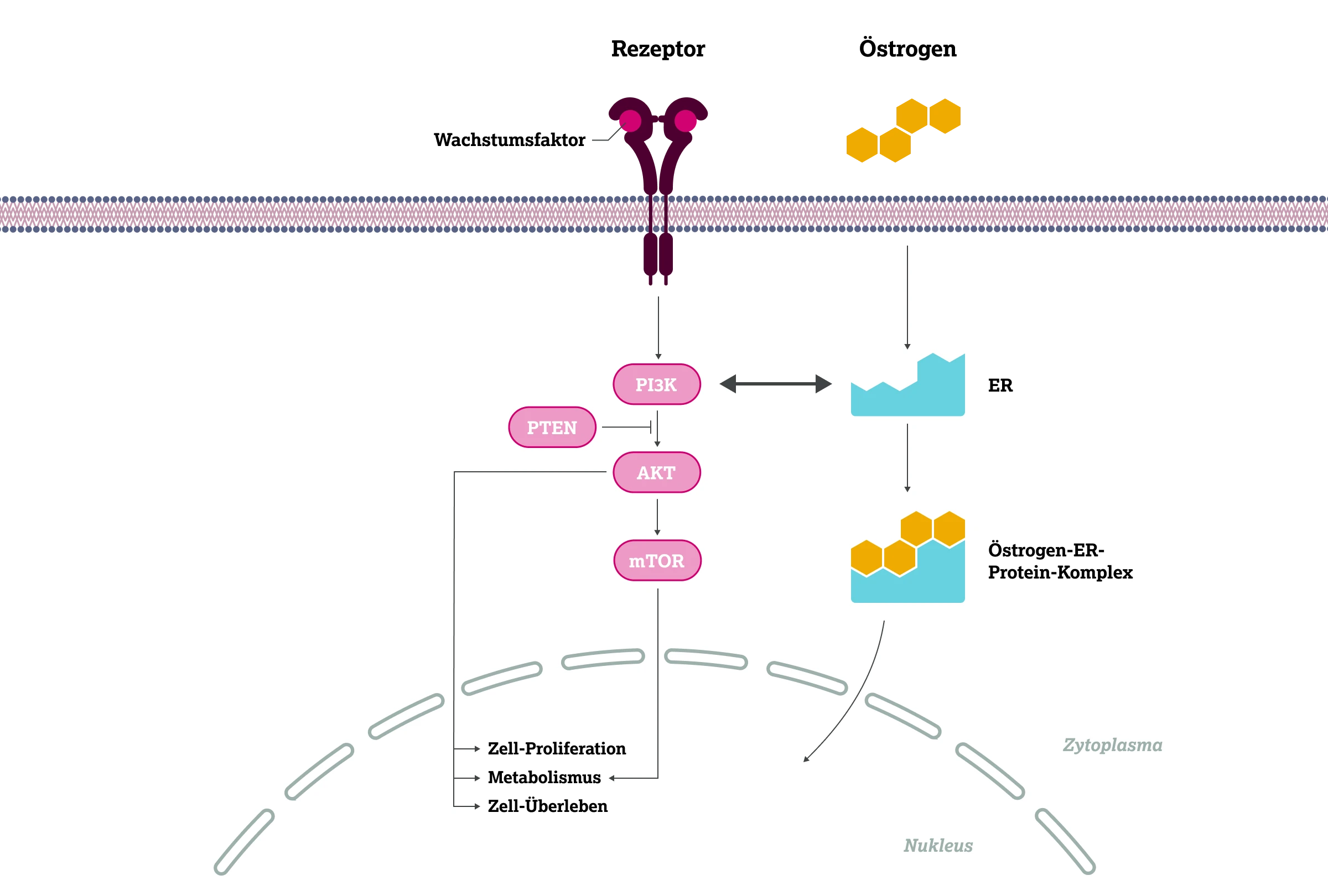
Der Östrogenrezeptor-(ER)-Signalweg ist von zentraler Bedeutung für die Entwicklung und Funktion der Brustdrüse. Unter physiologischen Bedingungen reguliert er essenzielle zelluläre Prozesse wie Proliferation, Zellteilung und Zellüberleben.13,14 Die Aktivierung erfolgt durch das Steroidhormon Östrogen, das über die Umwandlung von androgenen Vorläuferhormonen mittels Aromatase in Ovarien, Nebennieren, Fett- und Brustgewebe gebildet wird. Nach der Bindung von Östrogen an den ER (vor allem ERα, kodiert durch das ESR1-Gen) im Zytoplasma erfolgt die Translokation des Rezeptor-Hormon-Komplexes in den Zellkern, wo die Transkription proliferations- und wachstumsregulierender Zielgene initiiert wird.6,13
Neben seiner physiologischen Funktion spielt der ER-Signalweg eine zentrale Rolle in der Tumorgenese und Progression des Mammakarzinoms – insbesondere durch die Förderung maligner Zellproliferation. Die endokrine Therapie, die auf die Inhibition des ER-Signalwegs abzielt, stellt daher eine zentrale Behandlungsstrategie beim HR-positiven Mammakarzinom dar. Zu den therapeutischen Optionen zählen Aromataseinhibitoren, selektive Östrogenrezeptor-Modulatoren (SERMs) sowie selektive Östrogenrezeptor-Degrader (SERDs).12,13
Resistenzmechanismen und Interaktion mit dem PI3K/AKT/PTEN-Signalweg
- aktivierende (gain-of-function) Mutationen im ESR1-Gen,
- kompensatorische Aktivierung des PI3K/AKT/PTEN-Signalwegs, z. B. durch PIK3CA- und AKT1-Mutationen bzw. PTEN-Verlust.6,15
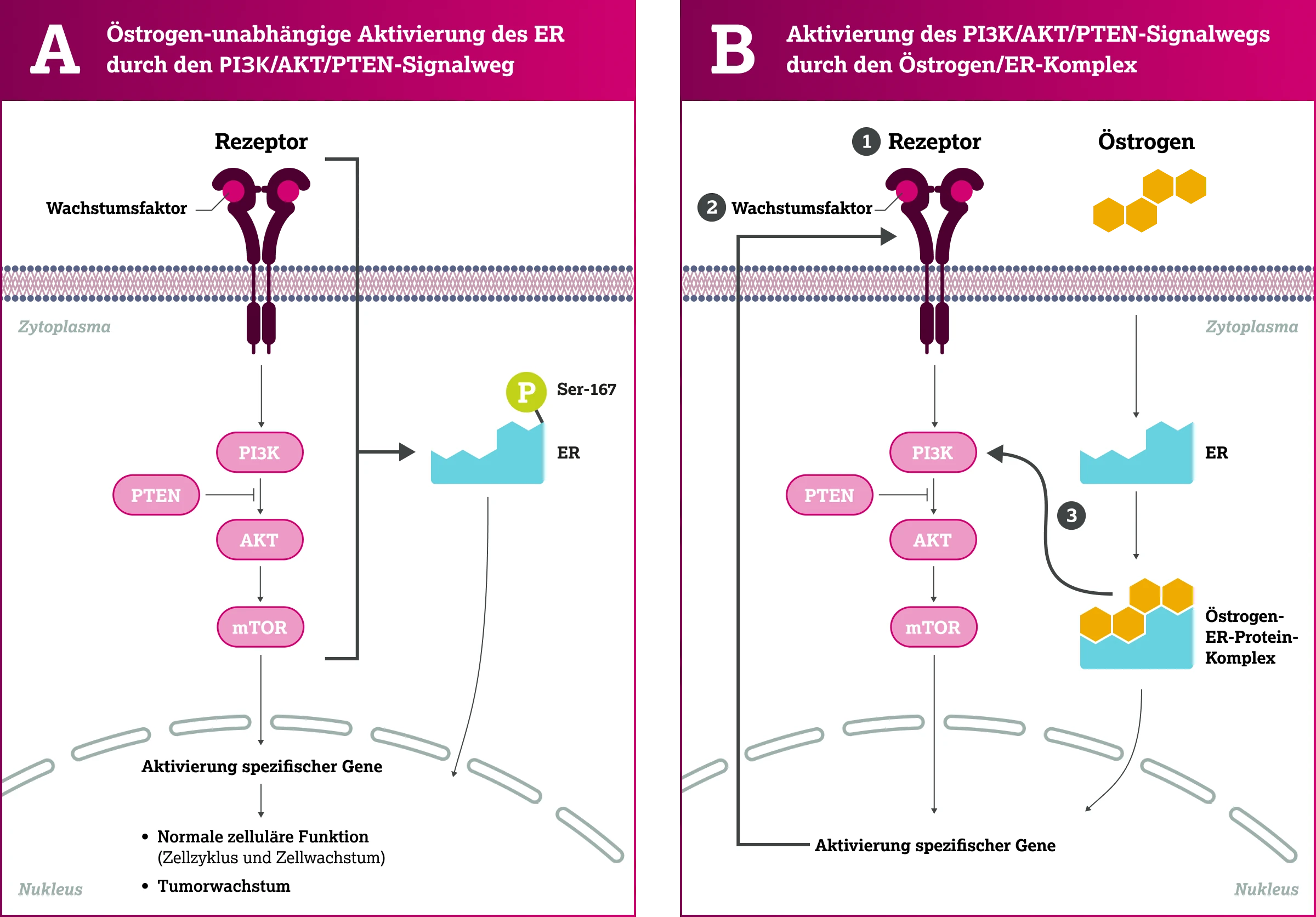
- AKT-vermittelte Phosphorylierung des ER an Serin-167 ermöglicht eine ligandenunabhängige Transkription von Zielgenen im Zellkern.6,12,16–18 (Abbildung A)
- indem er Zielgene transkribiert, die upstream-Komponenten des Signalwegs wie Zelloberflächenrezeptoren (1), deren Liganden (2) oder Adaptermoleküle kodieren, und
- indem er durch direkte Interaktion mit der regulatorischen PI3K-Untereinheit den Signalweg unmittelbar stimuliert (3).6,16,19,20 (Abbildung B)
Diese bidirektionalen Signalinteraktionen unterstreichen die Bedeutung des PI3K/AKT/PTEN-Signalwegs als therapeutisches Ziel bei HR-positiven Mammakarzinomen – insbesondere im Rahmen kombinierter Behandlungsstrategien.16
Studien- und Leitlinien-Empfehlungen zur PIK3CA/AKT1/PTEN-Testung beim Mammakarzinom
Bei Patient:innen mit HR-positivem, HER2-negativem, metastasiertem Brustkrebs ist die molekulargenetische Testung entscheidend für die Auswahl zielgerichteter Therapien.21
Die Arbeitsgemeinschaft Gynäkologische Onkologie e. V. (AGO) spricht sich in ihrer Empfehlung mit einem „+“ für die Durchführung dieser Testung aus. Die Testung auf den PI3KCA/AKT1/PTEN-Status sollte spätestens im Rahmen einer Krankheitsprogression oder eines Rezidivs nach endokriner Vortherapie durchgeführt werden. Ziel ist es, rechtzeitig eine fundierte, biomarkerbasierte Therapieentscheidung treffen zu können. Die Analyse kann sowohl am Primärtumor als auch an Metastasen erfolgen. Alternativ steht die Untersuchung zirkulierender Tumor-DNA im Blut (Liquid Biopsy) zur Verfügung.21
Die ESMO-Leitlinien empfehlen bei Patient:innen mit Krankheitsrückfall während oder innerhalb von zwölf Monaten nach Abschluss einer adjuvanten endokrinen Therapie die Bestimmung des somatischen PIK3CA-Mutationsstatus (ESCAT-Score: I-A).22 Für Patient:innen mit Progression nach einer Kombinationstherapie aus endokriner Behandlung und CDK4/6-Inhibitor ist eine erweiterte molekulargenetische Testung angeraten. Diese sollte die Gene PIK3CA (ESCAT-Score: I-A), AKT1 (ESCAT-Score: I/II), PTEN (ESCAT-Score: I/II) und ESR1 (ESCAT-Score: I-A) umfassen. Darüber hinaus wird empfohlen, den BRCA1/2-Mutationsstatus in der Keimbahn zu bestimmen (ESCAT-Score: I-A). Optional kann auch eine Testung auf Mutationen im PALB2-Gen erfolgen, das aktuell mit einem ESCAT-Score von II-B klassifiziert ist.23
Methoden, Probenquellen und klinische Empfehlungen von PIK3CA/AKT1/PTEN-Analysen
Für die Detektion von PIK3CA/AKT1/PTEN-Mutationen kommen sowohl PCR-basierte Einzelgenanalysen als auch moderne Next-Generation-Sequencing-(NGS)-Verfahren zum Einsatz. Letztere bieten den Vorteil einer höheren Sensitivität und ermöglichen die Identifikation auch seltener Mutationsereignisse. Die Probengewinnung kann aus formalinfixiertem, paraffineingebettetem (FFPE) Tumorgewebe oder über zirkulierende Tumor-DNA aus dem Plasma (Liquid Biopsy) erfolgen. Für eine PIK3CA/AKT1/PTEN-Testung ist eine Gewebeprobe die optimale Wahl, da im Vergleich zur Liquid Biopsy Alterationen in allen drei Genen mit höherer Prävalenz nachgewiesen werden können.23 Wichtig ist: Liegt ein negatives Ergebnis aus der Liquid Biopsy vor, sollte zur Sicherung der Aussagekraft eine ergänzende Testung am Tumorgewebe erfolgen.23,24
Abkürzungen:
AGO: Arbeitsgemeinschaft Gynäkologische Onkologie e. V.; AKT: AKT Serin/Threonin-Kinase (Protein); AKT1: AKT Serin/Threonin-Kinase 1 (Gen); ASCO: American Society of Clinical Oncology; CDK4/6: Cyclin-abhängige Kinasen 4 und 6; ER: Östrogenrezeptor; ESCAT: ESMO Scale for Clinical Actionability of Molecular Targets; ESMO: European Society for Medical Oncology; ESR1: Östrogenrezeptor-1 (Gen); FFPE: formalinfixiert, paraffineingebettet; FGFR: Fibroblasten-Wachstumsfaktor-Rezeptor; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HR: Hormonrezeptor; IGF1R: Insulin-like growth factor 1 receptor; mTOR: mechanistic target of rapamycin; NGS: Next-Generation-Sequencing; PCR: Polymerase-Kettenreaktion; PI3K: Phosphoinositid-3-Kinase (Protein); PIK3CA: Phosphoinositid-3-Kinase katalytische Untereinheit alpha (Gen); PTEN: Phosphatase- und Tensin- Homolog (Gen); PTEN: Phosphatase- und Tensin- Homolog (Protein); SERD: selektive Östrogenrezeptor-Degrader; SERM: selektiver Östrogenrezeptor-Modulator
- Liu L, et al. Cancers (Basel) 2024;17(1):16.
- Skolariki A, et al. Explor Target Antitumor Ther 2022;3(2):172–99.
- Fusco N, et al. Crit Rev Oncol Hematol 2025;207:104626.
- Miricescu D, et al. Int J Mol Sci 2020;22(1)173.
- Martorana F, et al. Front Pharmacol 2021;12:662232.
- Osborne CK, et al. Annu Rev Med 2011;62:233–47.
- Basu A, et al. Cancers (Basel) 2021;13(14):3445.
- Hinz N, et al. Cell Commun Signal 2019;17:154.
- Sabine VS, et al. J Clin Oncol 2014;32:2951–8.
- Cancer Genome Atlas Network. Nature 2012;490:61–70.
- Turner NC, et al. N Engl J Med 2023;388:2058–70.
- Alves CL, et al. Int J Mol Sci 2023;24:4522.
- Liang J, et al. Cell Cycle 2003;2:339–45.
- La Camera G, et al. Cancers (Basel) 2021;13:1160.
- Brufsky AM, et al. Oncologist 2018;23:528–39.
- Khatpe AS, et al. Cancers (Basel) 2021;13.
- Campbell RA, et al. J Biol Chem 2001;276:9817–24.
- Patel HK, et al. Pharmacol Ther 2018;186:1–24.
- Hanker AB, et al. Cancer Cell 2020;37:496–513.
- Burstein HJ. N Engl J Med 2020;383:2557–70.
- Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.V. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlungen 2025.1D. Therapiealgorithmen.
- ESMO Metastatic Breast Cancer Living Guideline, v1.2 April 2025; Verfügbar unter https://www.esmo.org/guidelines/living-guidelines/esmo-living-guideline-metastatic-breast-cancer. Letzter Zugriff Oktober 2025.
- Bhave MA, et al. Breast Cancer Res Treat 2024;207:599–609.
- Chaki M, et al. Breast Cancer Res 2025;27:122.



