Was ist KEAP1 und welche Funktion hat es?
Das Tumorsuppressor-Gen KEAP1 kodiert das Kelch-like ECH-associated protein 1 (KEAP1), welches mit dem Transkriptionsfaktor NRF2 (Nuclear factor erythroid 2-related factor 2) interagiert. NRF2 spielt eine zentrale Rolle bei der Reaktion von Zellen auf oxidativen Stress, indem es die Expression zahlreicher zytoprotektiver Gene reguliert.1 Der KEAP1/NRF2-Signalweg ist jedoch bei verschiedenen Krebsarten fehlreguliert, was das Überleben und die Metastasierung von Tumorzellen begünstigen kann.2
Eine der Hauptursachen für die pathologische Aktivierung von NRF2 in Tumorzellen sind somatische Mutationen im KEAP1-Gen auf Chromosom 19, die zu einem Funktionsverlust des KEAP1-Proteins führen.1,2 Der Verlust von KEAP1 kann zur Entstehung einer immunsuppressiven Tumormikroumgebung beitragen. Besonders ausgeprägt ist dieser Effekt in Tumoren mit gleichzeitigen KRAS‑Mutationen, in denen eine reduzierte Wirksamkeit von Immuntherapien beschrieben ist.3
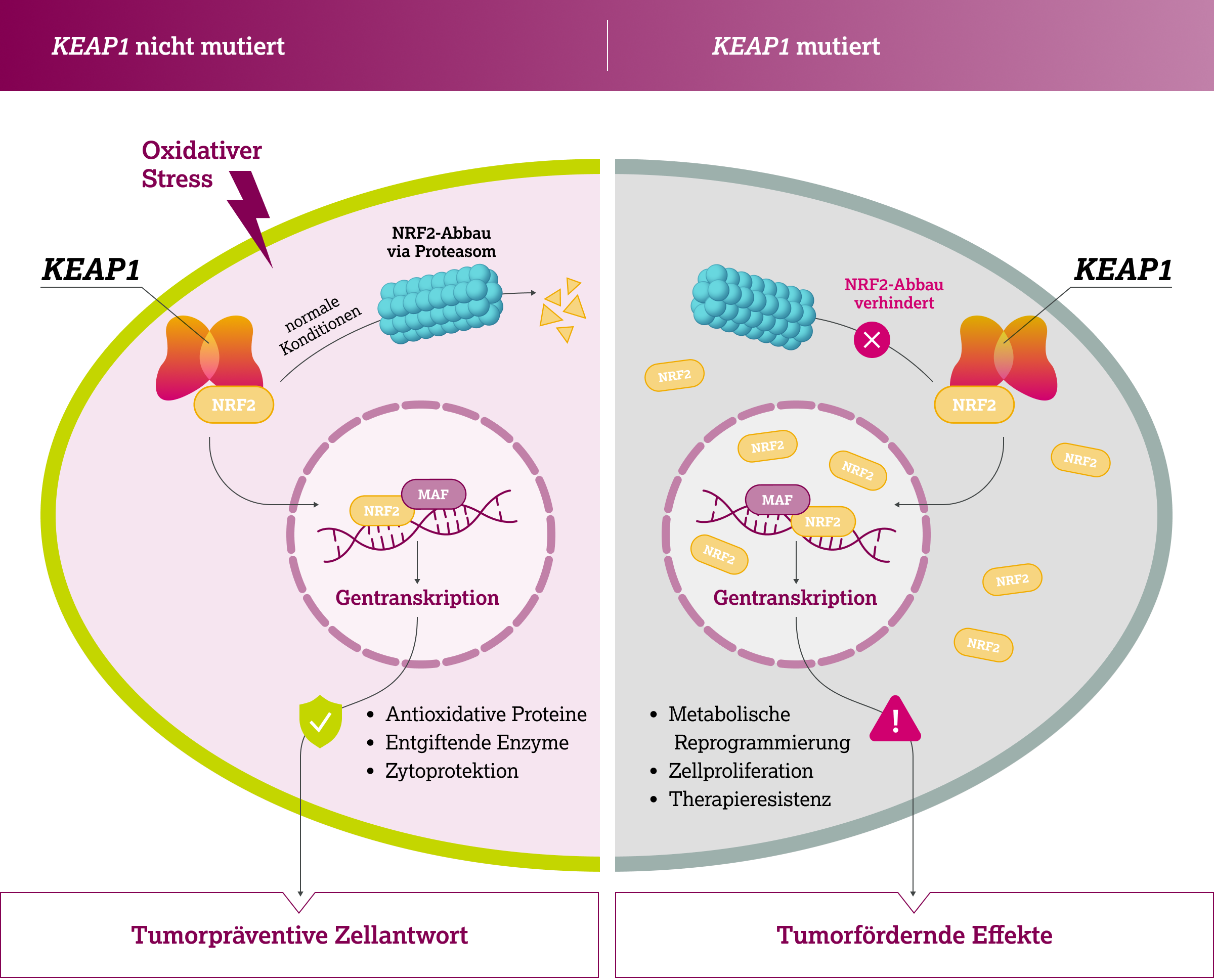
KEAP1/NRF2 reguliert die zelluläre Antwort auf oxidativen Stress
Zahlreiche Studien zeigen, dass der KEAP1-NRF2-Signalweg ein "zweischneidiges Schwert" darstellt: Er kann sowohl tumorpräventive als auch tumorfördernde Effekte entfalten.5,6 In gesunden Zellen reguliert KEAP1 den Transkriptionsfaktor NRF2 negativ, indem es dessen raschen proteasomalen Abbau vermittelt.5,7 Die dadurch bedingten niedrigen NRF2-Spiegel im Zellkern gewährleisten die Aufrechterhaltung der zellulären Homöostase.7 Bei erhöhtem oxidativem Stress wird NRF2 aktiviert und induziert vorübergehend die Transkription einer Vielzahl von Genen, die für antioxidative Proteine und Entgiftungsenzyme kodieren. Dadurch werden Karzinogene, reaktive Sauerstoffspezies (ROS) und andere DNA-schädigende Substanzen neutralisiert.5-7
Mutationen in KEAP1 führen zum Funktionsverlust des Proteins, wodurch die Interaktion mit NRF2 unterbrochen wird. Infolgedessen wird NRF2 nicht mehr abgebaut und akkumuliert in der Zelle, insbesondere im Zellkern.5-7 Auch die Aktivierung von Onkogenen wie KRASG12D kann über eine Transkriptionsinduktion von NRF2 zur nukleären Anreicherung führen.8
Ein dauerhaft erhöhter NRF2-Spiegel im Zellkern aktiviert nicht nur zytoprotektive Gene, sondern auch Stoffwechsel-Gene, die zur metabolischen Reprogrammierung und verstärkten Zellproliferation beitragen.7 Zusätzlich wird die Expression von Genen gesteigert, die am Arzneimittelmetabolismus beteiligt sind – was eine erhöhte Resistenz gegenüber Chemo-, Strahlen- und Immuntherapien zur Folge hat. Dieser Zustand wird als NRF2-Abhängigkeit bezeichnet.2,6,7,9
Tumoren mit dauerhaft hoher NRF2-Aktivität sind mit einer ungünstigen Prognose assoziiert. Dies ist nicht nur auf ihre Therapieresistenz, sondern auch auf ihre aggressive Proliferation zurückzuführen.
Daher ist die Identifizierung spezifischer KEAP1- und NRF2-Veränderungen von hoher klinischer Relevanz.8
Abkürzungen
KEAP1: Kelch-like ECH-associated protein 1 (Gen); KEAP1: Kelch-like ECH-associated protein 1 (Protein); KRAS G12D: Kirsten rat sarcoma mit G12D-Mutation; MAF: small musculoaponeurotic fibrosarcoma protein; NRF2: nuclear factor erythroid 2-related factor 2; ROS: reaktive Sauerstoffspezies
- Di Federico A, et al. Eur J Cancer 2021;157:108–13.
- Okazaki K, et al. Biophys Rev 2020;12(2):435–41.
- Ricciuti B, et al. J Thorac Oncol 2022;17(3):399–410.
- GeneCards®: The Human Gene Database. KEAP1 Gene - Kelch Like ECH Associated Protein 1. Verfügbar unter https://www.genecards.org/cgi-bin/carddisp.pl?gene=KEAP1. Letzter Zugriff: Januar 2026.
- Telkoparan-Akillilar P, et al. Molecules 2021;26(5):1417.
- Frank R, et al. Clin Cancer Res 2018;24(13):3087–96.
- Kansanen E, et al. Redox Biol 2013;1(1):45–9.
- Best SA, et al. Cell Metab 2018;27(4):935-943.e4.
- Scalera S, et al. J Thorac Oncol 2022;17(6):751–7.
