Entwicklung von Resistenzen gegenüber EGFR-TKI
Trotz initial hoher Ansprechraten entwickeln die meisten Patient:innen mit EGFR-mutiertem NSCLC im Verlauf eine Resistenz gegenüber EGFR-TKI. Bei über 60 % der Betroffenen tritt diese Resistenz innerhalb weniger Jahre auf und erfordert eine therapeutische Anpassung.1,2 Die zugrunde liegenden Mechanismen sind Folge der genetischen Plastizität maligner Zellen unter dem Selektionsdruck der zielgerichteten Therapie. Dieser führt zur Akkumulation zusätzlicher genetischer Alterationen, die die Wirksamkeit der EGFR-Inhibition unterlaufen.1–3
Mechanismen der EGFR-TKI-Resistenz
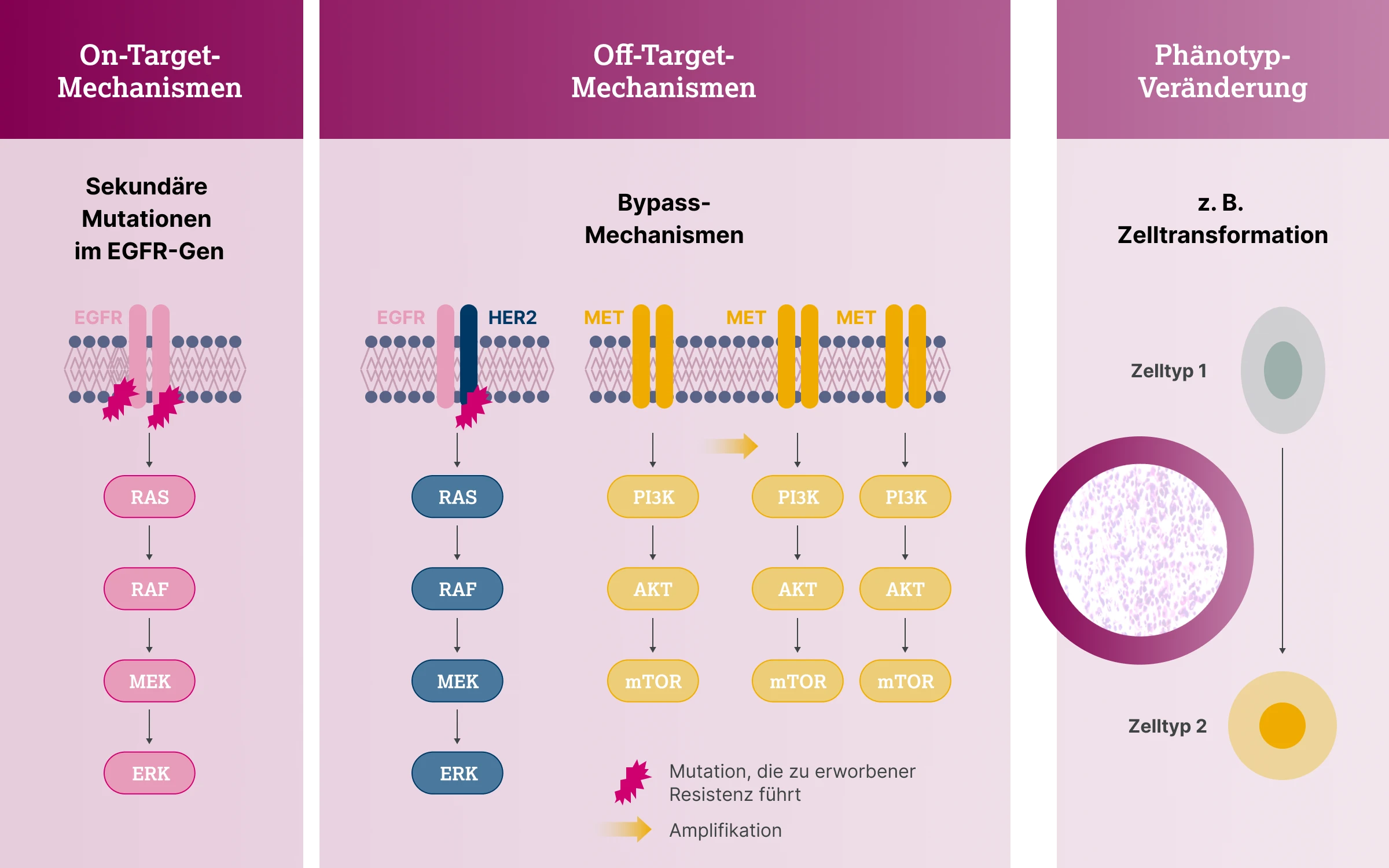
Die Resistenzentwicklung kann durch unterschiedliche Mechanismen bedingt sein, die in drei Hauptkategorien eingeteilt werden.
- On-target-Mechanismen: Sekundäre Mutationen im EGFR-Gen, wie z. B. T790M oder C797S, führen zu einer strukturellen Veränderung der Bindungsstelle und verringern so die Affinität des TKI.1
- Off-target- oder Bypass-Mechanismen: Hierbei liegt die Ursache außerhalb des EGFR-Gen, etwa in der Aktivierung alternativer Signalwege oder Mutationen anderer Onkogene wie MET, HER2 oder KRAS. Diese umgehen die Blockade des EGFR-Signalwegs.1
- Phänotypische Transformationen: Veränderungen im zellulären Differenzierungsstatus, etwa im Rahmen einer epithelial-mesenchymalen Transition (EMT) oder der Umwandlung in ein kleinzelliges Lungenkarzinom (SCLC), können zur Resistenz beitragen. Die molekularen Mechanismen sind hierbei bislang nicht vollständig aufgeklärt.1
Resistenzen unter TKI der 1. und 2. Generation
Unter einer Erstlinientherapie mit EGFR-TKI der 1. oder 2. Generation entwickeln die meisten Patient:innen im Verlauf erworbene Resistenzen. Am häufigsten wird dabei die T790M-Mutation nachgewiesen, die in etwa 50–60 % der Fälle für die Resistenz verantwortlich ist. Weniger häufig treten MET- oder HER2-Amplifikationen, PIK3CA-Mutationen sowie histologische Transformationen in ein kleinzelliges Lungenkarzinom (SCLC) auf.1,2,7
Die T790M-Mutation ist eine Missense-Mutation in der EGFR-Kinase-Domäne, bei der Threonin an Position 790 durch Methionin ersetzt wird. Der voluminösere Methioninrest behindert sterisch die Bindung des TKI an das ATP-Bindungszentrum, während die katalytische Funktion des EGFR erhalten bleibt.1 In solchen Fällen kann auf einen EGFR-TKI der 3. Generation umgestellt werden, der gezielt zur Überwindung der T790M-vermittelten Resistenz entwickelt wurde. Diese Inhibitoren binden kovalent und irreversibel an den mutierten EGFR und weisen eine höhere Selektivität auf.2,3
Resistenzen unter TKI der 3. Generation
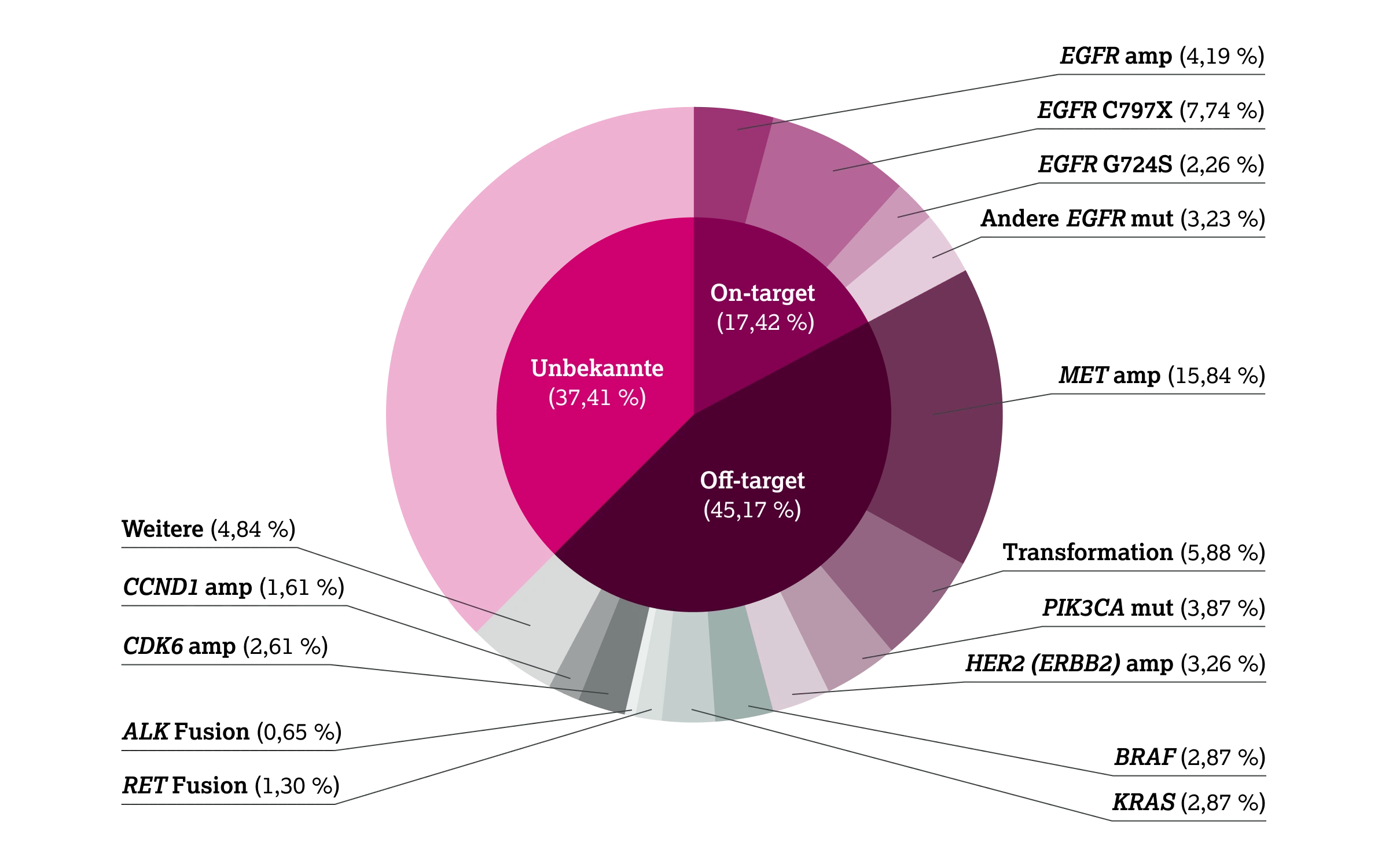
Unter Erstlinientherapie mit EGFR-TKI der 3. Generation werden On-target-Resistenzen deutlich seltener beobachtet (ca. 6–17 %) als unter TKI der 1. oder 2. Generation. Die häufigste EGFR-abhängige Resistenzmutation ist C797S. Sie kann isoliert oder in Kombination mit der T790M-Mutation auftreten.1
Weitere On-target-Veränderungen umfassen die G724S-Mutation in der P-Loop-Region, die durch eine Konformationsänderung der glycinreichen Schleife die Bindung des TKI verhindert. Darüber hinaus kann auch eine Amplifikation des Wildtyp-EGFR durch Reaktivierung von Signalwegen über Heterodimerisierung zu Resistenzen führen.1
Während der Behandlung mit EGFR-TKI der 3.Generation können Tumoren durch Nicht-EGFR-Mutationen oder Veränderungen in den Signalwegen resistent werden, vor allem durch MET-Amplifikation, Genfusionen, Reaktivierung nachgeschalteter EGFR-Signalwege und histologische Transformation.1
Die MET-Amplifikation stellt mit einem Anteil von etwa 16 % den häufigsten EGFR-unabhängigen Resistenzmechanismus unter EGFR-TKI der 3. Generation dar. Sie beruht auf der Bindung des Hepatozytenwachstumsfaktors (HGF) an den MET-Rezeptor, was zu einer Dimerisierung und Aktivierung führt. In der Folge werden EGFR-unabhängige Signalwege wie PI3K/AKT, JAK/STAT oder RAS/MAPK/ERK aktiviert, die die Wirksamkeit der Therapie unterlaufen. Folglich ist eine doppelte Hemmung von EGFR und MET erforderlich, um die durch MET-Amplifikation verursachte Resistenz zu überwinden.1
Auch die aberrante Aktivierung von HER2 kann zur Resistenz beitragen, indem sie unabhängig von der EGFR-Aktivität MAPK- und PI3K-Signalwege stimuliert.1 Darüber hinaus spielen onkogene Fusionen eine Rolle, die bei 1–10 % der Fälle auftreten. Sie betreffen unter anderem RET, BRAF, ALK, ROS1, FGFR3 und NTRK1 und führen über veränderte Tyrosinkinasen, Chromatinregulatoren oder Transkriptionsfaktoren zu einer anhaltenden Signalwegaktivierung.1
Abkürzungen
AKT: Serin/Threonin-Kinase AKT (Protein); ALK: Anaplastische Lymphomkinase (Gen); amp: amplifiziert; ATP: Adenosin-Triphosphat; BRAF: Serin/Threonin-Kinase B-Raf (Gen); C797S: Punktmutation im EGFR-Gen EGFR: epidermaler Wachstumsfaktor-Rezeptor (Protein); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); EMT: epithelial-mesenchymale Transition; ERK: extrazelluläre signalregulierte Kinase; FGFR: Fibroblasten-Wachstumsfaktor-Rezeptor; G724: Mutation in der Loop-Region des EGFR-Gens; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; HGF: Hepatozytenwachstumsfaktor; JAK: Januskinase; KRAS: Kirsten Rat Sarkoma (Gen); MEK: MAPK/ERK-Kinase; MET: Mesenchymal-epithelialer Transitionsfaktor (Gen); mTOR: mechanistic target of rapamycin; mut: mutiert; NSCLC: nicht-kleinzelliges Lungenkarzinom; NTRK: Neurotrophe Tyrosinrezeptor-Kinasen (Gen); PI3K: Phosphoinositid-3-Kinase (Protein); PIK3CA: Phosphoinositid-3-Kinase katalytische Untereinheit alpha (Gen); RAF: rapidly accelerated fibrosarcoma; RAS: Rat sarcoma (GTPase); RET: Rearranged during Transfection (Rezeptor-Tyrosinkinase); RET: Rearranged during Transfection (Gen); ROS1: ROS-Protoonkogen 1 (Gen); SCLC: kleinzelliges Lungenkarzinom; STAT: Signal Transducer and Activator of Transcription; T760M: Punktmutation im EGFR-Gen; TKI: Tyrosinkinase-Inhibitoren; WT: Wildtyp
- Zhou X, et al. Cancer Med 2025;14(9):e70921.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig (NSCLC); April 2025. Verfügbar unter www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: Februar 2026.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter register.awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: Februar 2026.
- Morgillo F, et al. ESMO Open 2016;1(3):e000060.
- Sun R, et al. Oncol Lett 2022;24(5):408.
- Li Y, et al. Cell Commun Signal 2023;21(1):71.
- Del Re M, et al. Int J Mol Sci 2019;20(16):3951.


