KRAS beim Lungenkarzinom
Bedeutung und Prävalenz von KRAS beim Lungenkarzinom
KRAS (Kirsten Rat Sarkoma) ist das bekannteste Onkogen mit der höchsten Mutationsrate aller Krebsarten und spielt eine Schlüsselrolle bei der Entstehung und Progression des nicht-kleinzelligen Lungenkarzinoms (NSCLC).1

Informationen zum KRAS-Protein.
Aktivierende KRAS-Mutationen zählen zu den häufigsten molekularen Alterationen beim NSCLC, insbesondere bei Adenokarzinomen der Lunge.2 Etwa 20–40 % der NSCLC-Adenokarzinome in westlichen Populationen weisen KRAS-Mutationen auf; Plattenepithelkarzinome in weniger als 5 %.2
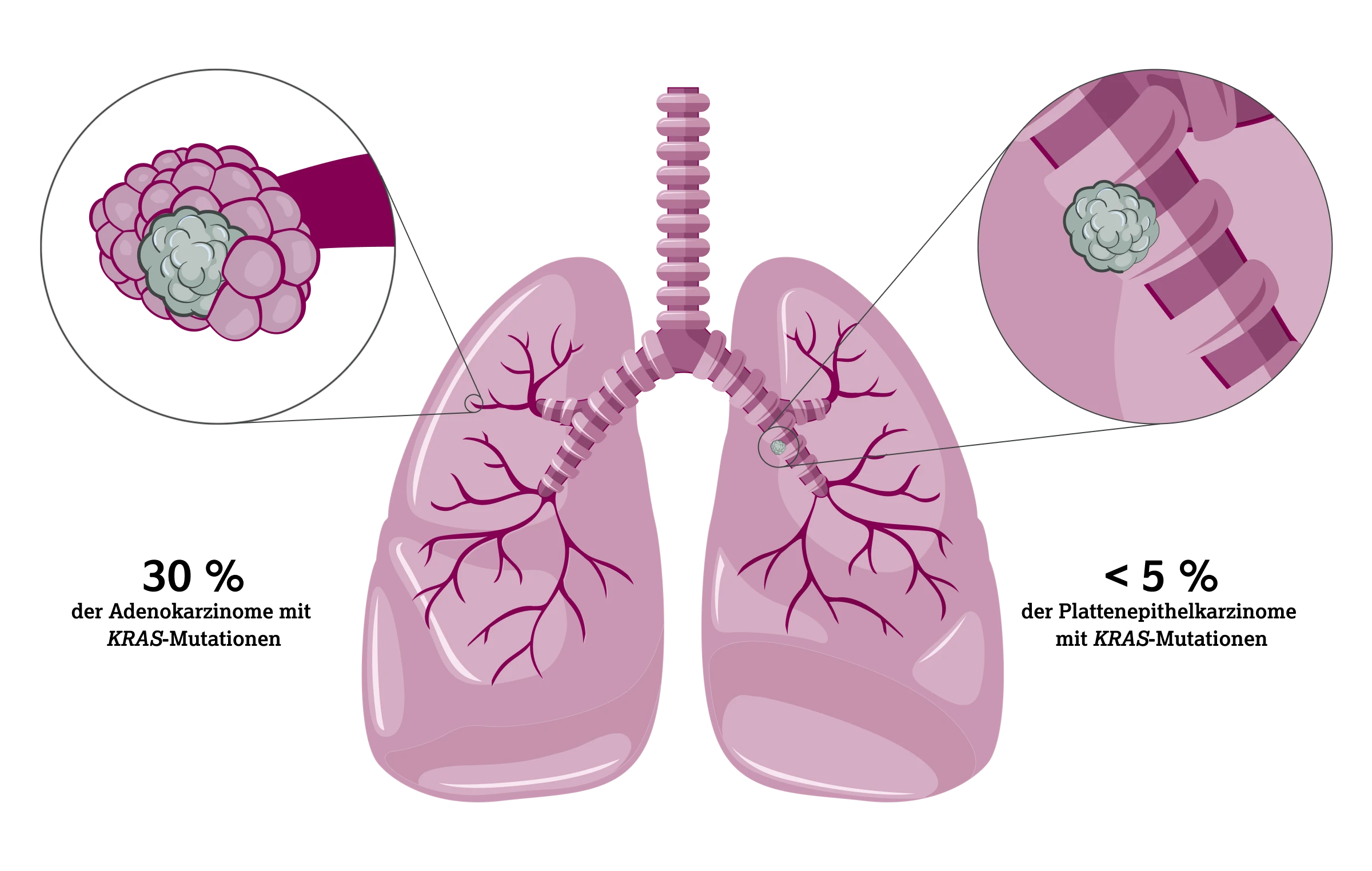
Zudem kommen KRAS-Mutationen bei Raucher:innen häufiger vor als bei Nichtraucher:innen (30 % vs. 11 %), bei Frauen häufiger als bei Männern (31 % vs. 24 %) und bei westlichen Patient:innen häufiger als bei asiatischen (26 % vs. 11 %).2,3
KRAS-Mutationen führen in der Regel zu einer dauerhaften Aktivierung des Signalwegs und begünstigen so das unkontrollierte Tumorwachstum. Lange Zeit galten diese Mutationen als nicht therapierbar („undruggable“), doch mit der Entwicklung spezifischer KRAS-Inhibitoren hat sich das therapeutische Spektrum entscheidend erweitert.1
Für die molekulare Diagnostik hat die KRAS-Testung heute eine zentrale Bedeutung: Zum einen ermöglicht sie eine präzise molekulare Subklassifikation des Tumors, zum anderen ist sie essenziell für die Auswahl zielgerichteter Therapien und für die Abgrenzung gegenüber anderen therapeutisch relevanten Treibermutationen.
KRAS G12C ist die häufigste somatische KRAS-Mutation beim NSCLC
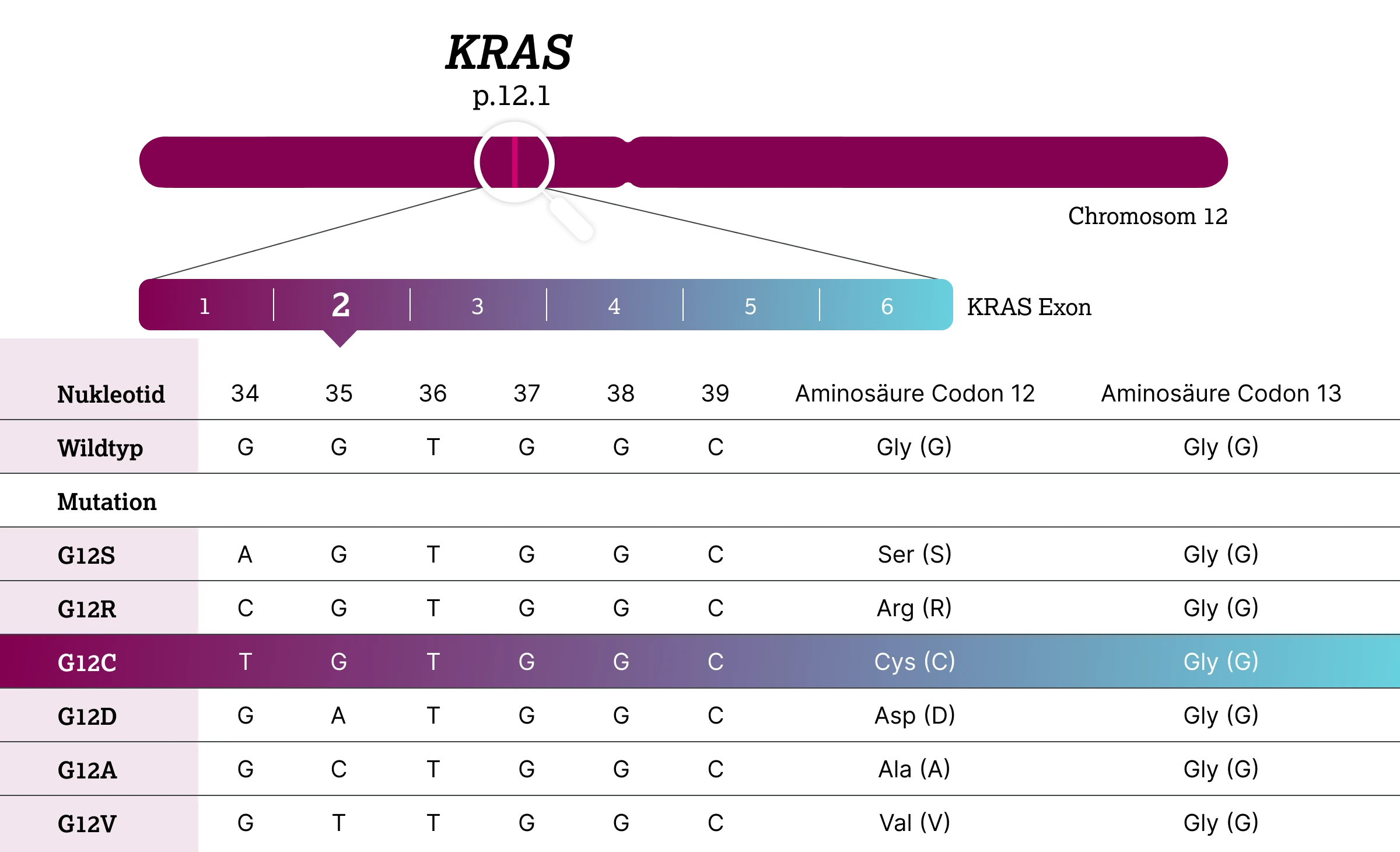
Etwa 90 % der KRAS-Mutationen werden im Exon 2 im Codon 12 nachgewiesen.2,3 Seltener sind Mutationen in Codon 13 (2-6 %) und Codon 61 (1 %).3 In der Regel führen die KRAS-Mutationen zu einer einzigen Aminosäuresubstitution.2
Beim NSCLC ist die häufigste somatische KRAS-Mutation KRAS G12C.2 Dabei wird ein Guanin (G) durch ein Thymin (T) an der Kodierungsposition 34 GGT->TGT (c.34G>T) ersetzt, was zu einem Austausch der Aminosäure Glycin (G) durch Cystein (C) führt (p.Gly12Cys).2
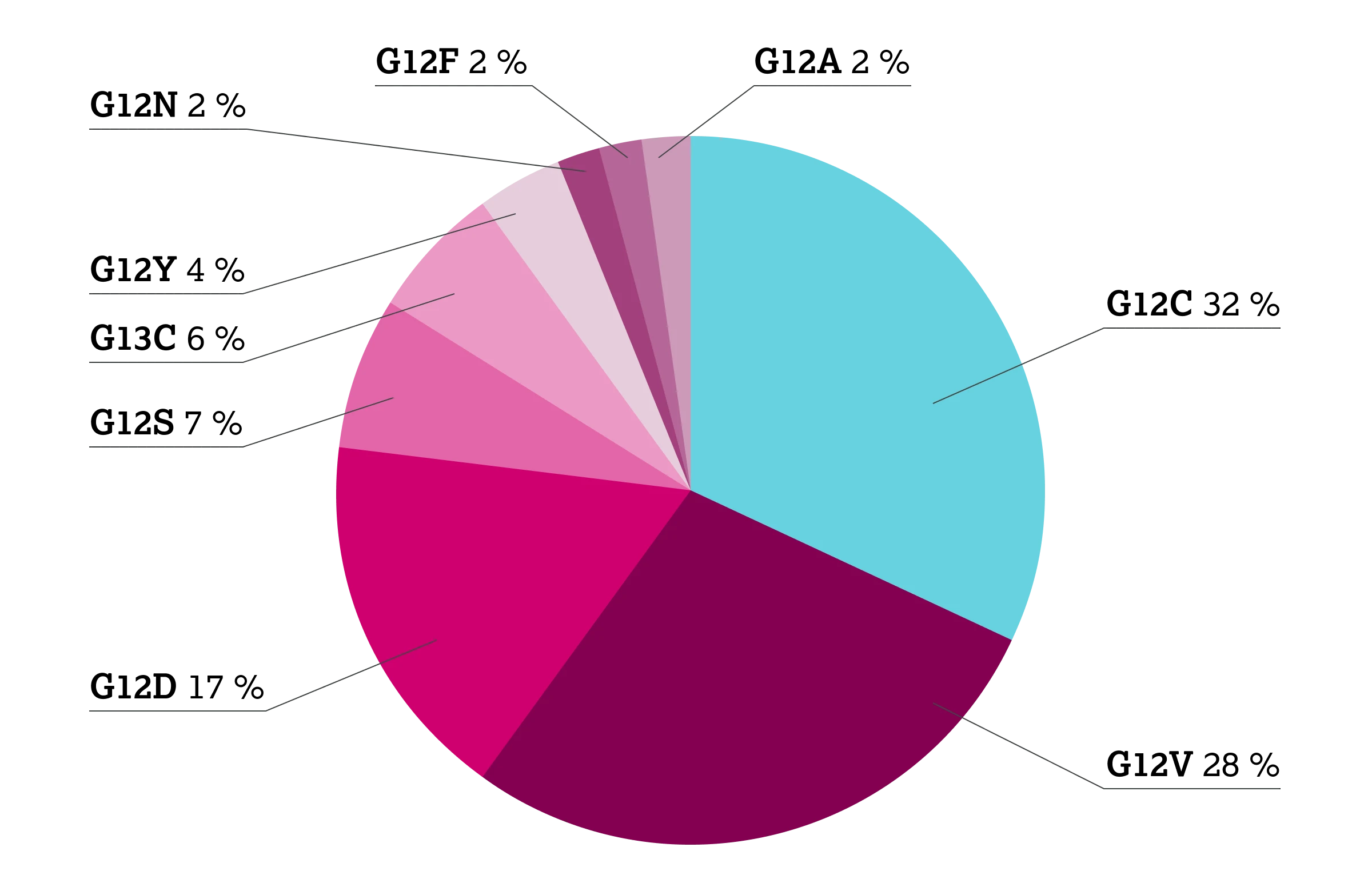
KRAS-G12C-Mutationen machen ca. 42 % der KRAS-Mutationen aus, 2 gefolgt von KRAS G12V (Mutation von Glycin zu Valin; ca. 21 %) und KRAS G12D (Mutation von Glycin zu Asparaginsäure; ca. 17 %).2 Andere Punktmutationen in Codon 12 wie G12A/R/S sind selten.3
KRAS-Mutationsvarianten und ihre unterschiedlichen Signalwege
Bemerkenswert ist, dass die verschiedenen KRAS-Mutationsvarianten ihre nachgeschalteten Signalwege unterschiedlich aktivieren können. So aktivieren die hydrophoben G12C und G12V bevorzugt den RAL-Signalweg, während die hydrophile G12D hauptsächlich über PI3K-AKT-Signale wirkt.3 Darüber hinaus können die KRAS-Mutationsvarianten unterschiedliche Auswirkungen auf den Tumor und die Metastasierung haben. KRAS-G12C-Mutanten sind beispielsweise eher mit Lungenmetastasen assoziiert (KRAS G12C vs. nicht-G12C: 38 % vs. 21 %; p = 0,043) und weniger mit Pleurametastasen oder lymphangitischer Karzinomatose (KRAS G12C vs. nicht-G12C: 4 % vs. 39 %, p = 0,0001).3 Erwähnenswert ist, dass Patient:innen mit KRAS-Mutationen keinen höheren Hirntropismus aufweisen als Patient:innen ohne KRAS-Alterationen, und dass die Häufigkeit von Hirnmetastasen bei verschiedenen KRAS-Mutationsvarianten gleich ist.3
Prädiktive und prognostische Rolle von KRAS-Mutationen beim NSCLC
In zahlreichen Studien wurde die prädiktive und prognostische Rolle von KRAS-Mutationen beim NSCLC untersucht – allerdings mit widersprüchlichen Ergebnissen.2,3,6 Viele Forscher berichteten, dass KRAS-Mutationen mit einem kürzeren Überleben und einer kürzeren Zeit bis zum Rezidiv korrelieren.6 In anderen Studien schließlich wurde kein Zusammenhang zwischen KRAS-Mutationen und Überleben festgestellt.6 Jedoch ist der KRAS-Mutationsstatus positiv mit der PD-L1-Expression korreliert. Dabei ist die mit KRAS-Mutationen assoziierte Prognose von gleichzeitig auftretenden molekularen Veränderungen abhängig: So wird eine schlechtere Prognose bei Patient:innen mit Co-Mutationen von KRAS und STK11 oder KEAP1 oder KRAS G12C und PD-L1-Expression beobachtet.4
KRAS-Co-Mutationen und deren Einflüsse
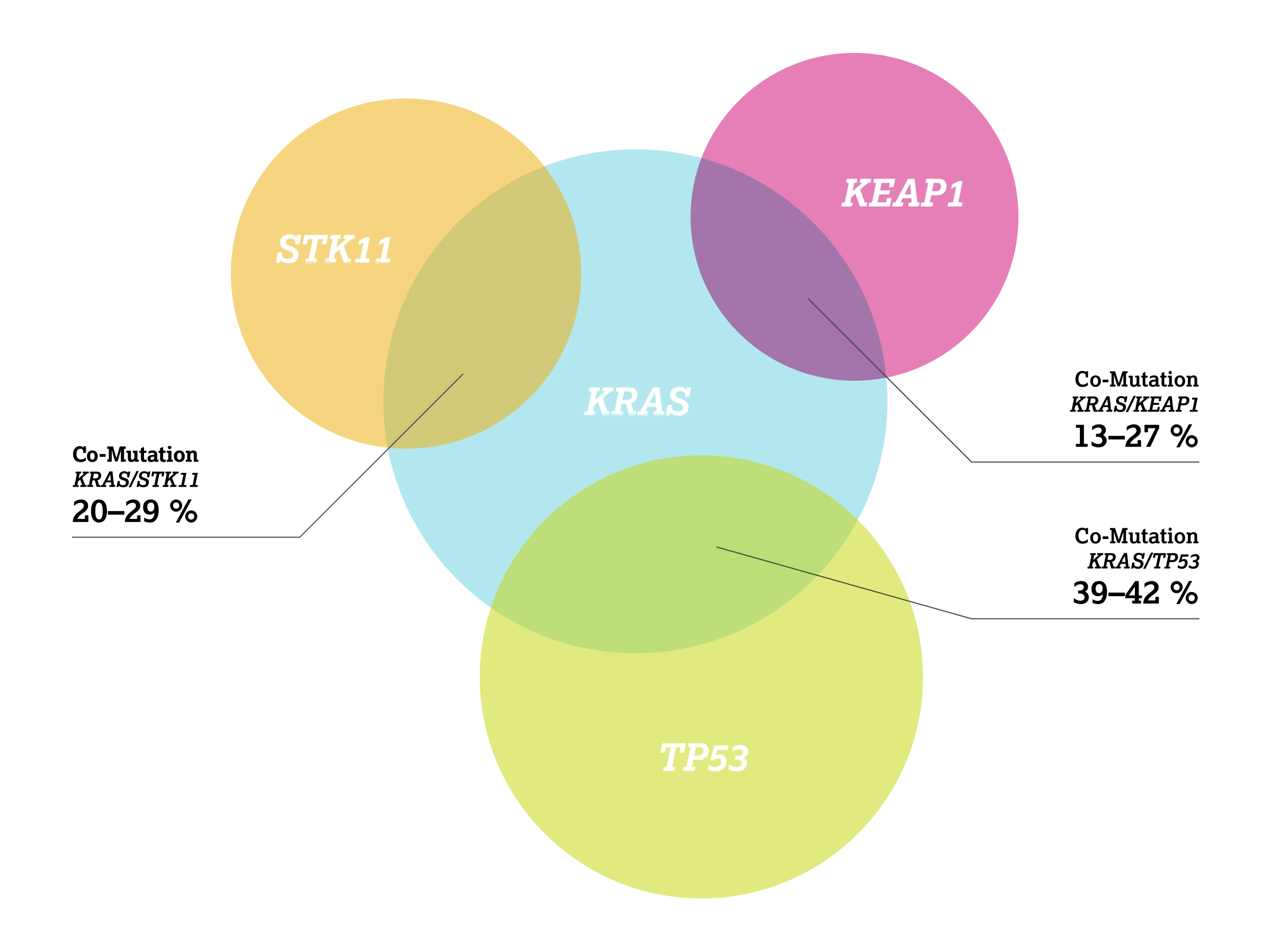
Bei etwa der Hälfte der KRAS-Mutationen treten zusätzlich Mutationen in anderen Onkogenen auf, wobei TP53 (39-42 %), STK11 (20-30 %) und KEAP1 (13-27 %) zu den am häufigsten berichteten Mutationen gehören.2,3 STK11 und KEAP1 wurden mit schlechteren Behandlungsergebnissen und einer schlechteren Prognose bei NSCLC-Patient:innen in Verbindung gebracht.2,7 Hingegen hat weder der TP53-Status noch die Anzahl der gleichzeitigen Mutationen das Gesamtüberleben (OS) beeinflusst.7
Die Co-Mutationen können sowohl über die intrinsischen RAS-Signalwege als auch über die Immuninfiltration der Tumoren wirken. So weisen beispielsweise KRAS/TP53-co-mutierte Tumore eine hohe CD8+-T-Zellen-Infiltrationsdichte und nur wenige regulatorische T-Zellen auf (sog. "heiße" Tumoren). Im Gegensatz dazu haben KRAS/STK11/KEAP1-co-mutierte Tumore nur eine geringe Dichte an infiltrierenden zytotoxischen CD8+-T-Lymphozyten, aber eine Fülle von regulatorischen T-Zellen (sog. "kalte" Tumoren) und sprechen weniger wahrscheinlich auf eine Immuntherapie an.1,2
Interessanterweise scheinen STK11- und KEAP1-Mutationen nur bei Patient:innen mit KRAS-mutiertem NSCLC zu schlechteren Ergebnissen bei der Immuntherapie zu führen, nicht aber bei KRAS-Wildtyp-Tumoren.2 Neuere Studien haben jedoch gezeigt, dass eine doppelte Immuntherapie das Outcome beim KRAS/STK11/KEAP-co-mutierten NSCLC verbessern kann.8
KRAS-Mutationen und andere molekulare Veränderungen beim NSCLC wie EGFR-Mutationen oder ALK- und ROS1-Fusionen schließen sich in der Regel gegenseitig aus.2 Jedoch wurden KRAS-Mutationen in ca. 3 % der MET Exon 14 Alterationen gefunden.3 Generell sollte bei KRAS-mutierten Tumoren auf andere Genveränderungen geachtet und eine individuelle Behandlung angestrebt werden.1

Informationen zu KEAP1 beim Lungenkarzinom.

Informationen zu STK11 beim Lungenkarzinom.
Studien & Leitlinienempfehlungen zur KRAS-Testung beim Lungenkarzinom
Die Bestimmung des KRAS-Status bei Patient:innen mit NSCLC ist für ein korrektes therapeutisches Management unerlässlich.3 Gemäß der aktuellen Onkopedia- und S3-Leitlinien sollte für alle Patient:innen mit NSCLC-Stadium IV vor Beginn einer medikamentösen Erstlinientherapie eine Testung auf KRAS G12C-Mutation im Rahmen einer umfassenden NGS-basierten Molekulardiagnostik durchgeführt werden.9,10
Grundsätzlich wird eine Testung auf alle therapeutisch relevanten, molekularen Veränderungen empfohlen.9,10 Nach derzeitigem Stand sollten diese zumindest folgende Biomarker vor Erstlinientherapie umfassen: ALK-Fusionen, BRAF V600E Mutationen, EGFR Exon 18-21 Mutationen, HER2-Mutationen, KRAS-G12C-Mutationen, c-MET Exon 14 Skipping Mutationen, NTRK-Fusionen, RET-Fusionen, ROS1-Fusionen.9,10
Auch das NCCN-Leitliniengremium für NSCLC empfiehlt nachdrücklich ein breiteres molekulares Profiling mit dem Ziel, seltene Treibermutationen zu identifizieren, für die möglicherweise bereits wirksame Medikamente zur Verfügung stehen, oder die Patient:innen angemessen über die Teilnahme an klinischen Studien zu beraten.11 Ein umfassendes molekulares Profiling ist ein wesentlicher Bestandteil der Verbesserung der Versorgung von Patient:innen mit NSCLC.11
Abkürzungen
AKT: Serin/Threonin-Kinase AKT (Protein); BRAF: Serin/Threonin-Kinase B-Raf (Gen); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Protein); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; KEAP1: Kelch-like ECH-associated protein 1 (Gen); KRAS: Kirsten Rat Sarkoma (Gen); MET: Mesenchymal-epithelialer Transitionsfaktor (Gen); NCCN: National Comprehensive Cancer Network; NSCLC: nicht-kleinzelliges Lungenkarzinom; NTRK: Neurotrophe Tyrosinrezeptor-Kinasen (Gen); OS: Gesamtüberleben; PD-L1: Programmed cell death ligand-1; PI3K: Phosphoinositid-3-Kinase (Protein); RAL: RAS-like GTPase; RAS: Rat sarcoma (GTPase); RET: Rearranged during Transfection (Rezeptor-Tyrosinkinase); RET: Rearranged during Transfection (Gen); ROS1: ROS-Protoonkogen 1 (Gen); STK11: Serin/Threonin-Kinase 11 (Gen); TP53: Tumorsuppressor-Protein P53 (Gen)
- Huang L, et al. Signal Transduct Target Ther 2021;6(1):386.
- Reita D, et al. Cancers (Basel) 2022;14(5):1321.
- Cascetta P, et al. Cancers (Basel) 2022;14(21):5430.
- Skoulidis F, et al. Nat Rev Cancer. 2019 Sep;19(9):495-509.
- Ricciuti B, et al. Ann Oncol. 2022 Oct;33(10):1029-1040.
- Cekani E, et al. Cancers (Basel) 2022;14(17):4103.
- Riely GJ, et al. J Clin Oncol 2016;34(15_suppl):9019.
- Johnson ML, et al. J Clin Oncol 2023:1213-1227.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig (NSCLC); April 2025. Verfügbar unter onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: Februar 2025.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: Februar 2025.
- NCCN Clinical Practice Guidelines in Oncology. Version 1.2026. November 6, 2025. Verfügbar unter https://www.nccn.org/professionals/physician_gls/pdf/nscl.pdf. Letzter Zugriff: Februar 2025.

