Was ist PD-L1 und welche Funktion hat es?
PD-L1 (Programmed Death-Ligand 1), auch bekannt als CD274 oder B7-H1, ist ein 40 kDa großes Typ-I-Transmembranprotein aus der B7-Familie immunregulatorischer Moleküle. Beim Menschen wird PD-L1 vom CD274-Gen kodiert, das sich auf Chromosom 9 befindet. Gemeinsam mit seinem Rezeptor PD-1 spielt es eine zentrale Rolle in der Regulation immunologischer Toleranz. PD-L1 wird sowohl auf Immunzellen (z. B. T- und B-Lymphozyten, Makrophagen, dendritische Zellen) als auch auf nicht-hämatopoetischen Zelltypen (z. B. in Endothel-, Leber-, Lungen- und Herzgewebe) exprimiert.1 Von besonderer klinischer Relevanz ist jedoch die Überexpression auf Tumorzellen, die zur Unterdrückung antitumoraler Immunantworten und somit zur Immunevasion beiträgt. Die Hochregulation von PD-L1 kann durch verschiedene Mechanismen ausgelöst werden, darunter genomische Amplifikationen, onkogene Signalwegaktivierung und inflammatorische Zytokinmilieus (z. B. IFN-γ und TNF-α).2–5
Molekularstruktur von PD-L1 und PD-1
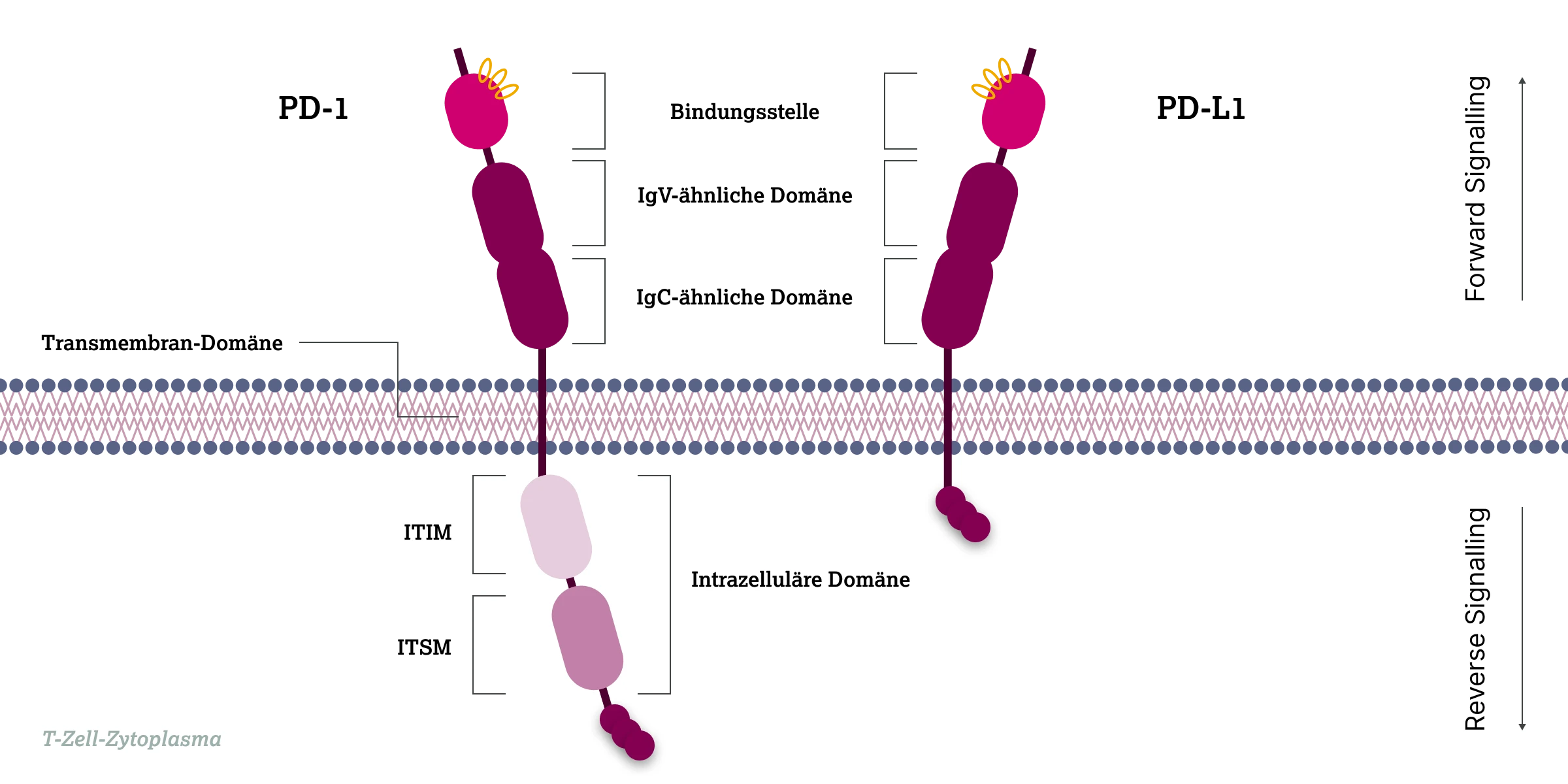
PD-L1 und sein Rezeptor PD-1 bestehen jeweils aus einer extrazellulären Domäne mit einer variablen Immunglobulin-ähnlichen Region (IgV-ähnliche Domäne) und einer konstanten Immunglobulin-ähnlichen Region (IgC-ähnliche Domäne), einer Transmembranregion sowie einer kurzen intrazellulären Domäne. Die IgV-Domäne vermittelt die spezifische Bindung von PD-L1 an PD-1 auf T-Zellen, während die IgC-Domäne zusätzliche strukturelle Stabilität bietet. Die verkürzte intrazelluläre Domäne von PD-L1 ist in der Lage, zellintrinsische Signalwege zu aktivieren.6,7
Die extrazellulären Domänen von PD-L1 und PD-1 sind strukturell ähnlich. Im Gegensatz dazu enthält die intrazelluläre Domäne von PD-1 zwei charakteristische Signalmotive: das Immunrezeptor-Tyrosin-basierte Inhibitionsmotiv (ITIM) und das Immunrezeptor-Tyrosin-basierte Switch-Motiv (ITSM). Beide sind entscheidend für die inhibitorische Signaltransduktion von PD-1.7
Funktion von PD-L1 im Immunsystem
Die Hauptfunktion von PD-L1 besteht in der Bindung an den inhibitorischen Rezeptor PD-1, der auf aktivierten T-Zellen sowie weiteren Immunzelltypen exprimiert wird. Diese Interaktion hemmt T-Zell-Proliferation, Zytokinproduktion und zytotoxische Effektoraktivität. Zudem fördert sie die Expansion regulatorischer T-Zellen und trägt zur Aufrechterhaltung der peripheren Immuntoleranz bei – ein Schutzmechanismus gegen Autoimmunität und exzessive Immunreaktionen.2–4
Tumorzellen nutzen diesen physiologischen Mechanismus gezielt aus, indem sie PD-L1 überexprimieren. Dadurch wird die lokale Immunantwort im Tumormikromilieu effektiv unterdrückt, was zur Immunevasion, Therapieresistenz und Tumorprogression führt.2–4

Forward und Reverse Signalling: Duale Rolle von PD-L1
PD-L1 fungiert nicht nur als Ligand, sondern auch als signalübertragendes Molekül. Diese bidirektionale Signalübertragung unterteilt sich in Signalling über a) die extrazellulare Domäne durch Interaktion mit PD-1 (Forward Signalling) und über b) die intrazelluläre Domäne, die zelltypspezifische, intrinsische Signalwege aktiviert (Reverse Signalling).
Die Bindung von PD-L1 an PD-1 auf T-Zellen führt zur Suppression der T-Zell-Aktivierung. Dies umfasst:
- Induktion peripherer Toleranz
- Umprogrammierung von Immunzellen (z. B. Makrophagen in immunsuppressive Phänotypen)
- Inhibition von Entzündungsreaktionen
Dieser Mechanismus bildet die Basis der Immunsuppression im Tumormikromilieu und ist das primäre Ziel der Immuncheckpoint-Inhibition.8,9
Die zytoplasmatische Domäne von PD-L1 kann selbst intrazelluläre Signaltransduktion auslösen, insbesondere nach Bindung an PD-1 oder ggf. andere Rezeptoren (z. B. CD80/CD86):
- In Tumorzellen fördert Reverse Signalling Tumorinitiation und Progression, indem es Zellproliferation, Überleben und metabolische Umprogrammierung unterstützt. Es werden AKT/mTOR, MAPK/ERK, β-Catenin und andere pro-proliferative Signalwege aktiviert.10–13
- In Immunzellen (z. B. dendritischen Zellen) reguliert Reverse Signalling die Zellmigration, das Überleben und möglicherweise die antigenpräsentierende Funktion.14,15
- Darüber hinaus trägt Reverse Signalling bei Tumorzellen zur Resistenz gegen Immuncheckpoint-Inhibitoren bei – etwa durch veränderte Glykolyse, Autophagie oder Anpassung an Stresssignale im Tumormilieu.16–19
Diese Erkenntnisse verdeutlichen die funktionelle Vielschichtigkeit von PD-L1: Als Ligand wirkt es immunregulatorisch, als Signalmolekül unterstützt es aktiv Tumorprogression und Therapieresistenz. Eine differenzierte Bewertung dieser Funktionen ist essenziell für die Entwicklung gezielter immunonkologischer Strategien.

Informationen zu den Studien- und Leitlinienempfehlungen zur PD-L1 Testung beim Lungenkarzinom.
Abkürzungen
AKT: Serin/Threonin-Kinase AKT (Protein); B7-H1: B7-Homolog 1; CD80: Cluster of Differentiation 80; CD86: Cluster of Differentiation 86; CD274: Cluster of Differentiation 274; ERK: extrazelluläre signalregulierte Kinase; IFN-γ: Interferon gamma; IgC: Immunglobulin-konstante Domäne; IgV: Immunglobulin-variable Domäne; ITIM: Immunrezeptor-Tyrosinbasiertes Inhibitionsmotiv; ITSM: Immunrezeptor-Tyrosinbasiertes Switch-Motiv; kDa: Kilodalton; MAPK: Mitogen-aktivierte Proteinkinase; mTOR: mechanistic target of rapamycin; PD-1: Programmed Death-1; PD-L1: Programmed Death-Ligand 1; TNF-α: Tumornekrosefaktor alpha
- Keir ME, et al. Annu Rev Immunol 2008;26:677–704.
- Sabaghian A, et al. J Cancer Metastasis Treat 2024;10:19.
- Han Y, et al. Am J Cancer Res 2020;10(3):727–42.
- Ortega MA, et al. J Mol Med (Berl) 2024;102(8):987–1000.
- Soltani M, et al. Clin Exp Med 2025;25(1):106.
- Li Z, et al. Biochim Biophys Acta Rev Cancer 2024;1879(5):189152.
- Sagrero-Fabela N, et al. Int J Mol Sci 2024;25(14):7726.
- Schöniger S, et al. Animals (Basel) 2022;12(19):2661.
- Wang Q, et al. Adv Biol (Weinh) 2021;5(9):e2100758.
- Yu W, et al. Cell Death Dis 2020;11(7):506.
- Lu M-M, et al. Front Immunol 2024;15:1395332.
- Gato-Cañas M, et al. Cell Rep 2017;20(8):1818–29.
- Jalali S, et al. Blood Cancer J 2019;9(3):22.
- Tamburini BAJ. FEBS J 2022;289(20):6256–66.
- Lucas E, et al. Appl Immunohistochem Mol Morphol 2019;27(6):403–9.
- Liechtenstein T, et al. Oncoimmunol 2014;3(7):e945378.
- Chang C-H, et al. Cell 2015;162(6):1229–41.
- Clark CA, et al. Cancer Research 2016;76(23):6964–74.
- Azuma T, et al. Blood 2008;111(7):3635–43.