STK11 beim Lungenkarzinom
Bedeutung und Prävalenz von STK11 beim NSCLC
STK11 kodiert für die Leber-Kinase B1 (LKB1), eine Serin/Threonin-Kinase, die eine zentrale Rolle in der Regulation von Zellwachstum und -proliferation spielt.1 Eine Inaktivierung von STK11 oder der Verlust der LKB1-Funktion hebt diese wachstumshemmenden Mechanismen auf und fördert die unkontrollierte Proliferation maligner Zellen.1,2
Somatische STK11-Mutationen zählen nach TP53 zu den am zweithäufigsten auftretenden Veränderungen in Tumorsuppressorgenen beim nicht kleinzelligen Lungenkarzinom (NSCLC).3 In großen NSCLC‑Kohorten, insbesondere beim Lungenadenokarzinom, liegt die berichtete Prävalenz typischerweise bei etwa 15–20 %.4–6 Eine Assoziation besteht insbesondere mit Adenokarzinom-Histologie und Tabakexposition.3
KRAS-Mutationen und STK11/KEAP1-Co-Mutationen
Die Mutation des Kirsten Rat Sarcoma Onkogen (KRAS) ist eine der häufigsten genomischen Alterationen beim NSCLC, insbesondere beim Lungenadenokarzinom. Bei etwa der Hälfte der Patient:innen mit KRAS-mutiertem NSCLC finden sich zusätzliche Mutationen in Tumorsuppressorgenen, am häufigsten STK11 (20–29 %) und KEAP1 (13–27 %).7

Informationen zur Diagnostik von KRAS, STK11 und KEAP1.
STK11/LKB1- und KEAP1-Co-Mutationen beim NSCLC
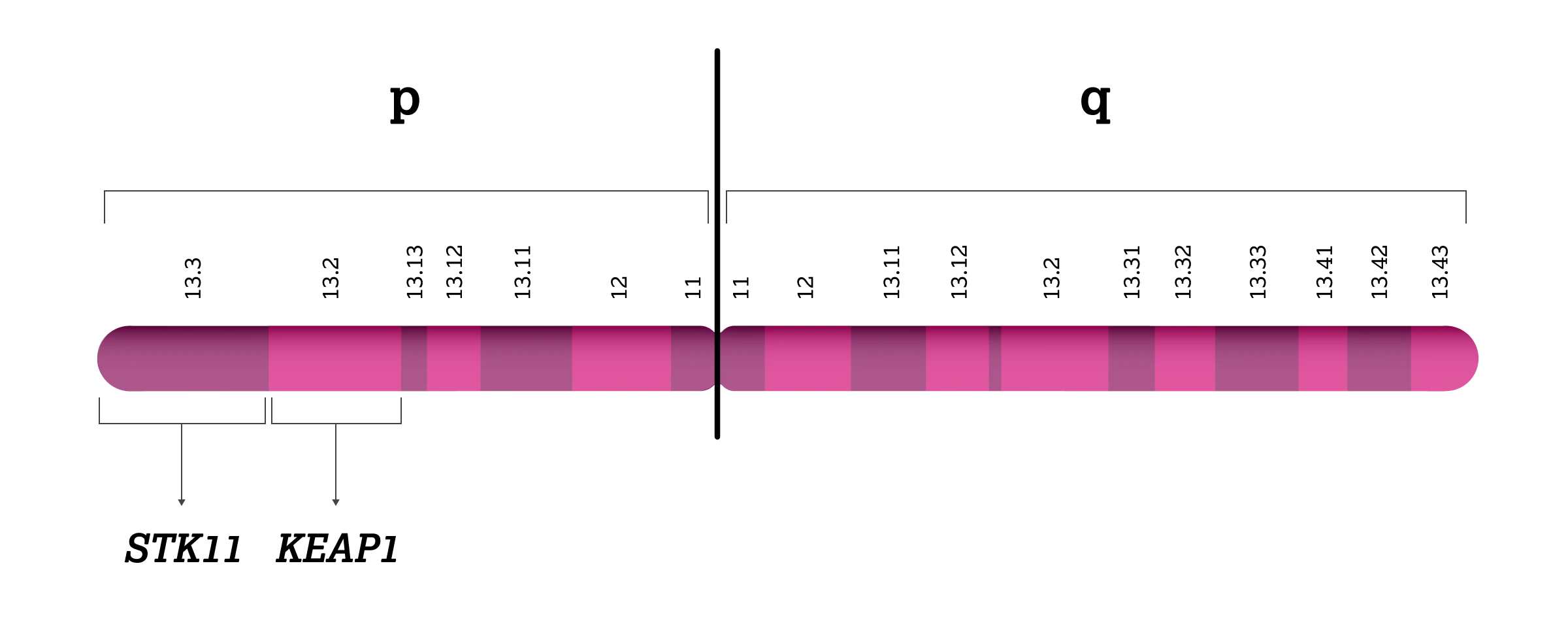
STK11‑ und KEAP1‑Mutationen treten beim NSCLC häufig gemeinsam auf.3 Eine mögliche Erklärung liegt in der Nähe beider Genorte auf dem kurzen Arm von Chromosom 19 (auf 19p13.3 für STK11 und auf 19p13.2 für KEAP1).3
Das gleichzeitige Auftreten von STK11- und KRAS-Mutationen beim NSCLC ist mit schlechteren Überlebensraten nach Chemo- und Immuntherapie assoziiert.2,10 Die durch die KRAS-Mutation initiierte onkogene Signaltransduktion wird durch die Inaktivierung von LKB1 weiter verstärkt, was zu erhöhter Zellproliferation, verringerter Differenzierung und gesteigertem metastatischem Potenzial führt.11
Auch bei KRAS-mutiertem NSCLC entfalten STK11- und KEAP1-Verlust eine synergistische onkogene Wirkung.3 In mehreren Studien war das gleichzeitige Vorliegen dieser Mutationen mit einem verminderten Ansprechen auf PD-(L)1 Inhibitoren verbunden.5,12–15 In einigen Studien wurden die Gesamtüberlebensergebnisse (OS) bei Patient:innen mit fortgeschrittenem NSCLC, die mit Chemotherapie, Immuntherapie oder Immunchemotherapie behandelt wurden, bei Patient:innen mit KRAS-mutiertem NSCLC mit Co-Mutationen in STK11 oder KEAP1 als schlechter festgestellt, verglichen mit Tumoren mit ausschließlich KRAS-Mutationen.1,16–18
„Kalte“ Tumormikroumgebung bei STK11-Mutationen
Präklinische und klinische Daten haben gezeigt, dass STK11-Mutationen und der daraus resultierende Verlust der LKB1-Funktion tiefgreifende Veränderungen in der Tumormikroumgebung (TME) bewirken.3,18 Diese Veränderungen führen zur Ausbildung einer „kalten“, immunsuppressiven TME, die durch folgende Merkmale gekennzeichnet ist:3

geringere Dichte infiltrierender zytotoxischer CD8+-T-Lymphozyten

verringerte PD-(L)1-Expression

vermehrte Infiltration neutrophiler Granulozyten
Diese immunologisch inaktive Mikroumgebung ist mit einem eingeschränkten Ansprechen auf Immuncheckpoint-Inhibitoren assoziiert.3,15,18

Informationen zu kalten Tumoren und möglichen Effekten einer dualen Immuncheckpoint-Blockade.
Studien & Leitlinienempfehlungen zur STK11-Testung beim Lungenkarzinom
Die Testung auf STK11-Mutationen hat in der Diagnostik und Therapieplanung beim NSCLC eine wichtige prognostische und potenziell prädiktive Rolle, auch wenn sie (Stand 2025) noch nicht zu den obligatorischen Biomarkern wie EGFR, ALK, ROS1, BRAF, NTRK, PDL-1, RET, MET und HER2 gehört.19,20 STK11 ist jedoch in zahlreichen kommerziell verfügbaren NGS-Panels enthalten.
STK11-Mutationen sind von prognostischer Bedeutung, insbesondere bei NSCLC-Patient:innen unter Therapie mit Immuncheckpoint-Inhibitoren (ICIs).
Frühe Studien weisen darauf hin, dass STK11-mutierte Tumoren – insbesondere bei begleitenden Alterationen in TP53, KRAS oder KEAP1 – eine primäre Resistenz gegenüber ICIs aufweisen.21
Angesichts der klinischen Relevanz erscheint die Mitaufnahme von STK11 und KEAP1 in routinemäßig eingesetzte NGS-Diagnostikpanels beim NSCLC sinnvoll und gerechtfertigt.1
Abkürzungen
ALK: Anaplastische Lymphomkinase (Gen); BRAF: Serin/Threonin-Protein-Kinase B-Raf (Gen); EGFR: epidermaler Wachstumsfaktor-Rezeptor (Gen); HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2 (Gen); ICB: Immuncheckpoint-Blockade; ICI: Immun-Checkpoint-Inhibitor; KEAP1: Kelch-like ECH-associated protein 1 (Gen); KRAS: Kirsten Rat Sarcoma Onkogen; LKB1: Leber-Kinase B1; MET: Mesenchymal-epitheliale Transition (Gen); NGS: Next-Generation Sequencing; NSCLC: nicht-kleinzelliges Lungenkarzinom; NTRK: Neurotrophe Tyrosinrezeptor-Kinase (Gen); PD-1: Programmed cell death-1; PD-L1: Programmed cell death ligand-1; RET: Rearranged during Transfection (Protoonkogen); ROS1: c-ROS Onkogen 1; STK11: Serin/Threonin-Kinase-11 (Gen); TME: Tumormikroumgebung; TP53: Tumorsuppressor-Gen p53
- Shiller M, et al. Front Oncol 2024;14:1459737.
- Shire NJ, et al. PLoS ONE 2020;15(9):e0238358.
- Pons-Tostivint E, et al. Cells 2021;10(11):3129.
- Devarakonda S, et al. Lancet Oncol 2015;16(7):e342-51.
- Papillon-Cavanagh S, et al. ESMO Open 2020;5(2):e000706.
- Cancer Genome Atlas Research Network. Comprehensive molecular profiling of lung adenocarcinoma. 2014;511(7511):543–50.
- Reita D, et al. Cancers (Basel) 2022;14(5):1321.
- GeneCards®: The Human Gene Database. STK11 Gene - Serine/Threonine Kinase 11. Verfügbar unter genecards.org/cgi-bin/carddisp.pl?gene=STK11. Letzter Zugriff: März 2026.
- GeneCards®: The Human Gene Database. KEAP1 Gene - Kelch Like ECH Associated Protein 1. Verfügbar unter genecards.org/cgi-bin/carddisp.pl?gene=KEAP1&keywords=KEAP1. Letzter Zugriff: März 2026.
- La Fleur L, et al. Lung Cancer 2019;130:50–8.
- Pavan A, et al. Transl Lung Cancer Res 2021;10(1):202–20.
- Di Federico A, et al. J Natl Cancer Inst 2023;115(1):29–42.
- Di Federico A, et al. Eur J Cancer 2021;157:108–13.
- Marinelli D, et al. Ann Oncol 2020;31(12):1746–54.
- Skoulidis F, et al. Nature 2024;635(8038):462–71.
- Julian C, et al. BMC Cancer 2023;23(1):352.
- Dabbous F, et al. J Clin Oncol 2023;41(16_suppl):e21186-e21186.
- Knetki-Wróblewska M, et al. Transl Lung Cancer Res 2024;13(12):3718–30.
- S3-Leitlinie Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Version 4.0, April 2025. Verfügbar unter awmf.org/assets/guidelines/020-007OLl_S3_Praevention-Diagnostik-Therapie-Nachsorge-Lungenkarzinom_2025-04.pdf. Letzter Zugriff: März 2026.
- onkopedia Leitlinie Lungenkarzinom, nichtkleinzellig (NSCLC); April 2025. Verfügbar unter onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html. Letzter Zugriff: März 2026.
- Mograbi B, et al. Diagnostics (Basel) 2021;11(2):196.


