Qualitätssicherung in pathologischen Laboren
Ein strukturiertes Qualitätsmanagementsystem (QMS) ist unverzichtbar für die diagnostische Qualität in pathologischen Laboren. Fehler in der Präanalytik, unvollständige Befundung oder unzureichend dokumentierte Ergebnisse seitens der Pathologie können schwerwiegende Folgen für Therapieentscheidungen und Verlaufskontrollen haben. Um die Qualität über alle Prozessschritte – von der Probenannahme bis zur Befundübermittlung – sicherzustellen, sind standardisierte Verfahren und kontinuierliche Qualitätssicherungsmaßnahmen erforderlich.
Zielsetzung der Qualitätssicherung in der Pathologie
Qualitätssicherung in der Pathologie verfolgt das Ziel, eine reproduzierbare, valide und nachvollziehbare Diagnostik zu gewährleisten. Dabei ist besonders auf die Komplexität der pathologischen Diagnostikkette zu achten, die zahlreiche, teilweise hochspezialisierte Methoden umfasst.1
Zu den Kernzielen zählen:

Minimierung präanalytischer Variabilität: standardisierte Fixierung, Transport und Probenannahme

Absicherung der diagnostischen Validität: Qualitätskontrolle bei der Herstellung der Gewebeschnitte, Färbungen, IHC, molekularpathologischen Verfahren und Erfassung digitaler Bilder

Verlässlichkeit der Befunderstellung: 4-Augen-Prinzip bei der Diagnosestellung, strukturierte Befundung, Einhaltung von Durchführungszeiträumen (TAT)

Sicherung der Nachvollziehbarkeit und Archivierung: Dokumentation gemäß gesetzlichen Vorgaben (z. B. DSGVO, IfSG) und digitale Langzeitarchivierung
Nationale Vorgaben: Rili-BÄK Pathologie (Beschluss 2025)
Am 23. April 2025 hat der Vorstand der Bundesärztekammer (BÄK) die Erstellung einer eigenständigen Qualitätssicherungsrichtlinie für die Pathologie beschlossen – die sogenannte „Rili-BÄK Pathologie“. Diese soll die bisherigen allgemeinen Vorgaben der Rili-BÄK (Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen)2 um fachlich spezifische Anforderungen erweitern und erstmals einen verbindlichen Qualitätsrahmen für die Fächer Pathologie und Neuropathologie etablieren.1
Die geplante Richtlinie soll:
- die gesamte Diagnostikkette der Pathologie – von der Probenannahme über die histologischen, immunhistochemischen, molekularen und digital gestützten Verfahren bis zur Befunderstellung – abdecken,
- verbindliche Standards für Qualitätskontrolle, Dokumentation, Befundvalidierung und Nachverfolgbarkeit setzen,
- bereits etablierte Strukturen wie Ringversuche (z. B. durch die QuIP) und freiwillige Akkreditierungsverfahren systematisch integrieren,
- und den Dialog mit den anderen in-vitro-diagnostischen Fachdisziplinen stärken.1
Die Richtlinie wird voraussichtlich im zweiten Halbjahr 2026 veröffentlicht und dann mit einer Übergangsfrist von 18 Monaten vollständig in Kraft treten. Sie soll bestehende freiwillige Initiativen konsolidieren und zugleich rechtssichere Mindeststandards für alle pathologischen Einrichtungen schaffen.1
Freiwillige Qualitätssicherung: QuIP und Akkreditierung
Bereits seit Jahren sind freiwillige Maßnahmen integraler Bestandteil der Qualitätssicherung in der Pathologie:
- Die QuIP (Qualitätssicherungs-Initiative Pathologie) wurde 2004 als fachgebietsbezogene Organisation gegründet. Über 300 Institute nehmen jährlich an den dort angebotenen Ringversuchen teil.1
- Der erste Ringversuch universitärer Institute wurde bereits 1999 durchgeführt.1
- Seit den frühen 2000er-Jahren besteht die Möglichkeit zur freiwilligen Akkreditierung pathologischer Labore, aktuell sind über 110 Institute für Pathologie und Neuropathologie entsprechend zertifiziert.1
Diese Instrumente bieten eine robuste Grundlage, auf der die geplante Rili-BÄK Pathologie aufbauen kann.
Internationale ISO-Normen für pathologische Einrichtungen
Auch pathologische Labore können von einer Orientierung an internationalen ISO-Normen profitieren – insbesondere, wenn eine Akkreditierung oder die Teilnahme an fachübergreifenden Netzwerken angestrebt wird:
Diese Norm definiert die Anforderungen an medizinische Laboratorien hinsichtlich Qualität und technischer Kompetenz. Sie wurde 2022 umfassend überarbeitet und bezieht nun auch Risiko- und Probenmanagement stärker ein – relevant für histologische und molekulare Pfade in der Pathologie.3
Die Akkreditierung nach ISO 15189 ist ein freiwilliges Verfahren, das in der ambulanten Labordiagnostik bereits nahezu flächendeckend umgesetzt wird.4 In bestimmten Bereichen ist sie jedoch gesetzlich vorgeschrieben – etwa bei Vaterschaftsuntersuchungen gemäß Gendiagnostikgesetz.4 Auch für ausgewählte Leistungen, wie das Neugeborenen-Screening, stellt die Akkreditierung nach ISO 15189 eine Voraussetzung für die Abrechenbarkeit dar.4
Diese Norm richtet sich primär an Inspektionsstellen, ist aber auch für bestimmte medizinische Bereiche wie Pathologie, Neuropathologie und Dermatohistologie bedeutsam, insbesondere bei der Bewertung und Inspektion von Befunden. Hier stehen Objektivität, Nachvollziehbarkeit und Unabhängigkeit im Fokus.5,6
Als prozessorientierte Managementnorm ist die DIN EN ISO 9001 branchenübergreifend einsetzbar. Viele pathologische Institute nutzen sie als Ergänzung zur ISO 15189 oder als Basis für ihr internes QM. Sie ist insbesondere für größere Strukturen mit Verwaltungseinheiten von Vorteil. Die Umsetzung kann durch Zertifizierung nachgewiesen werden, ist jedoch in pathologischen Laboratorien nicht weit verbreitet.4,7
Von freiwilliger Qualität zur regulatorischen Pflicht
Internationale Normen wie ISO 15189, ISO/IEC 17020 und ISO 9001 bilden die Grundlage für einheitliche und überprüfbare Qualitätsstandards in medizinischen Laboratorien – auch in der Pathologie. Doch mit der Einführung der In-vitro-Diagnostika-Verordnung (IVDR) auf EU-Ebene rückt nun zusätzlich ein verbindliches regulatorisches Rahmenwerk in den Mittelpunkt, das über ISO-Normen hinausgeht und auch rechtlich verbindliche Anforderungen an Qualität, Sicherheit und Nachvollziehbarkeit stellt.
Diese neue europäische Gesetzgebung hat wesentliche Auswirkungen auf die Struktur und das Qualitätsmanagement diagnostischer Labore in Deutschland – insbesondere auf pathologische Einrichtungen, die eigene Untersuchungsverfahren entwickeln oder anwenden.8

Informationen zur IVDR
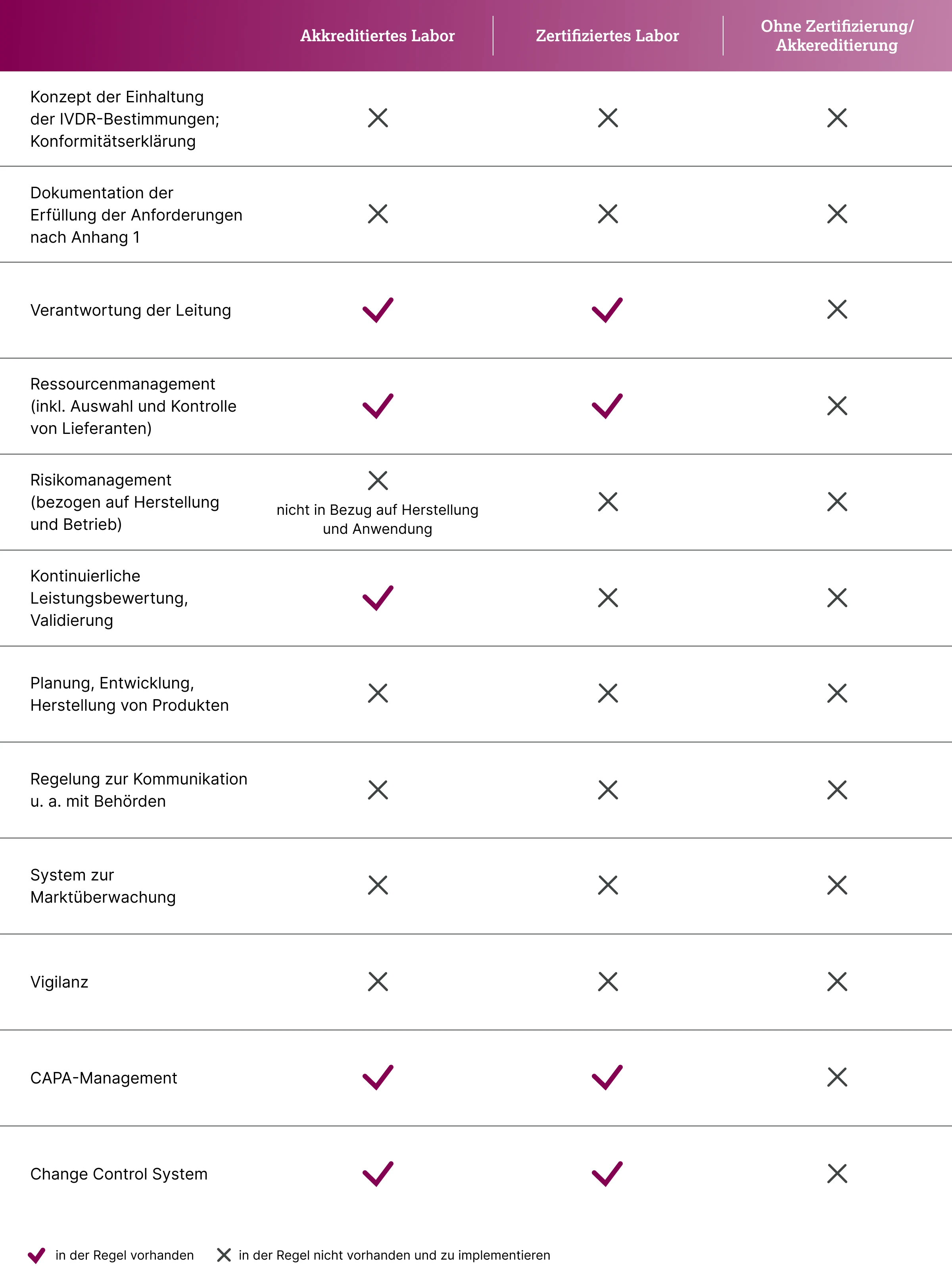
Qualitätsnachweis: Zertifizierung versus Akkreditierung
Die Qualität diagnostischer Prozesse in Laboren lässt sich durch Zertifizierungen oder Akkreditierungen belegen. Beide Verfahren zielen auf die Sicherstellung strukturierter Abläufe ab, unterscheiden sich jedoch erheblich in Aussagekraft und regulatorischer Relevanz – insbesondere im Kontext der EU-Verordnung über In-vitro-Diagnostika (IVDR, EU 2017/746).8
Während die Zertifizierung, etwa nach DIN EN ISO 9001, die Konformität eines Qualitätsmanagementsystems mit allgemeinen Anforderungen überprüft, trifft sie keine Aussage über die fachliche Kompetenz des Labors –insbesondere nicht über die Validität oder Reproduzierbarkeit diagnostischer Verfahren.7 Zertifizierungen werden durch akkreditierte Stellen (TÜV, DEKRA, etc.) erteilt. Für den Nachweis regulatorischer Eignung im Sinne der IVDR ist eine Zertifizierung allerdings nicht ausreichend.
Die Akkreditierung – insbesondere nach DIN EN ISO 15189 – geht darüber hinaus: Sie bewertet auch die fachlich-diagnostische Kompetenz eines Labors. Bewertet werden u. a. Validität und Verlässlichkeit eingesetzter Verfahren, Eignung des Personals und der Infrastruktur, Nachvollziehbarkeit und Reproduzierbarkeit diagnostischer Ergebnisse, Dokumentation von Prüfprozessen und Qualitätskennzahlen.3 Die Akkreditierung erfolgt in Deutschland durch die Deutsche Akkreditierungsstelle (DAkkS) und gilt als anerkannter Nachweis zur Erfüllung der IVDR-Anforderungen, insbesondere bei der Herstellung und Anwendung sogenannter Labor-entwickelter Tests (Laboratory developed Tests, LDTs).1,3,9
Zertifizierung
- Nachweis, dass ein Unternehmen ein definiertes QMS gemäß festgelegter Norm (z. B. DIN EN ISO 9001) besitzt.
- Systembewertung
Zertifizierungsstellen: z. B. TÜV, DEKRA Certification GmbH2,10
Akkreditierung
- Nachweis der technischen/fachlichen Kompetenz für bestimmte Tätigkeiten oder Prüfverfahren; umfasst auch Kompetenz und Validität der Prozesse (z. B. nach DIN EN ISO 15189 oder DIN EN ISO/IEC 17025).
- Fachliche Bewertung
Akkreditierungsstellen: DAkkS, ILAC6,10
Praktische Konsequenzen für medizinische Labore und Pathologien
Mit dem sogenannten Inhouse-Privileg dürfen Gesundheitseinrichtungen weiterhin eigene In-vitro-Diagnostika (Inhouse-IVD, IH-IVD) bzw. LDTs entwickeln und anwenden – vorausgesetzt, die Vorgaben des Artikels 5 (5) der IVDR werden vollständig erfüllt.11 Dazu zählt unter anderem die Forderung:
„Das Labor der Gesundheitseinrichtung entspricht der Norm DIN EN ISO 15189 oder gegebenenfalls nationalen Vorschriften einschließlich nationaler Akkreditierungsvorschriften.“11
Ein zertifiziertes Labor – etwa nach DIN EN ISO 9001 – genügt diesen Anforderungen nicht, da die Zertifizierung lediglich die formale Umsetzung eines QMS bestätigt, jedoch keine Aussage über die fachliche Kompetenz oder Validität diagnostischer Verfahren trifft.⁸ Für Labore, die Inhouse-IVDs einsetzen, ist daher eine Akkreditierung, typischerweise nach DIN EN ISO 15189, erforderlich. Sie dient dem Nachweis, dass Prüfverfahren wissenschaftlich valide, reproduzierbar und klinisch geeignet sind.11
Alle diagnostischen Labore – unabhängig vom Akkreditierungsstatus – müssen die grundlegenden Sicherheits- und Leistungsanforderungen gemäß Anhang I der IVDR einhalten. Diese Anforderungen umfassen unter anderem Produktdesign, Risikomanagement, Leistungsbewertung und klinische Evidenz.11
Labore ohne bestehende Akkreditierung müssen folgende Schritte umsetzen:
- Etablierung eines QMS nach DIN EN ISO 15189 oder DIN EN ISO/IEC 17020
- Systematische Erfassung der eingesetzten Inhouse-Verfahren (IH-IVD; LDTs)
- Entscheidung, welche IH-IVD weiterverwendet, und welche durch CE-IVDs ersetzt werden
- Validierung der IH-IVD (z.B. analytische Sensitivität, Spezifität, Robustheit)
- Verifizierung von CE-IVDs, wenn diese nicht in vollem Umfang dem vorgesehenen Anwendungszweck entsprechen
Ein Labor, das LDTs einsetzt, trägt die volle Verantwortung für die Einhaltung aller Anforderungen gemäß Artikel 5 (5) und Anhang I der IVDR – einschließlich der ordnungsgemäßen Leistungsbewertung.11 Je nach Ausgangslage eines Labors kann die Umsetzung dieser Anforderungen einen erheblichen strukturellen und personellen Anpassungsbedarf mit sich bringen.
Qualitätssicherung bei der HER2-Diagnostik
Die Qualität der eingesetzten Nachweisverfahren einschließlich Präanalytik und Auswertung soll durch interne und externe Qualitätssicherungsmaßnahmen bei den Laboren, die HER2-Testungen durchführen, sichergestellt werden.12–15
Interne Qualitätssicherungsmaßnahmen
Für eine zuverlässige und reproduzierbare HER2-Diagnostik werden u. a. folgende Maßnahmen empfohlen:14,15
Standardisiertes Vorgehen:
Verwendung standardisierter Protokolle
Verwendung standardisierter Kontrollen:
Integration von On-slide- und internen Kontrollen in jedem Testlauf
Färbeautomaten:
Nutzung automatisierter Systeme für die Immunhistochemie zur Minimierung von Fehlerquellen
Regelmäßige Qualitätskontrolle und Wartung:
Fortlaufende Überprüfung und Wartung aller Geräte
Schulung und Qualifikationsprüfung des Personals:
Kontinuierliche Weiterbildung und Überprüfung der Sachkunde aller Mitarbeitenden
Darüber hinaus ist es essenziell, die HER2-Testergebnisse stets mit dem histopathologischen Befund abzugleichen. Positive HER2-Befunde bei invasiven Karzinomen (G1) der folgenden histologischen Typen sind in der Regel nicht plausibel und sollten eine Re-Testung veranlassen:12,13,15
- Duktale oder lobuläre Karzinome mit positivem Hormonrezeptor-Status (Östrogenrezeptor, ER und/oder Progesteronrezeptor, PR)
- Tubuläre, muzinöse oder kribriforme Karzinome
- Adenoid-zystische Karzinome (typischerweise TNBC)
Kriterien für nicht verwertbare HER2 Test-Ergebnisse
Ein HER2 IHC-Ergebnis ist als nicht verwertbar einzustufen und sollte ggf. wiederholt werden, wenn eine der folgenden Bedingungen zutrifft:12,14
Die internen Kontrollen zeigen nicht das erwartete Ergebnis
Artefakte dominieren den überwiegenden Teil der Gewebeprobe
Normale Gangepithelien weisen eine unerwartet starke Membranfärbung auf (interne Positivkontrolle)
Ein HER2 ISH-Ergebnis gilt als nicht verwertbar und sollte wiederholt werden, wenn12,14
die Kontrollen nicht das erwartete Ergebnis liefern
< 2 Tumorareale beurteilbar sind
25 % der Signale zu schwach für eine sichere Auswertung sind
10 % der Signale zytoplasmatisch statt nukleär erscheinen
die nukleäre Auflösung schlecht ist
eine starke Autofluoreszenz vorliegt (bei FISH)
Abgleich mit der HER2-Positivitätsrate
Die zu erwartende HER2-Positivitätsrate beim invasiven Mammakarzinom liegt bei ca. 15 %.12,13,15 Zur Qualitätssicherung sollte die HER2-Positivitätsrate des eigenen Labors kontinuierlich dokumentiert und überprüft werden.12,13,15 Für typische Vergleichswerte kann sowohl die Bundesauswertung Mammachirurgie des Instituts für Qualitätssicherung und Transparenz im Gesundheitswesen (IQTIG) herangezogen werden als auch der HER2-Monitor des Instituts für Pathologie der Medizinischen Hochschule Hannover: https://webext.mh-hannover.de/pat/her2/login.php.
Externe Qualitätssicherungsmaßnahmen
Zur externen Qualitätssicherung werden u. a. folgende Maßnahmen empfohlen:12,15
Regelmäßige, erfolgreiche Teilnahme an externen Qualitätssicherungsmaßnahmen – insbesondere an Ringversuchen zur HER2-Diagnostik (IHC und ISH), die z. B. im Rahmen der Qualitätssicherungs-Initiative Pathologie (QuIP) der Deutschen Gesellschaft für Pathologie (DGP) und des Berufsverbandes Deutscher Pathologen (BDP) angeboten werden.
Über OnkoZert gibt es für Brustkrebszentren die Möglichkeit der Zertifizierung gemäß den „Fachlichen Anforderungen der Deutschen Krebsgesellschaft und der Gesellschaft für Seneologie“.15 Für Pathologien, die Kooperationspartner in Brustkrebszentren sind, steht ein eigener Erhebungsbogen "Pathologie" mit den Anforderungen an die Zertifizierung zur Verfügung.
Abkürzungen
BÄK: Bundesärztekammer; BDP: Berufsverband Deutscher Pathologen; CE: Conformité Euopéene; DAkkS: Deutsche Akkreditierungsstelle; DEKRA: Deutscher Kraftfahrzeug-Überwachungs-Verein; DGP: Deutsche Gesellschaft für Pathologie; DIN: Deutsches Institut für Normung; DSGVO: Datenschutz-Grundverordnung; EN: Europäische Norm; ER: Östrogenrezeptor; EU: Europäische Union; HER2: humaner epidermaler Wachstumsfaktor-Rezeptor 2; IEC: Internationale Elektrotechnische Kommission; IfSG: Infektionsschutzgesetz; IHC: Immunohistochemie; IH-IVD: Inhouse-In-vitro-Diagnostikum; ILAC: Internationale Kooperation von Akkreditierungsstellen; ISH: In-situ-Hybridisierung; ISO: Internationale Organisation für Normung; IVD: In-vitro-Diagnostikum; IVDR: In-vitro Diagnostik Verordnung; LDT: Laboratory Developed Test; PCR: Polymerase-Kettenreaktion; PR: Progesteronrezeptor; QM: Qualitätsmanagement; QMS: Qualitätsmanagement-System; QS: Qualitätssicherung; QulP: Qualitätssicherungs-Initiative Pathologie GmbH; Rili-BÄK: Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen; TAT: Turnaround Time; TNBC: triple-negatives Mammakarzinom; TÜV: Technischer Überwachungsverein
- Berufsverband Deutscher Pathologinnen und Pathologen e. V., et al. Berlin; 2025. Verfügbar unter pathologie.de/aktuelles/pressemitteilungen/2025/bundesaerztekammer-schafft-eigene-richtlinie-zur-qualitaetssicherung-in-der-pathologie. Letzter Zugriff: Januar 2026.
- Bundesärztekammer (2023). Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen. Verfügbar unter bundesaerztekammer.de/fileadmin/user_upload/BAEK/Themen/Qualitaetssicherung/_Bek_BAEK_RiLi_BAEK_ONLINE_FINAL_VERS_26_05_2023.pdf. Letzter Zugriff: Januar 2026.
- Deutsche Akkreditierungsstelle (2024). Regel zur Akkreditierung von medizinischen Laboratorien nach DIN EN ISO 15189:2024. Verfügbar unter https://www.dakks.de/files/Dokumentensuche/Dateien/R-15189_Akkreditierung%20von%20medizinischen%20Laboratorien.pdf. Letzter Zugriff: Januar 2026.
- Vogeser M, et al. Ger Med Sci 2025;23:Doc01.
- Deutsches Institut für Normung e. V. DIN EN ISO/IEC 17020 Konformitätsbewertung - Anforderungen an den Betrieb verschiedener Typen von Stellen, die Inspektionen durchführen (ISO/IEC 17020:2012). Verfügbar unter din.de/de/mitwirken/normenausschuesse/nqsz/veroeffentlichungen/wdc-beuth:din21:146320816. Letzter Zugriff: Januar 2026.
- Deutsche Akkreditierungsstelle. Medizinische Laboratoriumsdiagnostik 1 | Pathologie. Verfügbar unter dakks.de/de/fb-3.5.html. Letzter Zugriff: Januar 2026.
- Deutsches Institut für Normung e. V. DIN EN ISO 9001. Qualitätsmanagementsysteme - Anforderungen. Verfügbar unter din.de/de/wdc-beuth:din21:235671251. Letzter Zugriff: Januar 2026.
- Verordnung (EU) 2017/746 des Europäischen Parlaments und des Rates vom 5. April 2017 über In-vitro-Diagnostika und zur Aufhebung der Richtlinie 98/79/EG und des Beschlusses 2010/227/EU der Kommission (IVDR). Verfügbar unter eur-lex.europa.eu/legal-content/DE/TXT/HTML/?uri=CELEX:32017R0746&qid=1643555738061&from=DE. Letzter Zugriff: Januar 2026.
- Kahles A, et al. Pathologie (Heidelb) 2023;44(6):381–91.
- Deutsche Akkreditierungsstelle. Was ist Akkreditierung? Unterschiede zwischen Zertifizierung und Akkreditierung. Verfügbar unter dakks.de/de/was-ist-akkreditierung.html. Letzter Zugriff: Januar 2026.
- Regulation (EU) 2017/746 on in vitro diagnostic medical devices [Internet]. (2025). Verfügbar unter eur-lex.europa.eu/legal-content/DE/TXT/?uri=CELEX%3A02017R0746-20250110. Letzter Zugriff: Januar 2026.
- S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 5.0, Dez 2025. Verfügbar unter https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mammakarzinom_4_0/Version_5/LL_Mammakarzinom_Langversion_5.0.pdf. Letzter Zugriff: Januar 2026.
- Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.V. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlungen 2025.1D. Kapitel xy. Verfügbar unter https://www.ago-online.de/leitlinien-empfehlungen/leitlinien-empfehlungen/kommission-mamma. Letzter Zugriff: Januar 2026.
- Wolff AC, et al. J Clin Oncol 2023;41(22):3867-72.
- IQTIG – Institut für Qualitätssicherung und Transparenz im Gesundheitswesen. Berlin; 2021. Verfügbar unter iqtig.org/downloads/auswertung_begleitschreiben/IQTIG_Qualitaetsaspekte-der-HER2-Bestimmung-im-Rahmen-der-esQS_V1.4_Fragenkatalog_2021-01-05.pdf. Letzter Zugriff: Januar 2026.